
【題目】銅是人類發現最早并廣泛使用的一種金屬。回答下列問題:
(1)實驗室使用稀硫酸和H2O2溶解銅片,該反應的離子方程式為___。
(2)電子工業使用FeCl3溶液刻蝕印刷電路板銅箔,寫出該反應的化學方程式___。配制FeCl3溶液和FeCl2溶液都應保持___(填“酸性”“堿性”或“中性”),原因是___。配制FeCl2溶液時還應加入少量鐵屑,原因是___。
(3)溶液中Cu2+的濃度可采用碘量法測得:
①2Cu2++5I-=2CuI↓+I3- ②I3-+2S2O32-=3I-+S2O62-
反應①中的還原產物為___。現取10.00mL含Cu2+的溶液,加入足量KI充分反應后,用0.1000mol·L-1Na2S2O3標準溶液滴定至終點,消耗Na2S2O3溶液12.50mL,此溶液中Cu2+的濃度為___mol·L-1。
【答案】Cu+H2O2+2H+=Cu2++2H2O 2FeCl3+Cu=2FeCl2+CuCl2 酸性 抑制Fe3+、Fe2+水解 防止Fe2+被空氣中的氧氣氧化 CuI 0.125
【解析】
(1)稀硫酸具有氧化性,實驗室使用稀硫酸和H2O2溶解銅片生成硫酸銅和水;
(2)鐵離子具有氧化性,電子工業使用FeCl3溶液刻蝕印刷電路板銅箔,生成氯化亞鐵和氯化銅; 根據Fe3+、Fe2+都易水解分析;Fe2+具有還原性,易被氧氣氧化;
(3)根據元素化合價升降判斷還原產物;根據關系式2S2O32-~~~I3-~~~2Cu2+計算Cu2+的濃度。
(1)實驗室使用稀硫酸和H2O2溶解銅片生成硫酸銅和水,反應的離子方程式是Cu+H2O2+2H+=Cu2++2H2O;
(2)電子工業使用FeCl3溶液刻蝕印刷電路板銅箔,生成氯化亞鐵和氯化銅,反應的化學方程式是2FeCl3+Cu=2FeCl2+CuCl2;Fe3+、Fe2+都易水解,保持溶液呈酸性,可以抑制Fe3+、Fe2+水解;Fe2+具有還原性,易被氧氣氧化,為防止Fe2+被空氣中的氧氣氧化,配制FeCl2溶液時還應加入少量鐵屑;
(3)2Cu2++5I-=2CuI↓+I3-反應中銅元素化合價由+2降低為+1,還原產物是CuI;
設溶液中Cu2+的濃度為c;
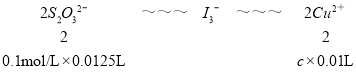
![]() =0.125mol/L。
=0.125mol/L。


 培優三好生系列答案
培優三好生系列答案 優化作業上海科技文獻出版社系列答案
優化作業上海科技文獻出版社系列答案科目:高中化學 來源: 題型:
【題目】某溫度(T ℃)時,測得0.01 mol·L-1NaOH溶液的pH=11,則該溫度下水的Kw=________。在此溫度下,將pH=a的NaOH溶液VaL與pH=b的H2SO4溶液VbL混合。
(1)若所得混合液為中性,且a=11,b=3,則Va∶Vb=__________。
(2)若所得混合液為中性,且Va∶Vb=10∶1,則a+b=__________。
(3)若所得混合液的pH=10,且a=12,b=2,則Va∶Vb=__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下列物質的溶液:①CH3COOH ②HCl ③H2SO4 ④NaHSO4
(1)若四種溶液的物質的量濃度相同,其c(H+)的大小比較為____________(用序號表示,下同)。
(2)將6 g CH3COOH溶于水制成1 L溶液,此溶液的物質的量濃度為___________,經測定溶液中c(CH3COO-)為1.4×10-3 mol/L,此溫度下醋酸的電離常數Ka=____________,溫度升高,Ka將_____(填“變大”“不變”或“變小”,下同),加入少量CH3COONa后c(H+)______,Ka______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業廢氣H2S經資源化利用后可回收能量并得到單質硫。反應原理為2H2S(g)+O2(g)=S2(s)+2H2O(l) ΔH=-632 kJ·mol-1。H2S燃料電池的工作原理如圖所示。下列有關說法不正確的是( )

A.電極a為電池的負極
B.電極b上的電極反應式為O2+4H++4e-===2H2O
C.若電路中通過2 mol電子,則電池內部釋放632 kJ熱能
D.若有17 g H2S參與反應,則會有1 mol H+經質子膜進入正極區
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,體積相同、濃度均為1.0 mol·L–1的HX溶液、HY溶液,分別加水稀釋,稀釋后溶液的pH隨稀釋倍數的對數的變化如圖所示,下列敘述正確的是( )
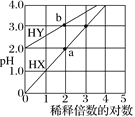
A.HX是強酸,溶液每稀釋10倍,pH始終增大1
B.常溫下HY的電離常數約為1.0×10–4
C.溶液中水的電離程度:a點大于b點
D.消耗同濃度的NaOH溶液體積:a點大于b點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】砷(As)原子序數為33,可以形成As2S3、As2O5、H3ASO3、H3AsO4等化合物,有著廣泛的用途。回答下列問題:
(1)砷在周期表中的位置為第___周期___族。
(2)工業上常將含砷廢渣(主要成分為As2S3)制成漿狀,通入O2氧化,生成H3AsO4和單質硫。若反應生成6mol單質硫,則需要___molO2。該反應需要在加壓下進行,原因是___。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3ASO4(s) △H1
H2(g)+2O2(g)=H3ASO4(s) △H1
H2(g)+![]() O2(g)=H2O(l) △H2
O2(g)=H2O(l) △H2
2As(s)+![]() O2(g)=As2O5(s) △H3
O2(g)=As2O5(s) △H3
則反應2H3AsO4(s)=As2O5(s)+3H2O(l)的△H=___。
(4)298K時,將10mL3xmol·L-1Na3AsO3、10mL3xmol·L-1I2和10mLNaOH溶液混合,發生反應:AsO33-(aq)+I2(aq)+2OH-(aq)=AsO43-(aq)+2I-(aq)+H2O(l)。溶液中c(AsO43-)與反應時間(t)的關系如圖所示。

①下列可判斷反應達到平衡的是___(填標號)。
a.v(OH-)=2v(AsO33-)
b.I2的濃度不再變化
c.![]() 不再變化
不再變化
d.c(I-)=ymol·L-1
②tm時,v正___v逆(填“大于”“小于”或“等于”)。
③圖中m點和n點的逆反應速率較大的是___。
④若平衡時溶液的c(H+)=10-14mol/L,則該反應的平衡常數K為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上用鈦白渣[主要成分為FeSO4,還含有少量Fe2(SO4)3、MgSO4及TiOSO4]為主要原料生產氧化鐵黃(FeOOH)的一種工藝流程如下:
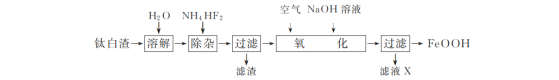
(1)“溶解”時,TiOSO4發生水解生成難溶于水的H2TiO3,反應的化學方程式為________。
(2)“除雜”時,加入NH4HF2固體的作用是________。
(3)“氧化”時,Fe2+生成FeOOH的離子方程式是________。
(4)濾液X中主要含有的陽離子是________(填化學式)。
(5)實驗測得反應溶液的pH、溫度對氧化鐵黃產率的影響如圖所示。
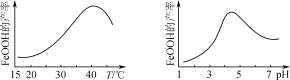
①反應溫度宜選擇________。
②氧化時應控制pH的合理范圍是4.5左右,pH過小或過大均會導致氧化鐵黃產率較低,其可能原因是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了配制NH4+濃度與Cl-的濃度比為1:1的溶液,可在NH4Cl溶液中加入:①適量HCl②適量NaCl③適量的氨水④適量的NaOH,正確的是
A. ①② B. ④ C. ③④ D. ③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2.3g乙醇和一定量的氧氣混合點燃,恰好完全燃燒,放出熱量為68.35kJ。
(1)該反應的熱化學方程式為___。
(2)已知:
化學鍵 | Si-Cl | H-H | H-Cl | Si-Si |
鍵能/kJ·mol-1 | 360 | 436 | 431 | 176 |
且硅晶體中每個硅原子和其他4個硅原子形成4個共價鍵。
工業上所用的高純硅可通過下列反應制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g),該反應的反應熱為___kJ·mol-1。
Si(s)+4HCl(g),該反應的反應熱為___kJ·mol-1。
(3)已知水的比熱容為4.2×10-3kJ·g-1·℃-1。8g硫黃在O2中完全燃燒生成氣態SO2,放出的熱量能使500g H2O的溫度由18℃升至58℃,則硫黃燃燒熱的熱化學方程式為___。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com