
(12分)某無色透明溶液中可能存在大量Ag+、Mg2+、K+、Cu2+中的一種或幾種,請填寫下列空白。
(1)不用做任何實驗就可以肯定溶液中不存在的離子是________________。
(2)取少量原溶液,加入過量稀鹽酸,有白色沉淀生成,再加入過量稀硝酸,沉淀不消失,說明原溶液中肯定存在的離子是________,反應的離子方程式為_______________。
(3)取(2)的濾液加過量的NaOH溶液,出現白色沉淀,說明原溶液中肯定有________,有關反應的離子方程式為________________。
(4)原溶液中可能大量存在的陰離子是
| A.Cl- | B.NO3- | C.CO3 2- | D.OH- |
(共12分)
(1)Cu2+;
(2)Ag+;Ag++Cl—=AgCl↓
(3)Mg2+;Mg2++2OH—= Mg(OH)2↓
(4)B (多選不得分)
解析試題分析:(1)、含有大量Cu2+的溶液顯藍色,則無色溶液中一定不存在Cu2+;(2)、Cl—與Ag+反應,生成白色的AgCl沉淀,不溶于水和稀硝酸,則實驗(2)說明原溶液中肯定存在Ag+,原因是Ag++Cl—=AgCl↓;(3)、由于稀鹽酸過量,實驗(2)所得濾液中無Ag+,OH—先與H+反應,生成水,OH—后與Mg2+反應,生成白色的Mg(OH)2沉淀,則實驗(3)說明原溶液中肯定有Mg2+,有關反應為OH—+H+= H2O、Mg2++2OH—= Mg(OH)2↓;(4)、Cl—與Ag+反應,則原溶液不可能含有大量的Cl—,A項錯誤;NO3-與Ag+、Mg2+均不能反應,無沉淀、氣體和水生成,B項正確;CO3 2-與Ag+、Mg2+均能反應,生成白色沉淀,C項錯誤;OH-與Ag+、Mg2+均能反應,生成白色沉淀,D項錯誤。
考點:考查離子的性質、離子方程式、離子共存、離子推斷等相關知識。


科目:高中化學 來源: 題型:填空題
有A、B、C、D四種溶液,它們是燒堿、硫酸、碳酸氫銨、氯化銅溶液中的某一種。各取少量,將其兩兩混合,其中A、B混合有藍色絮狀沉淀生成, C 與足量B或D混合均有無色氣體產生。根據題意回答下列問題:
(1)B、C分別是 、
(2)向A中滴加B,離子方程式:
向C中滴加D,離子方程式:
(3)少量B和C混合,現象:________,離子方程式:_______________________________。
(4)上述三個反應均屬于________________反應(填基本反應類型),反應發生的條件的不同點是 ;相同點是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在Na+濃度為0.5mol/L的某澄清溶液中,還可能含有下表中的若干種離子:
| 陽離子 | K+、Ag+、Mg2+、Ba2+ |
| 陰離子 | NO3-、CO32-、SiO32-、SO42- |
| 序號 | 實驗內容 | 實驗結果 |
| Ⅰ | 向該溶液中加入足量稀HCl | 產生白色沉淀并放出0.56L氣體 |
| Ⅱ | 將Ⅰ的反應混合液過濾,對沉淀洗滌、灼燒至恒重,稱量所得固體質量 | 固體質量為2.4g |
| Ⅲ | 在Ⅱ的濾液中滴加BaC12溶液 | 無明顯現象 |
| 陰離子 | NO3- | CO32- | SiO32- | SO42- |
| c/mol·L-1 | | | | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某強酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42ˉ、SiO32ˉ、NO3ˉ中的一種或幾種離子,取該溶液進行實驗,其現象及轉化如下圖。反應過程中有一種氣體是紅棕色。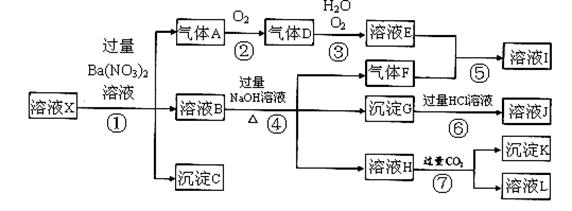
請回答下列問題:
(1)由強酸性條件即可判斷溶液X中一定不存在的離子有 :
(2)溶液X中,關于NO3ˉ的判斷一定正確的是 ;
a.一定有 b.一定沒有 c.可能有
(3)產生氣體A的離子方程式為 ;
(4)轉化⑥發生反應的現象為 ;
(5)轉化④中產生H的離子方程式為 ;
(6)若轉化③中,D、H2O、O2三種物質恰好發生化合反應生成E,則反應中D與O2的物質的量之比
為 ;
(7)對不能確定是否存在的離子,可以另取X溶液,加入下列溶液中的一種,根據現象即可判斷,該試劑最好是 。
①NaOH溶液, ②KSCN溶液, ③石蕊試劑, ④pH試紙,⑤KMnO4溶液,
⑥氯水和KSCN的混合溶液
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某無色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO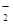 、MnO
、MnO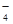 、CO
、CO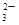 、SO
、SO 中的若干種離子組成,取溶液進行右圖實驗:
中的若干種離子組成,取溶液進行右圖實驗: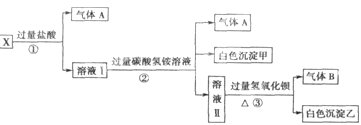
(1)白色沉淀甲是 。
(2)X溶液中一定存在的離子是 。
(3)白色沉淀乙中一定有: ,可能有 。
(4)若將過量的氣體A與適量的氣體B通入水中,寫出反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
按要求完成以下方程式:
(1)磁性氧化鐵溶于鹽酸的化學方程式:_________________________________________。
(2)氯化鐵溶液中通入SO2氣體的離子方程式:_______________ ____________________。
(3)偏鋁酸鈉溶液中通入過量CO2的離子方程式:_________________________________。
(4)碳單質和濃硝酸反應的化學方程式:_________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
某實驗小組為探究ClO-、I2、SO42-在酸性條件下的氧化性強弱,設計實驗如下:
實驗①:在淀粉碘化鉀溶液中加入少量次氯酸鈉溶液,并加入少量的稀硫酸,溶液立即變藍;
實驗②:向實驗①的溶液中加入4 mL 0.5 mol/L的亞硫酸鈉溶液,藍色恰好完全褪去。
(1)寫出實驗①中發生反應的離子方程式:______________________________________________。
(2)實驗②的化學反應中轉移電子的物質的量是________。
(3)以上實驗說明,在酸性條件下ClO-、I2、SO42-的氧化性由弱到強的順序是________
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
(10分)完成下列離子方程式
(1)硫酸酸化的高錳酸鉀溶液與草酸反應
(2)硫代硫酸鈉與硫酸反應
(3)硫酸溶液與淀粉碘化鉀溶液混合在空氣中放置一段時間
(4)K2Cr2O7的溶液中存在的平衡
(5)氯化鐵與硫氰化鉀溶液反應
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
根據下列反應事實:①X+Y2+=X2++Y;②Z+2H2O(冷)=Z(OH)2+H2↑;
③Z2+氧化性比X2+弱;④由Y、W電極組成的電池,電極反應為W2++2e-=W、
Y-2e-=Y2+,可知X、Y、Z、W的還原性由強到弱的順序為
| A.X>Z>Y>W | B.Z>W>X>Y | C.Z>Y>X>W | D.Z>X>Y>W |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com