
(10分)化工生產中常用到“三酸兩堿”,“三酸”指硝酸、硫酸和鹽酸,“兩堿”指燒堿和純堿。
(1) 從物質的分類角度看,不恰當的一種物質是________。(填寫化學式)
(2) "三酸”的稀溶液均能作為NH3的吸收劑廣三酸”中的任意“一酸”與KH3反應的離子方程式是________________________________
(3) 純堿生產工藝是沿用化學家侯德榜改革國外的純堿生產工藝,其生產流程可簡要表示如下:
①沉淀池中發生的化學反應方程式是________________
②使原料氯化鈉的利用率從70%提高到90%以上,主要是設計了循環________ (填“ I ”或“II”)。
(4) 若將1mol/L鹽酸逐滴加入0.5mol/L燒堿溶液至恰好完全中和,所得溶液中的離子濃度大小順序是________________________
科目:高中化學 來源: 題型:
(10分)現代化學工業遵循可持續發展原則,利用淀粉、纖維素等可再生資源合成多種化工產品。
⑴ 以淀粉為原料可制取香料乙酸乙酯,生產流程為:
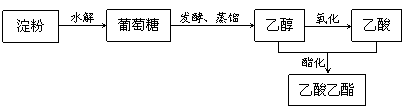 |
① 部分鏈狀葡萄糖分子在水溶液中通過分子內加成反應,以六元環或五元環的形式存在,其中六元環
的結構為 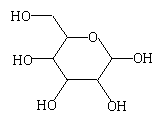 ,則葡萄糖在水溶液存在的五元環結構為 。
,則葡萄糖在水溶液存在的五元環結構為 。
② 若用1000 kg 含(C6H10O5)n 90%的淀粉(雜質不參與反應)為原料制取乙酸乙酯。生產中,淀粉的水解率為90%,乙醇的產率為85%,酯化反應中乙醇、乙酸的轉化率均為90%。計算生產中得到的乙酸乙酯的質量(kg)。
⑵ 纖維素的結構可表示為[(C6H7O2)(OH)3]n。10.00 g脫脂棉花(纖維素含量為100%)與乙酸、乙酸酐[(CH3CO)2O]的混合物在一定條件下發生酯化反應,可制得15.19 g醋酸纖維 (纖維素乙酸酯)。請通過計算推斷該醋酸纖維的結構簡式。
查看答案和解析>>
科目:高中化學 來源: 題型:
(08六都中學模擬)(10分)二氧化硫和氮的氧化物是常用的化工原料,但也是大氣的主要污染物。綜合治理其污染是環境化學當前的重要研究內容之一。
(1)硫酸生產中,SO2催化氧化生成SO3: 2SO2(g)+O2(g)![]() 2SO3(g)。某溫度下,SO2的平衡轉化率(a )與體系總壓強(p)的關系如圖所示。根據圖示回答下列問題:
2SO3(g)。某溫度下,SO2的平衡轉化率(a )與體系總壓強(p)的關系如圖所示。根據圖示回答下列問題:
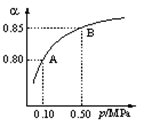
①將2.0 mol SO2和1.0 mol O2置于10 L密閉容器中,反應達平衡后,體系總壓強為0.10 MPa。該反應的平衡常數等于____________。
②平衡狀態由A變到B時,平衡常數K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化還原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g) = 4NO(g)+CO2(g)+2H2O(g);DH =-574 kJ/mol
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g);DH =-1160 kJ/mol
若用標準狀況下4.48 L CH4還原NO2至N2,整個過程中轉移的電子總數為_____________(阿伏加德羅常數的值用NA表示),放出的熱量為_________kJ。
(3)新型納米材料氧缺位鐵酸鹽(MFe2Ox,3<x<4,M = Mn、Co、Zn或Ni)由鐵酸鹽(MFe2O4)經高溫還原而得,常溫下,它能使工業廢氣中的酸性氧化物分解除去。轉化流程如圖所示:

請寫出MFe2Ox分解SO2的化學方程式______________________________________(不必配平)。
查看答案和解析>>
科目:高中化學 來源: 題型:
水煤氣是重要
燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:
C (s) + H2O(g) ![]() CO (g) +H2 (g) △H= +131.3 kJ•mol-1
CO (g) +H2 (g) △H= +131.3 kJ•mol-1
(1)實際工業生產中,向炭層間隔交替通入水蒸氣和空氣,其原因是 。
(2)一定溫度下,三個容器中均進行著上述反應,各容器中炭足量,其它物質的物質的量濃度及正逆反應速率關系如下表所示。請填寫表中相應的空格。
| 容器編號 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | ν正、ν逆比較 |
| I | 0.06 | 0.60 | 0.10 | ν正=ν逆 |
| Ⅱ | 0.12 | 0.20 | ________ | ν正=ν逆 |
| Ⅲ | 0.10 | 0.20 | 0.40 | ν正____ν逆 |
(3)生物乙醇可由淀粉或纖維素等生物質原料發酵獲得。利用乙醇可進而獲得合成氣(CO、H2)。
用乙醇生產合成氣有如下兩條路線:
a、水蒸氣催化重整:CH3CH2OH(g)+H2O(g)→4H2(g)+2CO(g)
b、部分催化氧化:CH3CH2OH(g)+1/2O2(g)→3H2(g)+2CO(g)
某生物質能研究所準備利用乙醇得到的合成氣合成一種生物汽油。乙醇各分一半按a、b兩式反應。合成氣合成生物汽油的反應為:2mCO+(2m+n)H2→2CmHn+2mH2O。假定合成的生物汽油中含有X、Y兩種成分,且X、Y都是有8個碳原子的烴,X是苯的同系物,Y是烷烴。
①X的分子式為 ,Y的分子式為 。
②50噸質量分數為92%的乙醇經上述轉化(假定各步轉化率均為100%),則最終可獲得X的質量為多少噸?
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com