
���}Ŀ��������еĵ����ϳɰ��ǾS�ֵ�����������������D(zhu��n)���^�̣�����҇��ɹ����Ƴ���Ч늴��̵�����Mo2N���������Ƴɹ�����Ч��ߵ������a(ch��n)Ч�ʡ�
�ش����І��}��
��1���f(Mo)λ�ڵ������ڣ��c�tͬ���壬�tMo�ăr����Ų�ʽ��______________��
��2�����B(t��i)��ԭ�Ӻ�����ӿ��g�\�Ӡ�B(t��i)��____�N����Ԫ�����������е�һ��x������ǰ���NԪ��������____�����ɴ�С�����?q��)����?/span>
��3����Ԫ�����γ�һϵ�еĻ������NH3��HN3���Y(ji��)��(g��u)ʽ��![]() ����H2NCH2COOH�ȡ�NH3�ķ��Ә�(g��u)�͞�________��HN3�Y(ji��)��(g��u)ʽ���g�ɂ���ԭ�ӵ��s��܉����͞�________��1��HN3�����к�______�����I��H2NCH2COOH�����c��182 �棩��CH3CH2COOH�����c��22 �棩�����������|(zh��)������ͬ�������c���ܴ����|(zh��)�Y(ji��)��(g��u)�ĽǶȷ���������ԓ�F(xi��n)�����Ҫԭ����______��
����H2NCH2COOH�ȡ�NH3�ķ��Ә�(g��u)�͞�________��HN3�Y(ji��)��(g��u)ʽ���g�ɂ���ԭ�ӵ��s��܉����͞�________��1��HN3�����к�______�����I��H2NCH2COOH�����c��182 �棩��CH3CH2COOH�����c��22 �棩�����������|(zh��)������ͬ�������c���ܴ����|(zh��)�Y(ji��)��(g��u)�ĽǶȷ���������ԓ�F(xi��n)�����Ҫԭ����______��
��4�����c�KԪ���γɵ�ij�N�����ᄃ����D��ʾ���tԓ������Ļ��Wʽ��______����ԓ������߅�L��d pm���t���w���ܶȞ�____ g/cm3��

���𰸡�4d55s1 7 Ne>F>N �����F�� sp2��sp 3 H2NCH2COOH�����g�γɵĚ��I��(sh��)Ŀ��CH3CH2COOH�����g�γɵĚ��I��(sh��)Ŀ�� PtN2 ![]()
��������
��1���t�ǵ�������Ԫ�أ���r����Ų�ʽ��3d54s1���f(Mo)�c�tͬ���壬�tMo�ăr����Ų�ʽ��4d55s1��
��2��ԭ�Ӻ��������һ����ӵ��\�Ӡ�B(t��i)����ͬ���ʻ��B(t��i)��ԭ�Ӻ�����ӿ��g�\�Ӡ�B(t��i)��7�N���ɵ�һ��x���f׃Ҏ(gu��)��֪���ڶ����ڵ�һ��x������ǰ���NԪ��������Ne��F��N���𰸞飺7��Ne>F>N��
��3��NH3�������F�η��ӣ�![]() ���c����I�ĵ�ԭ���γ���2�����I��߀��һ������ӌ���������sp2�s�������g�ĵ�ԭ���γ���2�����I���o����ӌ����ʞ�sp�s����1��HN3���������I����3����H2NCH2COOH��CH3CH2COOH�ɷN�������������|(zh��)�����1���ʷ����A������ͬ�����߷����g�����γɚ��I����ǰ�߷����д��ڃɷN���γɚ��I�Ĺ��r�I��N��H��O��H������ֻ��һ��O��H����ǰ�߷����g���I��(sh��)Ŀ�Ⱥ��ߵĶ࣬�������c�Ⱥ��߸ߣ��𰸞飺�����F�Σ�sp2��sp��3��H2NCH2COOH�����g�γɵĚ��I��(sh��)Ŀ��CH3CH2COOH�����g�γɵĚ��I��(sh��)Ŀ�ࡣ
���c����I�ĵ�ԭ���γ���2�����I��߀��һ������ӌ���������sp2�s�������g�ĵ�ԭ���γ���2�����I���o����ӌ����ʞ�sp�s����1��HN3���������I����3����H2NCH2COOH��CH3CH2COOH�ɷN�������������|(zh��)�����1���ʷ����A������ͬ�����߷����g�����γɚ��I����ǰ�߷����д��ڃɷN���γɚ��I�Ĺ��r�I��N��H��O��H������ֻ��һ��O��H����ǰ�߷����g���I��(sh��)Ŀ�Ⱥ��ߵĶ࣬�������c�Ⱥ��߸ߣ��𰸞飺�����F�Σ�sp2��sp��3��H2NCH2COOH�����g�γɵĚ��I��(sh��)Ŀ��CH3CH2COOH�����g�γɵĚ��I��(sh��)Ŀ�ࡣ
��4�������K�ľ�����Pt�Ĕ�(sh��)Ŀ�飺8��![]() +6��
+6��![]() =4��N�Ă���(sh��)��8���ʵ����K�Ļ��Wʽ��PtN2��һ�������к���4����PtN2������һ���������|(zh��)����
=4��N�Ă���(sh��)��8���ʵ����K�Ļ��Wʽ��PtN2��һ�������к���4����PtN2������һ���������|(zh��)����![]() ��223 g���������w�e��(1010d)3 cm3���ɴ˿�������ܶȣ��𰸞飺PtN2��
��223 g���������w�e��(1010d)3 cm3���ɴ˿�������ܶȣ��𰸞飺PtN2��![]() ��
��


 ��У�n��ϵ�д�
��У�n��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��![]() ���~��ӡˢ������ӡˢ�·�~�帯�g������Ҫ��ش����І��}��
���~��ӡˢ������ӡˢ�·�~�帯�g������Ҫ��ش����І��}��
(1)�Ȼ��F��Һ���g�~����x�ӷ���ʽ�� ______ ��
(2)��5��6����Ȼ��F��Һ���뵽25mL��ˮ�У��^�m(x��)�ӟᣬ�üt��ɫҺ�w��
�����������x�ӷ���ʽ�� ______ ��
(3)��100mL![]() �����X�@
�����X�@![]() ��Һ����ε���
��Һ����ε���![]()
![]() ��Һ���S��
��Һ���S��![]() ��Һ�w�eV��׃�����������|(zh��)����n��׃����D��ʾ��
��Һ�w�eV��׃�����������|(zh��)����n��׃����D��ʾ��
��Ո�J��˼���������������x�ӷ���ʽ��
OA�Σ� ______
OB�Σ� ______
BC�Σ� ______
CD�Σ� ______

�ڮ�![]() �x��ǡ��ȫ������r������
�x��ǡ��ȫ������r������![]() ���|(zh��)������ ______ mol��
���|(zh��)������ ______ mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��[���W�����x��5���ЙC���W���A]��Ȳ�N�ڴ��������¿ɰl(f��)��ż(li��n)�������Q��Glaser������
2R��C��C��H![]() R��C��C��C��C��R+H2
R��C��C��C��C��R+H2
ԓ�������о����Ͱl(f��)����ϡ������ӻ��W�ȷ��������Ҫ�rֵ������������Glaser�����Ƃ仯����E��һ�N�ϳ�·����

�ش����І��}��
��1��B�ĽY(ji��)��(g��u)��ʽ��______��D �Ļ��W���Q��______��
��2���������ķ�����ͷքe��______��______��
��3��E�ĽY(ji��)��(g��u)��ʽ��______����1 mol E�ϳ�1,4���������飬��Փ����Ҫ���Ě��_______mol��
��4�������![]() ��Ҳ�ɰl(f��)��Glaserż(li��n)�������ɾۺ��ԓ�ۺϷ����Ļ��W����ʽ��_____________________________________��
��Ҳ�ɰl(f��)��Glaserż(li��n)�������ɾۺ��ԓ�ۺϷ����Ļ��W����ʽ��_____________________________________��
��5�����㻯����F��C��ͬ�֮���(g��u)�w���������ֻ�ЃɷN��ͬ���W�h(hu��n)���Ě䣬��(sh��)Ŀ�Ȟ�3:1����������3�N�ĽY(ji��)��(g��u)��ʽ_______________________________��
��6��������2�����Ҵ���ԭ�ϣ������o�Cԇ�����x���Ƃ仯����D�ĺϳ�·��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ij�W��������֪���|(zh��)������ȵ��}���y��δ֪���|(zh��)������ȵ�NaOH��Һ�r���x���̪��ָʾ����Ո?zh��)���пհף?/span>
��1���ζ��K�c���Дࣺ��Һ��_____________��
��2�����в����п���ʹ���yNaOH��Һ�ĝ�Ȕ�(sh��)ֵƫ�͵�����_____��
A����ʽ�ζ���δ�ؘ��}�ϴ��ֱ��ע��˜��}��
B���ζ�ǰʢ��NaOH��Һ���F��ƿ�����sˮϴ����]�и���
C����ʽ�ζ����ڵζ�ǰ�К��ݣ��ζ��������ʧ
D���xȡ�}���w�e�r���_ʼ��ҕ�x��(sh��)���ζ��Y(ji��)���r��ҕ�x��(sh��)
��3�����ζ��_ʼ�ͽY(ji��)���r����ʽ�ζ����е�Һ����D��ʾ���t�����}����Һ���w�e��_________mL��

��4��ij�W������(j��)3�Ό��քeӛ����P��(sh��)��(j��)�����
�ζ� �Δ�(sh��) | ���yNaOH��Һ���w�e/mL | 0.1000 mol/L�}����w�e/mL | ||
�ζ�ǰ�̶� | �ζ���̶� | ƽ�������}�� �w�e/mL | ||
��һ�� | 25.00 | 0.00 | 26.15 | ��V=__________ |
�ڶ��� | 25.00 | 0.56 | 30.30 | |
������ | 25.00 | 0.20 | 26.35 | |
������(j��)�ϱ픵(sh��)��(j��)Ӌ��ԓNaOH��Һ�����|(zh��)�������________ (Ӌ��Y(ji��)��ȡ4λ��Ч��(sh��))��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��һ���ض��£���10 mL 0.40 mol��L-1 H2O2��Һ�м����m��FeCl3��Һ����ͬ�r�̜y������O2���w�e���������˜ʠ�r�����±���ʾ��
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
�Y���@ʾ�������փɲ��M�У�
��2Fe3++ H2O2 ![]() 2Fe2++O2��+2H+
2Fe2++O2��+2H+
�� H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
�����^��������׃�����҈D��ʾ�������f�������_����

A. 0��6 min��ƽ���������ʣ�v(H2O2) = 3.33��10-2 mol��L-1��min-1
B. Fe3+�������Ǽӿ��^������ķֽ�����
C. �����������ᷴ�����������Ƿşᷴ��
D. ����2H2O2(aq)![]() 2H2O(l) + O2(g)�ġ�H =E1-E2 < 0
2H2O(l) + O2(g)�ġ�H =E1-E2 < 0
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��HBr��һ�N��Ҫ�Ĺ��I(y��)ԭ�ϣ������Á����a(ch��n)�t(y��)��ˎƷ���ϳ�Ⱦ�ϻ����ϣ�����ʯ�ͻ����Ĵ����ȡ���D�ǹ��I(y��)�Ƃ�HBr��һ�N���a(ch��n)���̣�

��1�����wa��ȼú���I(y��)�ğ�������I(y��)���a(ch��n)�����β��ijɷ֣��Y(ji��)�Ͽ�D��Ϣ���Д����wa�ķ���ʽ��___���������мӵ�ˮ��___��������ˮ��������ˮ������ԭ����___��
��2��ԇ��b�麬�ȵ��}��b��___���û��Wʽ��ʾ������Ϣڵ�Ŀ����___���ڶ������s�������c����Һ����c��___��
��3�����a(ch��n)�����в���A�����Q___������������s��������___���M�еġ�������x�����Q��
��4�����I(y��)���a(ch��n)���ƵõĚ����Ꭷ�е������Sɫ�����Ǽס��҃�ͬ�W�OӋ�ˌ�����̽�����ټ�ͬ�W���O���I(y��)������ʵ��Sɫ����麬��Fe3+���t�����C��ԓ���O���õ�ԇ����___����Wʽ���������O�������^�쵽�ĬF(xi��n)���___��
����ͬ�W���O���I(y��)������ʵ��Sɫ��������к����s�|(zh��)___�������C��ԓ���O�����ķ�����___�����Ό������E����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ����늽��|(zh��)��ˮ��Һ�д�����xƽ�⡣
��1�������dz�Ҋ�����ᡣ
�ٴ�����ˮ��Һ�е���x����ʽ�� ___________________��
�����з����У�����ʹ����ϡ��Һ�� CH3COOH ��x�̶�������� __________________������ĸ��̖����
a �μ��������}�� b ����Һ c ��ˮϡ� d �������������c���w
��2���� 0.1 mol��L-1NaOH ��Һ�քe�ζ��w�e���� 20.00 mL����Ⱦ��� 0.1 mol��L-1���}��ʹ�����Һ���õ��ζ��^������Һ pH�S���� NaOH��Һ�w�e��׃���ăɗl�ζ�������

�ٵζ������������_______________������I������II������
���Ҝؕr���� 0.1 mol��L-1�Ĵ������x�Ȟ� 1%��Ӌ���@������Һ�� pH ֵ________��
�۵ζ��_ʼǰ�����N��Һ����ˮ��x���� c(H+)������________________��
�������� 0.1 mol��L-1�� NaOH ��Һ�ζ� 0.1 mol��L-1���}�ᣬ���в��������_����________________��
A���ؘ� NaOH ��Һ��ϴ�Aʽ�ζ��ܺ����b��˜ʉA��Һ
B���ô��y����Һ��ϴ�F��ƿ�����b����y����Һ
C���ζ��r���ۑ�עҕ�ζ�����Һ���׃��������ζ��^��
D���x��(sh��)�r��ҕ�����c�ζ��ܰ�Һ�������c����ˮƽ
�������ζ��÷�̪��ָʾ�����ζ��K�c�ĬF(xi��n)��_______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���������P늽��|(zh��)��Һ���f�����_���ǣ�������
A.���}���м��백ˮ�����ԣ���Һ�� ��1
��1
B.������Һ�͚������c��Һǡ�÷�������Һ��![]() >1
>1![]()
C.��0.1molL-1CH3COOH��Һ�м�������ˮ����Һ��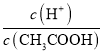 �pС
�pС
D.��CH3COONa��Һ��20��������30������Һ��![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ijԭ늳��b����D��ʾ���������P�����У����_����
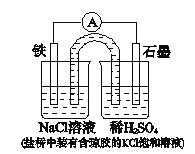
A.Fe�����O���l(f��)����������
B.ؓ�O������ 2H+ + 2e����H2��
C.����һ�Εr�g�ɟ�������ҺpH����׃
D.����һ�Εr�g��NaCl��Һ��c(Cl��)����
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com