
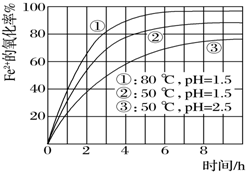
 為了研究一定濃度Fe2+的溶液在不同條件下被氧氣氧化的氧化率,實驗結果如圖所示,判斷下列說法錯誤的是( )
為了研究一定濃度Fe2+的溶液在不同條件下被氧氣氧化的氧化率,實驗結果如圖所示,判斷下列說法錯誤的是( )| A. | pH越小氧化率越小 | |
| B. | 溫度越高氧化率越大 | |
| C. | Fe2+的氧化率除受pH、溫度影響外,還受其它因素影響,如濃度等 | |
| D. | 實驗說明降低pH、升高溫度有利于提高Fe2+的氧化率 |
分析 由圖象知,當pH值等其它條件相同溫度不同時,溫度越高Fe2+的氧化率越大;當溫度和其它條件相同PH值不同時,pH值越大,Fe2+的氧化率越小,據此分析解答.
解答 解:A.根據圖象知,只有當溫度和其它條件相同PH值不同時,pH值越小,Fe2+的氧化率越大,故A錯誤;
B.只有當pH值等其它條件相同溫度不同時,溫度越高Fe2+的氧化率越大,故B正確;
C.亞鐵離子的氧化率不僅和溫度、pH有關,還與離子的濃度等其它因素有關,故C正確;
D.根據圖象知,降低pH、升高溫度亞鐵離子的氧化率增大,故D正確;
故選A.
點評 本題考查了外界條件對Fe2+氧化率的影響,難度不大,注意比較氧化率時,必須是其它條件相同只有一個條件不同時才能比較,否則無法得出結論.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 物質 | CH3OH | CH3OCH3 | H2O |
| 濃度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯聚合為聚乙烯高分子材料符合綠色化學原子經濟性要求 | |
| B. | 銀制品久置干燥空氣中因電化學腐蝕而使表面變暗 | |
| C. | 重金屬鹽能使蛋白質變性,所以誤食重金屬鹽會中毒 | |
| D. | 在合成洗滌劑中添加酶制劑可以提高洗滌效果 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com