
【題目】白銀(Ag)是高新技術產業的基礎材料之一。在一種光盤金屬層中回收少量白銀(金屬層中其他金屬含量過低,對實驗的影響可忽略)的流程如下:
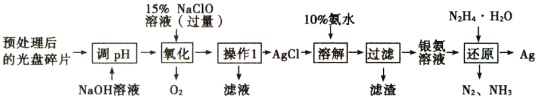
已知:NaC1O溶液在受熱或酸性條件下易分解。
下列敘述正確的是
A.“氧化”過程若在加強熱和強酸性條件下進行時可提高氧化速率
B.“操作1”所用到的玻璃儀器是玻璃棒、燒杯、分液漏斗
C.若“還原”過程通過原電池來實現,則N2為正極產物
D.“還原”過程中參加反應的n[Ag(NH3)![]() ]:n[N2H4·H2O]=4:1
]:n[N2H4·H2O]=4:1
 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案科目:高中化學 來源: 題型:
【題目】根據提供的情境書寫指定反應的方程式。
(1)工業上以碳酸錳礦(主要成分為MnCO3,另含少量FeO、Fe2O3、CaO等雜質)為主要原料生產二氧化錳的工藝流程如下:
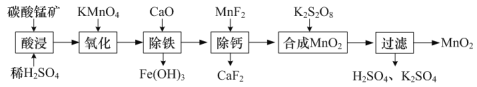
①“酸浸”時MnCO3發生反應的離子方程式為______。
②“氧化”時MnO![]() 轉化為Mn2+,該反應的離子方程式為_____。
轉化為Mn2+,該反應的離子方程式為_____。
③“合成MnO2”的化學方程式為______。
(2)氮氧化物是造成大氣污染的重要因素。
①在高壓下,NO在40 ℃下分解生成兩種化合物,體系中各組分的物質的量隨時間變化曲線如圖所示。NO分解的化學方程式為______。
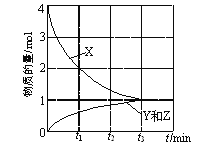
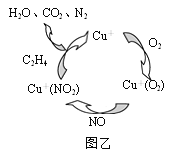
②一種以乙烯作為還原劑的脫硝(NO)機理示意圖如圖所示,該脫硝機理總反應的化學方程式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下圖所示的轉化關系,回答下列問題:

(1)寫出反應①的離子方程式:______________________________________________;寫出反應②的離子方程式:______________________。
(2)推出下列物質的化學式:E____________;I______________。
(3)在上述轉化過程中,B、C、F、H的氧化能力由弱到強的順序為______________________(寫化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設 NA 表示阿伏加德羅常數的值,下列說法中正確的是
A.標準狀況下,22.4L CCl4 含有的原子數為 5NA
B.1.8g 的 NH4+中含有的電子數為 NA
C.常溫常壓下,32 g O2 和 O3 的混合氣體中所含原子數為 1.5 NA
D.7.1g Cl2 溶于水,轉移電子數目為 0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期元素W、X、Y、Z在元素周期表中的相對位置如表所示,這四種元素的原子最外層電子數之和為21。下列說法不正確的是
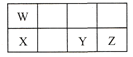
A.原子半徑大小:X > Y > Z
B.W、Y兩種元素都能與氧元素形成化合物WO2、YO2
C.氧化物對應水化物的酸性: Z > Y > W
D.Y能形成H2Y、H2YO4的化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,通過下列反應可以制備特種陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是

選項 | x | y |
A | 溫度 | 容器內混合氣體的密度 |
B | CO的物質的量 | CO2與CO的物質的量之比 |
C | SO2的濃度 | 平衡常數K |
D | MgSO4的質量(忽略體積) | CO的轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定體積的CO2通入NaOH溶液中,向所得的溶液A中逐滴加入1 mol·L-1的稀鹽酸,所加鹽酸的體積與產生CO2的體積關系如圖所示:
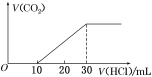
溶液A中的溶質是( )。
A.Na2CO3和NaHCO3B.NaOH和Na2CO3C.Na2CO3D.NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】反應![]() 在一個密閉容器中進行,下列措施可以使反應速率增大的是( )
在一個密閉容器中進行,下列措施可以使反應速率增大的是( )
①增加少量![]() ②升高溫度③體積不變,再通入
②升高溫度③體積不變,再通入![]() ④縮小體積增大壓強⑤體積不變,再通入He⑥壓強不變,再通入He
④縮小體積增大壓強⑤體積不變,再通入He⑥壓強不變,再通入He
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學通過以下裝置測定M樣品(只含Fe、Al、Cu)中各成分的質量分數。取兩份質量均為m g的M樣品,按實驗1(如圖1)和實驗2(如圖2)進行實驗,該同學順利完成了實驗并測得氣體體積分別為V1 mL和V2 mL(已折算到標準狀況下)。
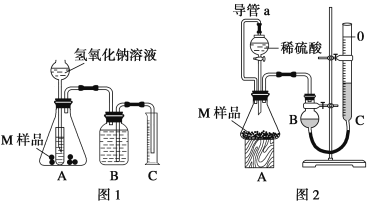
(1)寫出實驗1中可能發生反應的離子方程式:____________。
(2)該實驗需要0.50 mol·L-1的NaOH溶液480 mL,請回答下列問題:
①配制時應用托盤天平稱量______g NaOH,應選擇________ ml容量瓶。
②配制NaOH溶液時,NaOH固體中含有Na2O雜質會導致所配溶液濃度________。(填“偏大”、“偏小”或“無影響”)。
(3)該實驗中所用稀硫酸是用98%的濃硫酸(ρ=1.84g/cm3)配制的,則該濃硫酸的物質的量濃度是_______。
(4)對于實驗2,讀數時冷卻至室溫除視線平視外,還應進行的操作是: ___________。
(5)實驗2中導管a的作用_________。
(6)M樣品中銅的質量的數學表達式為(用V1和V2 表示):_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com