
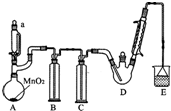
 某探究小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗.查閱資料,有關信息如下:
某探究小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗.查閱資料,有關信息如下:| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
| 熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 與水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
分析 A裝置利用二氧化錳與濃鹽酸制備氯氣,B裝置用飽和食鹽水除去HCl,C裝置盛放濃硫酸干燥氯氣,D中反應制備CCl4CHO,E裝置盛放氫氧化鈉溶液,吸收尾氣中氯氣、HCl防止污染空氣.
(1)二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣與水;
(2)用飽和食鹽水除去HCl;撤去B裝置,增大副反應C2H5OH+HCl→C2H5Cl+H2O的發生;控制反應溫度在70℃左右,應采取水浴加熱;
(3)有機物易揮發性,冷凝回流揮發的有機物;E裝置盛放氫氧化鈉溶液,吸收尾氣中氯氣、HCl,氯氣與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉與水,HCl與氫氧化鈉反應生成氯化鈉與水;
(4)CCl3COOH溶于乙醇與CCl3CHO;
(5)根據消耗的Na2S2O3計算剩余I2的物質的量,進而計算與HCOO-反應的I2的物質的量,再根據關系式:CCl3CHO~HCOO-~I2計算;
(6)a.酸性越強,電離程度越大,溶液pH越小;
b.電離程度越大,酸性越強,溶液中離子濃度越大,導電能力越強;
c.酸性越弱,其鈉鹽的水解程度越大,溶液pH越大.
解答 解:A裝置利用二氧化錳與濃鹽酸制備氯氣,B裝置用飽和食鹽水除去HCl,C裝置盛放濃硫酸干燥氯氣,D中反應制備CCl4CHO,E裝置盛放氫氧化鈉溶液,吸收尾氣中氯氣、HCl防止污染空氣.
(1)二氧化錳與濃鹽酸在加熱條件下反應生成氯化錳、氯氣與水,反應方程式為:MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案為:MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)B裝置用飽和食鹽水除去HCl,減少副反應發生,撤去B裝置,氯氣中混有HCl,增大副反應C2H5OH+HCl→C2H5Cl+H2O的發生,導致裝置D中副產物C2H5Cl增多,控制反應溫度在70℃左右,應采取水浴加熱,受熱均勻,偏于控制溫度,
故答案為:飽和食鹽水;C2H5Cl;水浴;
(3)有機物易揮發性,冷凝回流揮發的有機物;EE裝置盛放氫氧化鈉溶液,吸收尾氣中氯氣、HCl防止污染空氣,反應離子方程式為:Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O,
故答案為:冷凝回流;Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O;
(4)CCl3COOH溶于乙醇與CCl3CHO,應采取蒸餾方法進行分離,
故答案為:不可行,CCl3COOH溶于乙醇與CCl3CHO;
(5)剩余I2的物質的量0.02000mol•L-1×0.02L×$\frac{1}{2}$=2×10-4mol,與HCOO-反應的I2的物質的量為0.1000mol•L-1×0.02L-2×10-4mol=1.8×10-3mol,由CCl3CHO~HCOO-~I2可知,CCl3CHO的物質的量為1.8×10-3mol,則產品的純度為$\frac{1.8×1{0}^{-3}mol×147.5g/mol}{0.4g}$×100%=66.4%,
故答案為:66.4%;
(6)a.酸性越強,電離程度越大,溶液pH越小;
b.電離程度越大,酸性越強,溶液中離子濃度越大,導電能力越強;
c.酸性越弱,其鈉鹽的水解程度越大,溶液pH越大.
a.分別測定0.1mol•L-1兩種酸溶液的pH,三氯乙酸的pH較小,說明三氯乙酸電離程度比乙酸的大,則三氯乙酸的酸性比乙酸的強,故a正確;
b.用儀器測量濃度均為0.1mol•L-1的三氯乙酸和乙酸溶液的導電性,測得乙酸溶液的導電性弱,三氯乙酸溶液中離子濃度更大,說明三氯乙酸電離程度比乙酸的大,則三氯乙酸的酸性比乙酸的強,故b正確;
c.測定等物質的量濃度的兩種酸的鈉鹽溶液的pH,乙酸鈉溶液的pH較大,說明乙酸鈉的水解程度更大,則乙酸的酸性比三氯乙酸的弱,故c正確,
故選:abc.
點評 本題考查有機物制備、物質含量程度、實驗方案設計等,關鍵是明確反應原理與各裝置作用,掌握常用物質分離提純方法,注意對題目信息的應用,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2CH3CH2OH+2Na-→2CH3CH2ONa+H2↑ | |
| B. | CH3COOCH2CH3+H2O$?_{△}^{稀硫酸}$CH3COOH+CH3CH2OH | |
| C. | CH2═CH2+Br2-→CH2BrCH2Br | |
| D. | 2CH3CHO+O2$\stackrel{催化劑}{→}$2CH3COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
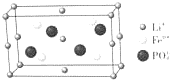 鋰的某些化合物是性能優異的材料.請回答:
鋰的某些化合物是性能優異的材料.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子式分別為C2H6和C4H10的兩種有機化合物一定互為同系物 | |
| B. | 某反應過程中的能量變化如圖所示,可見催化劑能改變該反應的焓變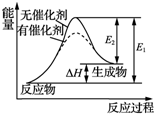 | |
| C. | 非金屬氧化物一定是酸性氧化物 | |
| D. | 1 mol N2與3 mol H2在一定條件下充分反應可得2 mol NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 某原電池裝置如圖所示,電池總反應為2Ag+Cl2═2AgCl,電解液為1mol•L-1的鹽酸.下列說法正確的是( )
某原電池裝置如圖所示,電池總反應為2Ag+Cl2═2AgCl,電解液為1mol•L-1的鹽酸.下列說法正確的是( )| A. | 正極反應為AgCl+e-═Ag+Cl- | |
| B. | 放電時交換膜右側溶液中有大量白色沉淀生成 | |
| C. | 放電后交換膜右側溶液酸性增強 | |
| D. | 當電路中轉移0.01 mol e-時交換膜左側溶液中約減少0.01 mol離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3個 | B. | 4個 | C. | 5個 | D. | 6個 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com