
| Y | Z | M | |
| W |
| A. | 原子半徑:W>Y>Z>M>X | |
| B. | 熱穩定性:XM>X2Z,沸點:X2Z>YX3 | |
| C. | X、Y、Z三種元素形成的化合物中不可能含離子鍵 | |
| D. | ZM2、YM3、WM4分子中每個原子最外層均滿足8電子結構 |
分析 X、Y、Z、M、W為5種短周期元素,X的質子總數與電子層數相同,則X為H元素;
Y、Z、M同周期且相鄰,W原子核外電子數是M原子最外層電子數的2倍,則Z為O元素,可推知Y為N元素、M為F元素、W為Si,據此判斷即可.
解答 解:X、Y、Z、M、W為5種短周期元素,X的質子總數與電子層數相同,則X為H元素;
Y、Z、M同周期且相鄰,W原子核外電子數是M原子最外層電子數的2倍,則Z為O元素,可推知Y為N元素、M為F元素、W為Si,
綜上所述:X為氫、Y為氮、Z為氧、M為氟、W為硅;
A.同周期自左而右原子半徑減小,電子層越多原子半徑越大,故原子半徑Si>N>O>F>H,故A正確;
B.XM為HF,X2Z為H2O,元素的非金屬性越強,其氣態氫化物越穩定,由于非金屬性F>O,故HF>H2O正確;水中含有氫鍵,O-H鍵長短與N-H,故沸點:H2O>NH3,故B正確;
C.H、N、O三種元素形成的化合物可以是硝酸銨,硝酸銨中既有離子鍵又有共價鍵,故C錯誤;
D.ZM2、YM3、WM4分別為OF2、NH3、SiF4,此三種物質每個原子最外層均滿足8電子結構,故D正確,
故選C.
點評 本題考查結構性質位置關系應用,難度中等,推斷元素是解題關鍵,注意氫鍵鍵能大小比較.


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源: 題型:解答題
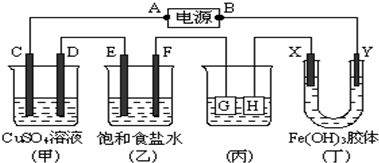
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
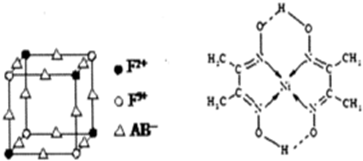
;
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 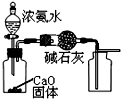 制取并收集干燥的NH3 | |
| B. | 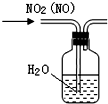 可除去NO2中的NO | |
| C. | 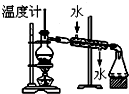 分離兩種互溶但沸點相差較大的液體混合物 | |
| D. | 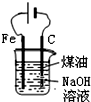 制備Fe(OH)2并能較長時間觀察其顏色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氟原子的結構示意圖: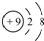 | |
| B. | 鄰硝基甲苯的結構簡式: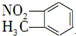 | |
| C. | 質子數為27、中子數為33的Co原子:${\;}_{27}^{60}$Co | |
| D. | H2O2的電子式: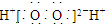 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2氣體通入NaOH溶液中,產生倒吸現象,說明SO2極易溶于水 | |
| B. | SO2氣體通入溴水中,溴水的顏色褪去,說明SO2具有漂白性 | |
| C. | SO2氣體通入酸性KMnO4溶液中,溶液的顏色變淺,說明SO2具有還原性 | |
| D. | SO2氣體通入Ba(NO3)2溶液中,溶液出現渾濁現象,說明有BaSO3沉淀生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用白醋除鐵銹:Fe2O3•xH2O+6H+═(3+x)H2O+2Fe3+ | |
| B. | 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++2OH-+N${{H}_{4}}^{+}$+H++S${{O}_{4}}^{2-}$═BaSO4↓+NH3•H2O+H2O | |
| C. | 純堿溶液和苯酚反應:C${{O}_{3}}^{2-}$+2C6H5OH→2C6H5O-+CO2↑+H2O | |
| D. | 用過氧化氫從酸化的海帶灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
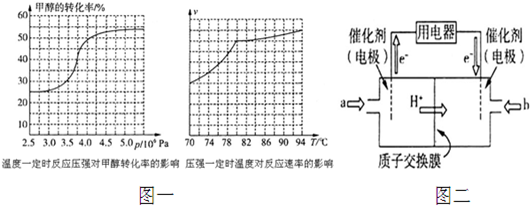
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
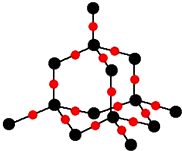 現代世界產量最高的金屬是Fe、Al、Cu.
現代世界產量最高的金屬是Fe、Al、Cu. )分子中碳原子雜化類型為SP2,分子中σ鍵比π鍵多5個.
)分子中碳原子雜化類型為SP2,分子中σ鍵比π鍵多5個.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com