
| A. | 稀醋酸中加入少量醋酸鈉能增大醋酸的電離程度 | |
| B. | 25℃時,等體積等濃度的硝酸與氨水混合后,溶液pH=7 | |
| C. | 25℃時,0.1mol•L-1的硫化氫溶液比等濃度的硫化鈉溶液的導電能力弱 | |
| D. | 0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) |
分析 A.加入醋酸鈉,溶液中醋酸根離子濃度增大,抑制醋酸的電離;
B.25℃時,等體積等濃度的硝酸與氨水混合后為NH4NO3溶液,溶液中銨根離子水解,溶液呈酸性;
C.硫化氫為弱電解質,而硫化鈉為強電解質,等濃度溶液中硫化氫溶液中離子濃度遠遠小于硫化鈉溶液中離子濃度;
D.AgCl與AgI的溶度積不同,所得溶液中c(Cl-)≠c(I-).
解答 解:A.稀醋酸溶液中存在平衡:CH3COOH?CH3COO-+H+,加入醋酸鈉,溶液中CH3COO-離子濃度增大,抑制醋酸的電離,故A錯誤;
B.25℃時,等體積等濃度的硝酸與氨水混合后為NH4NO3溶液,溶液中銨根離子水解,溶液呈酸性,故溶液pH<7,故B錯誤;
C.硫化氫為弱電解質,部分電離,而硫化鈉為強電解質,等濃度溶液中硫化氫溶液中離子濃度遠遠小于硫化鈉溶液中離子濃度,硫化氫溶液比等濃度的硫化鈉溶液的導電能力弱,故C正確;
D.均存在溶解平衡,溶液中Ag+濃度相同,AgCl與AgI的溶度積不同,所得溶液中c(Cl-)≠c(I-),故D錯誤,
故選C.
點評 本題考查弱電解質的電離平衡,題目難度中等,A為易錯點,學生容易認為醋酸根與氫離子結合,平衡右移,促進電離.


科目:高中化學 來源: 題型:選擇題
| A. | 可將地下輸油鋼管與外加直流電源的負極相連以保護鋼管不受腐蝕 | |
| B. | 常溫條件下,鋁在空氣中不易被腐蝕 | |
| C. | 鍍層破壞后,白鐵(鍍鋅的鐵)比馬口鐵(鍍錫的鐵)更耐腐蝕 | |
| D. | 用鋅與稀硫酸刮氫氣時,往稀硫酸中滴少量硫酸銅溶液能加快反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
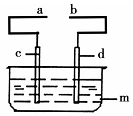 某小組為研究電化學原理,設計如圖所示裝置:
某小組為研究電化學原理,設計如圖所示裝置:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用飽和Na2CO3溶液除去乙酸乙酯中混有的少量乙醇和乙酸 | |
| B. | 用H2除去乙烷中混有的少量乙烯 | |
| C. | 用濃溴水除去苯中混有的少量苯酚 | |
| D. | 用金屬鈉除去乙醇中混有的少量水 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只用肉眼就可以把膠體和溶液、濁液區別開來 | |
| B. | 向Fe(OH)3膠體中滴加少量H2SO4溶液,會生成紅褐色沉淀 | |
| C. | 用滲析的方法凈化膠體時,使用的半透膜只能讓較小的分子、離子透過 | |
| D. | 膠粒的表面積較大,微粒具有較大的表面積,能吸附陽離子或陰離子,故在電場作用下會產生電泳現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
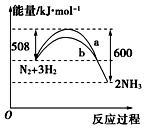 N2與H2反應生成NH3的過程中能量變化曲線如圖所示.若在一個容積固定的密閉容器中充入1mol N2和 3mol H2使反應N2+3H2?2NH3達到平衡,測得反應放出熱量為Q kJ
N2與H2反應生成NH3的過程中能量變化曲線如圖所示.若在一個容積固定的密閉容器中充入1mol N2和 3mol H2使反應N2+3H2?2NH3達到平衡,測得反應放出熱量為Q kJ查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com