
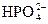 +H2O
+H2O H3O++
H3O++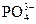 ,欲使溶液中c(
,欲使溶液中c(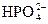 )、c(H3O+)、c(
)、c(H3O+)、c(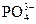 )均下降,可采用的方法是()
)均下降,可采用的方法是()| A.加少量水 | B.加熱 |
| C.加消石灰 | D.加AgNO3 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學(xué)生10分鐘應(yīng)用題系列答案
小學(xué)生10分鐘應(yīng)用題系列答案科目:高中化學(xué) 來源:不詳 題型:填空題
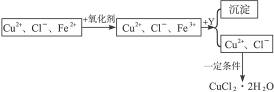
| A.K2Cr2O7 | B.NaClO | C.H2O2 | D.KMnO4 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
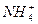 、Cl-、H+、OH-四種離子,下列說法中錯誤的是( )
、Cl-、H+、OH-四種離子,下列說法中錯誤的是( )A.溶液中四種離子之間可能滿足:c(Cl-)>c(H+)>c(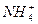 )>c(OH-) )>c(OH-) |
B.若溶液中的溶質(zhì)是NH4Cl和NH3·H2O,則粒子濃度大小:c(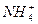 )>c(Cl-)>c(NH3·H2O)>c(H+)可能正確 )>c(Cl-)>c(NH3·H2O)>c(H+)可能正確 |
C.若溶液中四種離子滿足:c(Cl-)>c(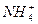 )>c(H+)>c(OH-),則溶液中的溶質(zhì)一定只有NH4Cl )>c(H+)>c(OH-),則溶液中的溶質(zhì)一定只有NH4Cl |
D.若溶液中c(Cl-)=c(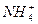 ),則該溶液呈中性 ),則該溶液呈中性 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.明礬凈水 |
| B.使用熱的純堿溶液去除油污 |
| C.實驗室配制FeCl3溶液時加入少量稀鹽酸 |
| D.實驗室制氫氣時加入CuSO4可加快反應(yīng)速率 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.加入的堿過量 |
| B.混合前,在酸與堿中溶質(zhì)的物質(zhì)的量相等 |
| C.生成的鹽不發(fā)生水解 |
| D.反應(yīng)后溶液中A-和M+的物質(zhì)的量濃度相等 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.x=104y | B.x=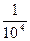 y y | C.x="y" | D.不能確定 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.1 | B.0.1 | C.10 | D.0.01 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com