
【題目】(1)請根據氧化還原反應Fe+2H+=Fe2++H2↑設計成原電池:
①負極材料為:__________發生的電極反應是: ,電流__________(填“流出”或“流入”)
②正極發生的電極反應是: ,該反應為 (填“氧化反應”或“還原反應”) 。
③若電路中轉移6.02×1022個e﹣,則產生標況下H2的體積為_____ _____。
(2)鐵處于Ⅰ、Ⅱ、Ⅲ三種不同的環境中如圖所示,則鐵被腐蝕的速率由慢到快的順序是(填序號) 。

【答案】(1)①Fe;Fe﹣2e﹣═Fe2+;流出; ②2H++2e﹣═H2↑;還原反應;③1.12L
(2)Ⅱ<Ⅲ<Ⅰ
【解析】
試題分析:(1)①根據方程式Fe+2H+=Fe2++H2↑可知鐵失去電子作還原劑,則負極材料為Fe,發生的電極反應是Fe﹣2e﹣═Fe2+;原電池中電流從正極流出;
②原電池中正極發生得到電子的還原反應,則正極是溶液中的氫離子放電,發生的電極反應是2H++2e﹣═H2↑,該反應為還原反應。
③若電路中轉移6.02×1022個e﹣,電子的物質的量是0.1mol,則產生標況下H2的體積為![]() =1.12L。
=1.12L。
(2)處于Ⅰ時鐵和碳構成原電池,鐵是負極,加快腐蝕;處于Ⅱ時鐵和鋅構成原電池,鐵是正極,被保護;處于Ⅲ時鐵發生化學腐蝕,因此三種不同的環境中則鐵被腐蝕的速率由慢到快的順序是Ⅱ<Ⅲ<Ⅰ。


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:
【題目】某課外活動小組模擬工業制備純堿,方案如下:
(一)實驗原理:向飽和食鹽水中通入足量氨氣和過量二氧化碳,析出溶解度較小的碳酸氫鈉。(1)寫出相關離子方程式 。
(二)實驗裝置:所需實驗藥品和裝置如下圖所示:

(三)實驗步驟:
(2)組裝好裝置,然后應該進行的操作是 。
(3)中間的燒瓶中加入20mL飽和食鹽水,并將其浸入冰水中;D中加入足量氫氧化鈉固體,E中加入足量濃氨水;B中加入足量碳酸鈣粉末,A中加入足量稀硫酸于(可分多次加入)。儀器A的名稱是 ,選擇用稀硫酸而不用稀鹽酸的好處是 。
(4)先打開 (填K1或K2),將裝置A或E中的試劑慢慢加入圓底燒瓶。大約20分鐘左右時,觀察到飽和食鹽水上方有 現象時,再打開 (填K1或K2),將裝置A或E中的試劑慢慢加入圓底燒瓶,大約5分鐘即有渾濁出現,約15分鐘出現大量白色固體。
(四)純堿制備:
(5)上述實驗結束后,欲得到純堿,將固體過濾、洗滌后,還需進行的操作是 (不加任何其它試劑,裝置任選),反應的化學方程式為 ;若將上述操作產生的氣體全部通過濃硫酸,再通過足量的過氧化鈉,過氧化鈉增重0.28g,則制得的純堿質量為 g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙二酸(俗名草酸)廣泛存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5。草酸的鈉鹽和鉀鹽易溶于水,但其鈣鹽難溶于水。其晶體(H2C2 O4·2H2O)無色,熔點為101℃,易溶于水,受熱脫水、升華,170℃以上分解。回答下列問題:
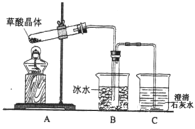
(1)某實驗小組同學想通過實驗探究草酸晶體的分解產物,設計了右圖的裝置,其中裝置B的主要作用是_____________________。通過觀察裝置C中的__________________________現象,可以確定草酸晶體分解的產物中有_________________________________。
(2)另一組同學認為草酸晶體分解的產物中不可能只有CO2,從氧化還原反應知識的原理推測可能含有 CO,為了進驗證此猜想,該組同學選用了實驗中的裝置 A、B 和下圖所示的部分裝置(可以重復選用)進行實驗。
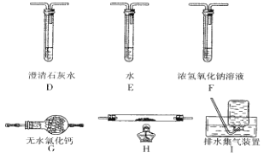
①該組同學的實驗裝置中,依次連接的合理順序為 A、B、_______________。裝置H反應管中盛有的物質是__________________。
②能證明草酸晶體分解產物中有CO的現象是____________________________________。
(3)設計實驗證明草酸的酸性比碳酸的強___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于某有機物 的性質敘述正確的是( )。
的性質敘述正確的是( )。
A.1 mol該有機物可以與3 mol Na發生反應
B.1 mol該有機物可以與3 mol NaOH發生反應
C.1 mol該有機物可以與6 mol H2發生加成反應
D.1 mol該有機物分別與足量Na或NaHCO3反應,產生的氣體在相同條件下體積相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑨ 種元素,填寫下列空白:

(1)在這些元素中,化學性質最不活潑的是: (填具體元素符號,下同)。
(2)在最高價氧化物的水化物中,酸性最強的化合物的分子式是 ,堿性最強的化合物的電子式是: 。
(3) 最高價氧化物是兩性氧化物的元素是 ;寫出它的氧化物與氫氧化鈉反應的離子方程式 。
(4)用電子式表示元素④與⑥形成的的化合物的形成過程 ,該化合物屬于 (填“共價”或“離子”)化合物。
(5)元素①的氫化物的電子式為 ,該化合物是由 (填“極性”或“非極性”)鍵形成的。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉬酸鈉晶體( Na2MoO4·2H2O)是一種無公害型冷卻水系統的金屬緩蝕劑。工業上利用鉬精礦(主要成分是不溶于水的MoS2)制備鉬酸鈉的兩種途徑如圖所示:

(1) NaClO的電子式是
(2) 寫出焙燒時生成MoO3的化學方程式為
(3)途徑I堿浸時發生反應的化學反應方程式為
(4)途徑Ⅱ氧化時發生反應的離子方程式為
(5)分析純的鉬酸鈉常用鉬酸銨[(NH4)2MoO4]和氫氧化鈉反應來制取,若將該反應產生的氣體與途徑I所產生的尾氣一起通入水中,得到正鹽的化學式是
(6)鉬酸鈉和月桂酰肌氨酸的混合液常作為碳素鋼的緩蝕劑。常溫下,碳素鋼在三種不同介質中的腐蝕速率實驗結果如下圖:

①要使碳素鋼的緩蝕效果最優,鉬酸鈉和月桂酰肌氨酸的濃度比應為 。
②當硫酸的濃度大于90%時,腐蝕速率幾乎為零,原因是 。
③試分析隨著鹽酸和硫酸濃度的增大,碳素鋼在兩者中腐蝕速率產生明顯差異的主要原因是 。
(7)鋰和二硫化鉬形成的二次電池的總反應為:xLi + nMoS2![]() Lix(MoS2)n。則電池放電時的正極反應式是: 。
Lix(MoS2)n。則電池放電時的正極反應式是: 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某優質甜櫻桃中含有一種羥基酸(用M表示),M的碳鏈結構無支鏈,分子式為C4H6O5;1.34 g M與足量的碳酸氫鈉溶液反應,生成標準狀況下的氣體0.448 L。M在一定條件下可發生如下轉化:M![]() A
A![]() B
B![]() C(M、A、B、C分子中碳原子數目相同)。下列有關說法中不正確的是( )
C(M、A、B、C分子中碳原子數目相同)。下列有關說法中不正確的是( )
A. M的結構簡式為HOOC—CHOH—CH2—COOH
B. B的分子式為C4H4O4Br2
C. 與M的官能團種類、數量完全相同的同分異構體還有1種
D. C物質不可能溶于水
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過渡元素鐵可形成多種配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
(1)Fe2+基態核外電子排布式為 。
(2)科學研究表明用TiO2作光催化劑可將廢水中CN-轉化為OCN-、并最終氧化為N2、
CO2。OCN-中三種元素的電負性由大到小的順序為 。
(3)與CN-互為等電子體的一種離子為 (填化學式);1mol [Fe(CN)6]4-中含有σ鍵的數目為 。
(4)鐵的另一種配合物Fe(CO)5熔點為﹣20.5℃,沸點為103℃,易溶于CCl4,據此可以判斷Fe(CO)5晶體屬于 (填晶體類型)。
(5)鐵鋁合金的一種晶體屬于面心立方結構,其晶胞可看成由8個小體心立方結構堆砌而成.已知小立方體如圖所示.該合金的化學式為 。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物X和Y可作為“分子傘”給藥載體的傘面和中心支撐架(未表示出原子或原子團的空間排列)。
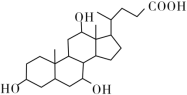
X(C24H40O5)
H2NCH2CH2CH2NHCH2CH2CH2CH2NH2 Y
下列敘述錯誤的是 ( )。
A.1 mol X在濃硫酸作用下發生消去反應,最多生成3 mol H2O
B.1 mol Y發生類似酯化的反應,最多消耗2 mol X
C.X與足量HBr反應,所得有機物的分子式為C24H37O2Br3
D.Y和癸烷的分子鏈均呈鋸齒形,但Y的極性較強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com