
分析 由(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
據(jù)蓋斯定律,(2)×2+(3)×2-(1)得:
2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=-488KJ/mol,由CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);△H1=-870.3kJ/mol,可知反應(yīng)熱為870.3kJ/mol,由反應(yīng)(3)可知消耗標況下22.4L的氫氣,放出熱量為:285.8kJ,由此分析解答.
解答 解:由(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ•mol-1
(2)C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
(3)H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ•mol-1
據(jù)蓋斯定律,(2)×2+(3)×2-(1)得:
2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=-488KJ/mol,由CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l);△H1=-870.3kJ/mol,可知反應(yīng)熱為870.3kJ/mol,由反應(yīng)(3)可知消耗標況下22.4L的氫氣,放出熱量為:285.8kJ,所以當有71.45KJ的熱量放出時需要燃燒標準狀況下的H2的體積為:$\frac{71.45KJ}{285.8kJ}×22.4L$=5.6L,故答案為:-488KJ/mol;870.3kJ/mol; 5.6.
點評 本題考查學(xué)生蓋斯定律計算反應(yīng)熱的知識,可以根據(jù)所學(xué)知識進行回答,難度不大.


科目:高中化學(xué) 來源: 題型:選擇題
| A. | 化學(xué)反應(yīng)速率:4v正(O2)=5v逆(NO) | |
| B. | NH3、O2、NO、H2O的分子個數(shù)比是4:5:4:6 | |
| C. | 單位時間內(nèi)生成4 mol NO的同時消耗6 mol H2O | |
| D. | 反應(yīng)混合物中NH3的體積分數(shù)不再改變 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
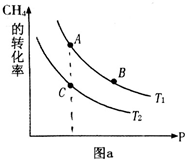 氫氣、甲醇是優(yōu)質(zhì)的清潔燃料,可制作燃料電池.
氫氣、甲醇是優(yōu)質(zhì)的清潔燃料,可制作燃料電池.查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
| 化學(xué)式 | H2(g) | CO(g) | CH3OH(l) |
| 標準燃燒熱(25℃) △H/kJ•mol-1 | -285.8 | -283.0 | -726.5 |
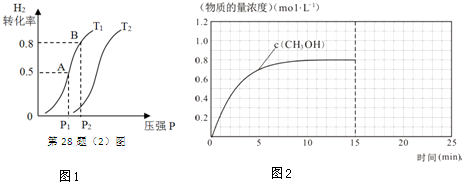
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 ,其中氮的化合價為②-2,實驗室可用次氯酸鈉溶液與氨反應(yīng)制備聯(lián)氨,反應(yīng)的化學(xué)方程式為③NaClO+2NH3=N2H4+NaCl+H2O .
,其中氮的化合價為②-2,實驗室可用次氯酸鈉溶液與氨反應(yīng)制備聯(lián)氨,反應(yīng)的化學(xué)方程式為③NaClO+2NH3=N2H4+NaCl+H2O .查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
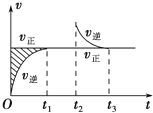 恒溫密閉容器發(fā)生可逆反應(yīng):Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應(yīng)達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態(tài)后未再改變條件.下列有關(guān)說法中正確的是( )
恒溫密閉容器發(fā)生可逆反應(yīng):Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應(yīng)達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態(tài)后未再改變條件.下列有關(guān)說法中正確的是( )| A. | Z和W在該條件下有一種是為氣態(tài) | |
| B. | t1~t2時間段與t3時刻后,兩時間段反應(yīng)體系中氣體的平均摩爾質(zhì)量不可能相等 | |
| C. | 若在該溫度下此反應(yīng)平衡常數(shù)表達式為K=c(X),則t1~t2時間段與t3時刻后的X濃度不相等 | |
| D. | 若該反應(yīng)只在某溫度T0以上自發(fā)進行,則該反應(yīng)的平衡常數(shù)K隨溫度升高而增大 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | 1 mol H2中含有6.02×1023個H | B. | 1 mol氧含有6.02×1023個O2 | ||
| C. | 1 mol CaCl2溶液里含有1 mol離子 | D. | 1 mol H+中含有H+數(shù)為NA |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | ⑧⑨⑩ | B. | ⑦⑧⑨ | C. | ③⑦⑩ | D. | ⑦⑧⑩ |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com