
【題目】常溫下,向10mL0.10 mol/L CuCl2溶液中滴加0.10mol/L Na2S溶液,滴加過程中-lgc(Cu2+)與Na2S溶液體積(V)的關系如圖所示。下列說法正確的是

A. Ksp(CuS)的數量級為10-21
B. 曲線上a點溶液中,c(S2-)c(Cu2+) > Ksp(CuS)
C. a、b、c三點溶液中,n(H+)和n(OH-)的積最小的為b點
D. c點溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
【答案】D
【解析】
向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,發生反應:Cu2++S2-CuS↓,Cu2+單獨存在或S2-單獨存在均會水解,水解促進水的電離,結合圖象分析解答。
A.該溫度下,平衡時c(Cu2+)=c(S2-)=10-17.7mol/L,則Ksp(CuS)=c(Cu2+)c(S2-) =10-17.7mol/L×10-17.7mol/L=10-35.4,則Ksp(CuS)的數量級為10-36,故A錯誤;
B.沉淀溶解平衡常數Ksp(CuS)只與溫度有關,并且Ksp(CuS)=10-35.4,很小,所以隨著Na2S溶液的滴加,溶液中c(Cu2+)減小、-lgc(Cu2+)增大,二者關系始終滿足c(S2-)c(Cu2+)=定值=Ksp(CuS),故B錯誤;
C.溫度不變,Kw=c(H+)c(OH-)不變,則n(H+) n(OH-)= KwV2,說明溶液的體積越小,n(H+) n(OH-)越小,因此n(H+)和n(OH-)的積最小的為a點,故C錯誤;
D.c點時溶質為濃度之比2∶1的NaCl和Na2S混合溶液,Na2S是弱酸強堿鹽,水解使溶液顯堿性,所以c點溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+),故D正確;
答案選D。


科目:高中化學 來源: 題型:
【題目】甲型H1N1流感病毒曾在全球廣泛傳播,給人類健康、社會經濟帶來了巨大的負面影響。我國采取積極應對措施,使病毒得到了有效的控制,從很大程度上減少了損失,在這里,消毒液功不可沒。
(1)生產消毒液是將氯氣通入NaOH溶液中,該反應的離子方程式為________。
(2)取少量消毒液滴加AgNO3溶液,現象是出現白色沉淀,說明消毒液中有____離子(寫離子符號),該反應的的離子方程式為____________。
(3)消毒液稀釋后噴灑在空氣中,可以生成具有漂白性的物質,該物質為_________;該物質有漂白性是因為它有強的氧化性,但是它也很不穩定,寫出它分解反應的化學方程式:_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用如下裝置制取氯氣,并用氯氣進行實驗。回答下列問題:

(1)A中盛有濃鹽酸,B中盛有MnO2,寫出反應的離子方程式__________________________。
(2)E中為紅色干布條,F中為紅色濕布條,可觀察到的現象是________________________,對比E和F中現象的差異可得出的結論及解釋是________________________________。
(3)試管C和D中試劑各為_____________________________。
(4)裝置G處發生反應的離子方程式為_______________________________。
(5)用離子方程式表示試劑X的作用_________________________。
(6)家庭中常用消毒液(主要成分NaClO)與潔廁靈(主要成分鹽酸)清潔衛生。某品牌消毒液包裝上說明如下圖。

①“與潔廁靈同時使用”會產生有毒的氯氣,寫出反應的離子方程式__________________。
②需“密閉保存”的原因____________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
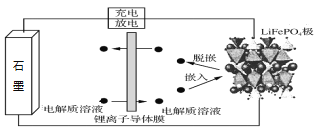
【題目】以石墨負極(C)、LiFePO4正極組成的鋰離子電池的工作原理如圖所示(實際上正負極材料是緊貼在鋰離子導體膜兩邊的)。充放電時,Li+在正極材料上脫嵌或嵌入,隨之在石墨中發生了LixC6生成與解離。下列說法正確的是
A. 鋰離子導電膜應有保護成品電池安全性的作用
B. 該電池工作過程中Fe元素化合價沒有發生變化
C. 放電時,負極材料上的反應為6C+xLi++ xe- =LixC6
D. 放電時,正極材料上的反應為LiFePO4 - xe- = Li1-xFePO4 + xLi+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,向一個容積可變的容器中,通入3 mol SO2和2 mol O2及固體催化劑,使之反應:2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-196.6 kJ·mol-1,平衡時容器內氣體壓強為起始時的90%。保持同一反應溫度,在相同容器中,將起始物質的量改為4 mol SO2、3 mol O2、2 mol SO3(g),下列說法正確的是( )
2SO3(g) ΔH=-196.6 kJ·mol-1,平衡時容器內氣體壓強為起始時的90%。保持同一反應溫度,在相同容器中,將起始物質的量改為4 mol SO2、3 mol O2、2 mol SO3(g),下列說法正確的是( )
A. 第一次平衡時反應放出的熱量為294.9 kJ
B. 兩次平衡SO2的轉化率相等
C. 第二次達平衡時SO3的體積分數大于![]()
D. 達平衡時用O2表示的反應速率為0.25 mol·(L·min)-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究和深度開發CO、CO2的應用具有重要的社會意義。回答下列問題:
Ⅰ.CO可用于高爐煉鐵,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H1=a kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H2=b kJ/mol
則反應Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)的△H3=________kJ/mol(用含a、b的代數式表示)。
Ⅱ.一定條件下,CO2和CO可以互相轉化。
(1)某溫度下,在容積為2L的密閉容器按甲、乙兩種方式投入反應物發生反應:CO2(g)+H2(g)![]() CO(g)+H2O(g)。
CO(g)+H2O(g)。
容器 | 反應物 |
甲 | 8 mol CO2(g)、16 mol H2(g) |
乙 | w mol CO2(g)、x mol H2(g)、y mol CO(g)、z mol H2O(g) |
甲容器15 min后達到平衡,此時CO2的轉化率為75%。則0~15 min內平均反應速率v(H2)=______,此條件下該反應的平衡常數K=______。
欲使平衡后乙與甲中相同組分氣體的體積分數相等,則w、x、y、z需滿足的關系是:y______z(填“>”、“<”或“=”),且y=______(用含x、w的等式表示)。
(2)研究表明,溫度、壓強對反應“C6H5CH2CH3(g)+CO2(g)![]() C6H5CH=H2(g)+CO(g) +H2O(g) △H ”中乙苯的平衡轉化率影響如圖所示:
C6H5CH=H2(g)+CO(g) +H2O(g) △H ”中乙苯的平衡轉化率影響如圖所示:

則△H_____0(填“>”、“<”或“=”),壓強p1、p2、p3從大到小的順序是________。
(3)CO可被NO2氧化:CO+NO2![]() CO2+NO。當溫度高于225℃時,反應速率v 正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分別為正、逆反應速率常數。在上述溫度范圍內,k正、k逆與該反應的平衡常數K之間的關系為________。
CO2+NO。當溫度高于225℃時,反應速率v 正=k正·c(CO)·c(NO2)、v逆=k逆·c(CO2)·c(NO),k正、k逆分別為正、逆反應速率常數。在上述溫度范圍內,k正、k逆與該反應的平衡常數K之間的關系為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ⅡBⅥA族半導體納米材料(如CdTe、CdSe、ZnSe、ZnS等)在光電子器件、太陽能電池以及生物探針等方面有廣闊的前景。回答下列問題:
(1)基態鋅(Zn)原子的電子排布式為[Ar]_____。
(2)“各能級最多容納的電子數,是該能級原子軌道數的二倍”,支撐這一結論的理論是______(填標號)
a 構造原理 b 泡利原理 c 洪特規則 d 能量最低原理
(3)在周期表中,Se與As、Br同周期相鄰,與S、Te同主族相鄰。Te、As、Se、Br的第一電離能由大到小排序為_______。
(4)H2O2和H2S的相對分子質量相等,常溫下,H2O2呈液態,而H2S呈氣態,其主要原因是______;![]() 的中心原子雜化類型為_______,其空間構型為_______。
的中心原子雜化類型為_______,其空間構型為_______。
(5)ZnO具有獨特的電學及光學特性,是一種應用廣泛的功能材料。
①已知鋅元素、氧元素的電負性分別為1.65、3.5,ZnO中化學鍵的類型為______。ZnO可以被NaOH溶液溶解生成[Zn(OH)4]2—,請從化學鍵角度解釋能夠形成該離子的原因。_______。

②一種ZnO晶體的晶胞如圖所示。晶胞邊長為a nm、阿伏加德羅常數的值為NA,其晶體密度為________g·cm3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是
A. 22.4LCl2溶于足量水,所得溶液中Cl2、Cl-、HClO和ClO-四種微粒總數為NA
B. 標準狀況下,38g3H2O2中含有3NA共價鍵
C. 常溫下,將5.6g鐵塊投入足量濃硝酸中,轉移0.3NA電子
D. 0.1molL-1MgCl2溶液中含有的Mg2+數目一定小于0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】能源是人類賴以生存和發展的重要物質基礎,常規能源的合理利用和新能源的合理開發是當今社會面臨的嚴峻課題,回答下列問題:
(1)乙醇是未來內燃機的首選環保型液體燃料。2.0g乙醇完全燃燒生成液態水放出59.43kJ的熱量,則乙醇燃燒的熱化學方程式為__________________________________________________________ 。
(2)由于C3H8(g)![]() C3H6(g)+H2(g) ΔH=+bkJ·mol-1(b>0)的反應中,反應物具有的總能量________(填“大于”“等于”或“小于”)生成物具有的總能量,那么在化學反應時,反應物就需要________(填“放出”或“吸收”)能量才能轉化為生成物。
C3H6(g)+H2(g) ΔH=+bkJ·mol-1(b>0)的反應中,反應物具有的總能量________(填“大于”“等于”或“小于”)生成物具有的總能量,那么在化學反應時,反應物就需要________(填“放出”或“吸收”)能量才能轉化為生成物。
(3)關于用水制取二次能源氫氣,以下研究方向不正確的是(________)
A.組成水的氫和氧都是可以燃燒的物質,因此可研究在水不分解的情況下,使氫成為二次能源
B.設法將太陽光聚焦,產生高溫,使水分解產生氫氣
C.尋找高效催化劑,使水分解產生氫氣,同時釋放能量
D.尋找特殊催化劑,用于開發廉價能源,以分解水制取氫氣
(4)已知下列兩個熱化學方程式:
A、2H2(g)+O2(g)![]() 2H2O(l) △H=-571.6kJ·mol-1
2H2O(l) △H=-571.6kJ·mol-1
B、C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) △H=-2220kJ·mol-1
3CO2(g)+4H2O(l) △H=-2220kJ·mol-1
其中,能表示燃燒熱的熱化學方程式為__________,其燃燒熱△H=______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com