
���}Ŀ��H2O2����Gɫ����������(y��ng)���ڏUˮ̎�����켈�ͻ��W(xu��)�ϳɵ��ИI(y��)��
��1����֪��H2(g)+![]() O2(g)=H2O(l) ��H1=��285.8kJ��mol-1
O2(g)=H2O(l) ��H1=��285.8kJ��mol-1
H2(g)+O2(g)=H2O2(l) ��H2=��135.8kJ��mol-1
��H2(g)�cO2(g)�ķ���(y��ng)�У��ڟ����W(xu��)�ϸ������Įa(ch��n)����__��ԭ����__��
�ڳ����£�H2O2�ֽ�ğữ�W(xu��)����ʽ��__��
��2���҇��ƌW(xu��)��ʹ��Ag9�F(tu��n)�����������о�H2O2�ĺϳɡ������E�Ļ�ܺͷ���(y��ng)�ᣬ�����ʾ������Ӌ��C(j��)ģ�M����(y��ng)�v����D��ʾ��TS��ʾ�^�ɑB(t��i)����ʾ��������������N����
Ag9�F(tu��n)��������H2O2�Ļ��Ea�ͷ���(y��ng)��![]()
���E | �^�ɑB(t��i) | Ea/kJ |
| |
A | Ag9 | TS1 | 74.1 | +68.7 |
B | H��Ag9 | TS2 | 108.7 | -27.2 |
C | H��Ag9��H+ O2 | TS3 | 78.4 | -75.4 |
D | HOO | TS4 | 124.7 | +31.3 |

��ͨ�^���Ͳ��E___������ĸ�����܉�����ܣ��������^�������ߺϳɷ���(y��ng)�����ʡ�
�ڷ���(y��ng)�v����2��3���ѵĻ��W(xu��)�I��___������̖����
A.O2�е������I B.H2�еĚ���I C.Ag9OOH�е������I
��3�������ꖘOͬ����늮a(ch��n)��H2O2���^�����@[(NH4)2S2O8]��ԭ����D��ʾ��ꖘO�Ϸ�늵��x����___��ꎘO��늘O����(y��ng)ʽ��___��

��4�������£�H2O2�ֽ����ʷ���v=0.0625��c(H2O2)mg��L-1��s-1��c(H2O2)�S�r�g׃�����±���
C(H2O2) (mg | 10000.0 | 8000.0 | 4000.0 | 2000.0 | 1000.0 |
�ֽ�r�g(s) | 0 | 7 | 23 | 39 | 55 |
�ٮ�(d��ng)c(H2O2)=8000.0mg��L-1�r��v=__mg��L-1��s-1��
�ڮ�(d��ng)c(H2O2)����5000.0mg��L-1�r���ֽ�r�g��___s��
���𰸡�H2O ��S���pС��������H1����H2��С���a(ch��n)��H2O�ķ���(y��ng)څ�ݸ��� 2H2O2(l)=2H2O(l)+O2(g) ��H=-300.0kJ��mol-1 D AB SO42- O2+2H++2e-=H2O2 500 16
��������
����ͨ�^![]() ���Д෴��(y��ng)��څ�ݣ����W(xu��)����(y��ng)�������ɷ���(y��ng)���������IJ��E�Q���ģ�����(j��)늽���b�ã�������x����ꖘOʧ�������S2O82-����Ԫ�ػ��σr���ͣ��^��������ꎘO���ɡ�
���Д෴��(y��ng)��څ�ݣ����W(xu��)����(y��ng)�������ɷ���(y��ng)���������IJ��E�Q���ģ�����(j��)늽���b�ã�������x����ꖘOʧ�������S2O82-����Ԫ�ػ��σr���ͣ��^��������ꎘO���ɡ�
��1���ُğ����W(xu��)څ�݁�����ͬ����(y��ng)�ﷴ��(y��ng)�r���ɷ���(y��ng)����S���pС��������H1����H2��С������(j��)![]() ���a(ch��n)��H2O�ķ���(y��ng)څ�ݸ���
���a(ch��n)��H2O�ķ���(y��ng)څ�ݸ���
�ڸ���(j��)�w˹���ɣ��ɷ���(y��ng)1-����(y��ng)2�ɵó�H2O2�ֽ�ğữ�W(xu��)����ʽ��2H2O2(l)=2H2O(l)+O2(g) ��H=-300.0kJ��mol-1��
��2������Ҫ�^�������ߺϳɷ���(y��ng)�����ʣ�ȡ�Q�ڷ���(y��ng)�ěQ������(y��ng)���ʵIJ��E���ǾͿ�ÿ������(y��ng)�Ļ�ܵĴ�С���ɱ���(sh��)��(j��)��֪���ED�Ļ��������ͨ�^���Ͳ��ED���܉�����ܣ��������^�������ߺϳɷ���(y��ng)�����ʡ�
�ڷ���(y��ng)�v����2��3����(y��ng)�ķ���ʽ��Ag9O2+H2![]() H-Ag9OOH����֪O2�������I�cH2�К���I�����ѡ�
H-Ag9OOH����֪O2�������I�cH2�К���I�����ѡ�
��3������(j��)늽���b�ÿ�֪����Ԫ�ػ��σr���ߣ���������x����ꖘOʧ�������S2O82-����ꎘO�l(f��)��߀ԭ����(y��ng)�����������c���x�������^�����䣬늘O����(y��ng)ʽ��O2+2H++2e-=H2O2��
��4���ٮ�(d��ng)c(H2O2)=8000.0mg��L-1�r���ֽ�����v=0.0625��c(H2O2)mg��L-1��s-1=��0.0625![]() 8000.0��mg��L-1��s-1=500 mg��L-1��s-1��
8000.0��mg��L-1��s-1=500 mg��L-1��s-1��
�������^�������Ȝp��һ�����͕r�g֮�g�P(gu��n)ϵ�����l(f��)�F(xi��n)�^�������Ȝp��һ�����õĕr�g�鶨ֵ������16s���ʮ�(d��ng)c(H2O2)��10000 mg��L-1����5000.0mg��L-1�r���ֽ�r�g��16s��


 99��1�I(l��ng)����ĩ��Ӗ(x��n)��ϵ�д�
99��1�I(l��ng)����ĩ��Ӗ(x��n)��ϵ�д� �ُ�(qi��ng)��У��ĩ�_��100��ϵ�д�
�ُ�(qi��ng)��У��ĩ�_��100��ϵ�д� �óɿ�1��1��ĩ�_��100��ϵ�д�
�óɿ�1��1��ĩ�_��100��ϵ�д� ���Ԫ����(y��u)�þ�ϵ�д�
���Ԫ����(y��u)�þ�ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M(f��i)�n�����]�� | ��һ | ��һ���M(f��i)�n�����]�� |
| �߶� | �߶����M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
| ���� | �������M(f��i)�n�����]�� | ���� | �������M(f��i)�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����(sh��)�(y��n)����ȡ���w�b��һ���ɰl(f��)���b�á������b�á��ռ��b���Լ�β�������b�ýM�ɡ���Cl2�Č�(sh��)�(y��n)���Ʒ�����(Ҋ�D)��
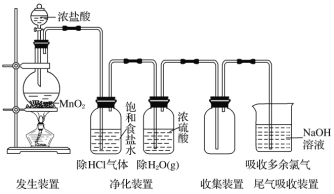
��1������(y��ng)ԭ�����Ï�(qi��ng)������(��KMnO4��K2Cr2O7��KClO3��MnO2��)�������}�ᡣMnO2��4HCl(��)![]() MnCl2��Cl2����2H2O
MnCl2��Cl2����2H2O
��2���Ƃ��b����ͣ����w��Һ�w![]() ���w
���w
��3��������������___________________��ȥHCl�����Ý������ȥˮ���⡣
��4���ռ�������________________�������ʳ�}ˮ����
��5��β�����գ��Ï�(qi��ng)�A��Һ(��NaOH��Һ)���գ�����Ca(OH)2��Һ���յ�ԭ����_________________________________________________________________________��
��6���(y��n)�M���������ĵ���-KIԇ������ʢCl2��ԇ��ƿ�ڣ��^�쵽__________________���t�C���Ѽ��M����?q��)��?/span>_________________����ʢCl2��ԇ��ƿ�ڣ��^�쵽ԇ����׃�t����ɫ���t�C���Ѽ��M��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��ij�ض��£�![]() ��
��![]() ����x����(sh��)�քe��
����x����(sh��)�քe��![]() ��
��![]() ����
����![]() ���w�e����ͬ�ăɷN����Һ�քeϡጣ���
���w�e����ͬ�ăɷN����Һ�քeϡጣ���![]() �S��ˮ�w�e��׃����D��ʾ�����Д������_���ǣ� ��
�S��ˮ�w�e��׃����D��ʾ�����Д������_���ǣ� ��

A. ����������![]() ��Һ
��Һ
B. ��Һ��ˮ����x�̶ȣ�b�c(di��n)��c�c(di��n)
C. ��c�c(di��n)��d�c(di��n)����Һ�� ���ֲ�׃������
���ֲ�׃������![]() ��
��![]() �քe��������(y��ng)���������x�ӣ�
�քe��������(y��ng)���������x�ӣ�
D. ��ͬ�w�ea�c(di��n)�ă���Һ�քe�c![]() ǡ���кͺ���Һ��
ǡ���кͺ���Һ��![]() ��ͬ
��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��ǰ20̖Ԫ��M��N��R��Q��Z��ԭ����(sh��)�����f����M�cZ��N�cQ�քeͬ���壬M��N�γɵij�Ҋ��������M2N��M2N2����ԓ5�NԪ�ؽM�ɵ�ij�Y(ji��)��������X��������ˮ�������Д����e�`���ǣ� ��
A.������X����x���I���r�I
B.�����x�Ӱ돽�ɴ�С�����?y��n)?/span>ZRQN
C.N��Q�քe�cZ�γɻ������ˮ��Һ���ʉA��
D.R��Q��Z����߃r�������ˮ�����g�������(y��ng)
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ�����ڿ��淴��(y��ng)��A(g)��3B(s)![]() 2C(g)��2D(g)���ڲ�ͬ�l���µķ���(y��ng)�������£����б�ʾ�ķ���(y��ng)���������ǣ� ��
2C(g)��2D(g)���ڲ�ͬ�l���µķ���(y��ng)�������£����б�ʾ�ķ���(y��ng)���������ǣ� ��
A.v(A)��0.5mol��L��1��min��1B.v(B)��1.2mol��L��1��s��1
C.v(D)��0.4mol��L��1��min��1D.v(C)��0.1mol��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ����܇β��������аl(f��)���ķ���(y��ng)��2NO(g)+2CO(g)![]() N2(g)+2 CO2(g)��һ���ض��£� �������w�e����1.0L�������]�����аl(f��)����������(y��ng)���y�����P(gu��n)��(sh��)�(y��n)��(sh��)��(j��)���£�
N2(g)+2 CO2(g)��һ���ض��£� �������w�e����1.0L�������]�����аl(f��)����������(y��ng)���y�����P(gu��n)��(sh��)�(y��n)��(sh��)��(j��)���£�
���� | �ض�/���棩 | ��ʼ���|(zh��)������mol) | ƽ�����|(zh��)������mol) | ||||
NO | CO | N2 | CO2 | N2 | CO2 | ||
I | 400 | 0.2 | 0.2 | 0 | 0 | 0.12 | |
II | 400 | 0.4 | 0.4 | 0 | 0 | ||
III | 300 | 0 | 0 | 0.1 | 0.2 | 0.075 | |
�����f�����_��
A. ԓ����(y��ng)�Ħ�S<0����H<0
B. ����I���_(d��)��ƽ������r�g2s���tv(N2)=0.06 molL-1��S-1
C. �_(d��)��ƽ��r���wϵ��c(CO)�P(gu��n)ϵ��c(CO,����II)>2c(CO������I)
D. ����ʼ�r��I�г���NO��CO��N2��CO2��0.1mol���_ʼ�rV��>V��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��25��r����0.1molL-1HX��Һ����u����NaOH���w���֏�(f��)��ԭ�ضȺ� �cpH���P(gu��n)ϵ��D��ʾ(������Һ�w�e׃��)���������P(gu��n)���������_����
�cpH���P(gu��n)ϵ��D��ʾ(������Һ�w�e׃��)���������P(gu��n)���������_����
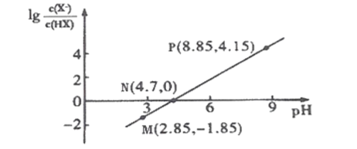
A.HX��Ka�Ĕ�(sh��)������10-5
B.P �c(di��n)����Һ�У�c(Na+)>c(X-)>c(OH-)>c(H+)
C.N �c(di��n)����Һ�У�c(Na+)+c(H+) = c(HX)+c(OH-)
D.M �c(di��n)����Һ�У�c(Na+)+c(HX) +c(H+) = 0.1 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��T��r����2L�����]�����У����wX��Y��Z�����|(zh��)�����S�r�g��׃��������D��ʾ��
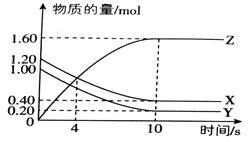
��1��ԓ����(y��ng)�Ļ��W(xu��)����ʽ��_________________________.
��2��0~10s��(n��i)��X�Ļ��W(xu��)����(y��ng)���ʞ�___________________.
��3��ԓ����(y��ng)�ڲ�ͬ�ض��µ�ƽ�ⳣ��(sh��)�����ʾ��
T/�� | 100 | 220 | 830 | 1000 | 1200 |
K | 45.00 | 32.00 | 1.00 | 0.60 | 0.38 |
�tԓ����(y��ng)�Ħ�H__________0 (�>������<����=��)
��4��830��r�����ݷe��10L�ĺ������]�����г���5molX���w��7.8molY���w��7.1mol Z���w���˕r��(��)_______��(��) (�>������<����=��)
��5���ψD��ʾ����(y��ng)�ĜضȞ�_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�
���}Ŀ��Ī���}�Ļ��W(xu��)ʽ��![]() �����������|(zh��)����392����������ˮ���������Ҵ�����һ�N��Ҫ��߀ԭ�����ڿ՚��б�һ��ā��F�}��(w��n)����������ij�W(xu��)��(x��)С�M�O(sh��)Ӌ�Ƃ�����Ī���}�Č�(sh��)�(y��n)�b�ü����E���ش����P(gu��n)���}��
�����������|(zh��)����392����������ˮ���������Ҵ�����һ�N��Ҫ��߀ԭ�����ڿ՚��б�һ��ā��F�}��(w��n)����������ij�W(xu��)��(x��)С�M�O(sh��)Ӌ�Ƃ�����Ī���}�Č�(sh��)�(y��n)�b�ü����E���ش����P(gu��n)���}��
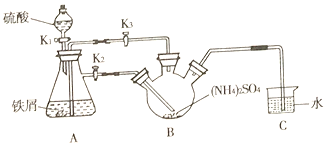
���Eһ����ȡĪ���}
��1���B���b�ã��z���b�Ú����Ժ����ˎƷ�����F��ƿ�м���![]() �Fм��������̼�ۣ������i��ƿ�м���
�Fм��������̼�ۣ������i��ƿ�м���![]() ���w����������̼�۵�������_____��
���w����������̼�۵�������_____��
��2�����Һ©����ע��![]() ϡ������P(gu��n)�]����
ϡ������P(gu��n)�]����![]() �����_
�����_![]() ��
��![]() ����ϡ����ע���F��ƿ���P(gu��n)�]
����ϡ����ע���F��ƿ���P(gu��n)�]![]() ��
��![]() �b���з���(y��ng)���x�ӷ���ʽ��______��
�b���з���(y��ng)���x�ӷ���ʽ��______��
��3�������F���ܽ���_![]() ���P(gu��n)�]
���P(gu��n)�]![]() ���˕r���Կ����ĬF(xi��n)���_____��ԭ����_____��
���˕r���Կ����ĬF(xi��n)���_____��ԭ����_____��
��4���P(gu��n)�]����![]() ��
��![]() ������100��ˮԡ���l(f��)
������100��ˮԡ���l(f��)![]() ��ˮ�֣�Һ��a(ch��n)����Ĥ�r��ֹͣ�ӟᣬ��s�Y(ji��)����____����������Q�����ßoˮ�Ҵ�ϴ�쾧�w��ԓ����(y��ng)���������^����������Һ��
��ˮ�֣�Һ��a(ch��n)����Ĥ�r��ֹͣ�ӟᣬ��s�Y(ji��)����____����������Q�����ßoˮ�Ҵ�ϴ�쾧�w��ԓ����(y��ng)���������^����������Һ��![]() ��1~2֮�g����Ŀ�Ğ�_____��
��1~2֮�g����Ŀ�Ğ�_____��
��5���b��![]() ������______��
������______��
���E�����y��Ī���}��Ʒ�ļ���
��6���Qȡ����Ī���}��Ʒ![]() ������к���s�����sˮ���
������к���s�����sˮ���![]() ��Һ��ȡ
��Һ��ȡ![]() ��Һ����ϡ���ᣬ��
��Һ����ϡ���ᣬ��![]() ��
��![]() ��Һ�ζ����_(d��)���ζ��K�c(di��n)�r����
��Һ�ζ����_(d��)���ζ��K�c(di��n)�r����![]() ��Һ���ζ�����(y��ng)���x�ӷ���ʽ��________��ԓ��Ʒ�ļ��Ȟ�________��
��Һ���ζ�����(y��ng)���x�ӷ���ʽ��________��ԓ��Ʒ�ļ��Ȟ�________��
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com