
下列各項內容中,排列順序正確的是
①固體的熱穩定性:Na2CO3>CaCO3>NaHCO3 ②物質的熔點Li>Na>K
③微粒半徑:K+>S2->F- ④單質的密度Na<K<Rb ⑤氫化物的沸點:H2Se>H2S>H2O
| A.①③ | B.②④ | C.①② | D.③⑤ |
C
解析試題分析:碳酸鈉穩定不分解,碳酸鈣高溫分解,碳酸氫鈉加熱易分解,因此固體熱穩定性:Na2CO3>CaCO3>NaHCO3,故①正確;堿金屬自上而下單質的熔點逐漸降低,所以物質的熔點Li>Na>K,②正確;電子層數越多,離子半徑越大。核外電子排布相同的微粒,其微粒半徑隨原子序數的增大而減小,所以微粒半徑:S2->K+>F-,③不正確;堿金屬自上而下單質的密度逐漸增大,但鈉的密度大于鉀的密度,即單質的密度K<Na<Rb,④不正確;氫化物的相對分子質量越大,其沸點越高,但由于水分子間存在氫鍵,因此氫化物的沸點:H2O>H2Se>H2S,⑤不正確,答案選C。
考點:考查物質穩定性、微粒半徑、熔沸點以及密度大小比較


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:單選題
依據元素周期表及元素周期律,下列推斷正確的是
| A.同一周期元素的原子,半徑越小越容易失去電子 |
| B.ⅠA族元素的金屬性比ⅡA族元素的金屬性強 |
| C.若M+和R2-的核外電子層結構相同,則原子序數R>M |
| D.主族元素的最高正化合價等于該元素原子的最外層電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列說法正確的是
| A.電子層結構相同的微粒,其化學性質一定相似 |
| B.第三周期非金屬元素含氧酸的酸性從左到右依次增強 |
| C.非金屬元素的原子兩兩結合形成的化合物不一定是共價化合物 |
| D.元素周期律是元素原子核外電子排布周期性變化的結果 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列遞變規律正確的是( )
| A.Na、Mg、Al的金屬性依次減弱 |
| B.P、S、Cl元素的最高正價依次降低 |
C.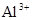 、 、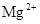 、 、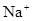 的離子半徑依次減小 的離子半徑依次減小 |
| D.HNO3、H3PO4、H2SO4酸性依次增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
X、Y、Z、W是原子序數依次遞增的4種短周期元素。其中X是周期表中原子半徑最小的元素,Y原子最外層電子數是次外層電子數的3倍,Z原子的L層電子數比K層與M層電子數之和多5個,W在同周期元素中非金屬性最強。下列說法正確的是( )
| A.X、Y、Z 3種元素組成的化合物中陰、陽離子所含電子數不等 |
| B.X與Z為同主族元素,它們的單質與W單質反應均失去電子 |
| C.Y、Z、W 3種元素組成的某種化合物可用于消毒 |
| D.Y與Z的單質在常溫下反應生成Z2Y2 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
已知X+、Y2+、Z-、W2-四種離子均具有相同的電子層結構。下列關于X、Y、Z、W四種元素的描述,正確的是 ( )
| A.原子半徑:X>Y>Z>W |
| B.原子序數:Y>X>Z>W |
| C.原子最外層電子數:Y>X>Z>W |
| D.金屬性:X<Y,還原性:W2->Z- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
短周期主族元素X、Y、Z、W、Q的原子序數依次增大,X的氣態氫化物極易溶于Y的氫化物中;常溫下,Z的單質能溶于W的最高價氧化物對應水化物的稀溶液,卻不溶于其濃溶液。下列說法正確的是
| A.通過電解熔融的Z、Q形成的化合物可制取Z單質 |
| B.原子半徑的大小順序為W>Q>Z>X>Y |
| C.元素Y的最高正化合價為+6 |
| D.XQ3分子中,中心原子是sp3雜化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com