
(8分)有下列八種晶體A.金剛石 B.蔗糖 C.氧化鎂 D.白磷 E.晶體氬
F.鋁 G.水晶 H 氫氧化鈉,用序號回答下列問題:
(1)只有離子鍵構成的化合物是 。
(2)直接由原子構成的分子晶體是 。
(3)在常溫下能導電的是 。
(4)受熱熔化時,需克服共價鍵的化合物是 。
科目:高中化學 來源: 題型:閱讀理解
(20分)
(I)多項選擇題(6分)
下列說法中正確的是 。
A.丙烯分子中有8個σ鍵,1個π鍵
B.在SiO2晶體中,1個Si原子和2個O原子形成2個共價鍵
C.NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3只有范德華力
D.NCl3和BC13分子中,中心原子都采用sp3雜化
E.在“冰→水→水蒸氣→氧氣和氫氣”的變化過程中,各階段被破壞的粒子間主要的相互作用依次是氫鍵、分子間作用力、極性鍵
(II)(14分)
人類在使用金屬的歷史進程中,經歷了銅、鐵、鋁之后,第四種將被廣泛應用的金屬被科學家預測是鈦(Ti),它被譽為“未來世紀的金屬”。試回答下列問題:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基態原子的電子排布式為________。
(2)在Ti的化合物中,可以呈現+2、+3、+4三種化合價,其中以+4價的Ti最為穩定。偏鈦酸鋇的熱穩定性好,介電常數高,在小型變壓器、話筒和擴音器中都有應用.偏鈦酸鋇晶體中晶胞的結構示意圖如圖所示,它的化學式是 ,其中Ti4+的氧配位數為 ,Ba2+的氧配位數為 ,
(3)常溫下的TiCl4是有刺激性臭味的無色透明液體,熔點-23.2℃,沸點136.2℃,所以TiCl4應是 化合物,其固體是 晶體。TiCl4在潮濕空氣中易揮發,水解而冒白煙,這是因為水解后有 生成。
(4)已知Ti3+可形成配位數為6的配合物,其空間構型為正八面體,如下圖1所示,我們通常可以用下圖2所示的方法來表示其空間構型(其中A表示配體,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空間構型也為八面體型,它有 種同分異構體,請在下圖方框中將其畫出。
查看答案和解析>>
科目:高中化學 來源:2012屆河北省衡水中學高三上學期四調考試化學試卷 題型:填空題
(I)多項選擇題
下列說法中正確的是 。
A.丙烯分子中有8個σ鍵,1個π鍵
B.在SiO2晶體中,1個Si原子和2個O原子形成2個共價鍵
C.NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3只有范德華力
D.NCl3和BC13分子中,中心原子都采用sp3雜化
E.SO3與CO32-互為等電子體,SO3是極性分子
(II)人類在使用金屬的歷史進程中,經歷了銅、鐵、鋁之后,第四種將被廣泛應用的金屬被科學家預測是鈦(Ti),它被譽為“未來世紀的金屬”。試回答下列問題:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基態原子的電子排布式為________。
(2)在Ti的化合物中,可以呈現+2、+3、+4三種化合價,其中以+4價的Ti最為穩定。偏鈦酸鋇的熱穩定性好,介電常數高,在小型變壓器、話筒和擴音器中都有應用.偏鈦酸鋇晶體中晶胞的結構示意圖如右圖所示,它的化學式是 ,其中Ti4+的氧配位數為 ,Ba2+的氧配位數為 ,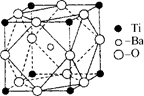
(3)常溫下的TiCl4是有刺激性臭味的無色透明液體,熔點-23.2℃,沸點136.2℃,所以TiCl4是 晶體。
4)已知Ti3+可形成配位數為6的配合物,其空間構型為正八面體,如下圖1所示,我們通常可以用下圖2所示的方法來表示其空間構型(其中A表示配體,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空間構型也為八面體型,它有 種同分異構體。
(Ⅲ)
(1)已知過氧化氫分子的空間結構如右圖所示,分子中氧原子采取 雜化。
(2)R是1~36
號元素中未成對電子數最多的原子。R3+在溶液中存在如下轉化關系: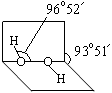
R3+ 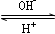 R(OH)3
R(OH)3 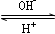 [R(OH)4]-
[R(OH)4]-
①基態R原子的價電子排布式為 ;
②[R(OH)4]-中存在的化學鍵是 。
A.離子鍵 B.極性鍵 C.非極性鍵 D.配位鍵
查看答案和解析>>
科目:高中化學 來源:2011屆海南省海口市高三下學期高考調研測試(二)化學試卷 題型:填空題
(20分)
(I)多項選擇題(6分)
下列說法中正確的是 。
| A.丙烯分子中有8個σ鍵,1個π鍵 |
| B.在SiO2晶體中,1個Si原子和2個O原子形成2個共價鍵 |
| C.NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3只有范德華力 |
| D.NCl3和BC13分子中,中心原子都采用sp3雜化 |


 色透明液體,熔點-23.2℃,沸點136.2℃,所以TiCl4應是 化合物,其固體是 晶體。TiCl4在潮濕空氣中易揮發,水解而冒白煙,這是因為水解后有 生成。
色透明液體,熔點-23.2℃,沸點136.2℃,所以TiCl4應是 化合物,其固體是 晶體。TiCl4在潮濕空氣中易揮發,水解而冒白煙,這是因為水解后有 生成。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年四川省德陽市高三第一次診斷性考試化學試卷 題型:填空題
(12分)A、B、C、D、E五種均為短周期元素,原子序數依次增大。A元素原子最外層電子數是核外電子層數的3倍,A與D同主族,A和D可形成化合物X’X可以使溴水褪色。A元素的單質和C元素的單質化合可生成Y, Y晶體中無分子,也無A、C的離子。A、B元素的單質一定條件下反應生成化合物M,D、B元素的單質反應生成化合物N,化合物M和化合物N的相對分子質量相等,且餡色反應均呈黃色。
請回答下列問題:
(1) 元素C的氣態氫化物是________分子(填寫“極性”或“非極性”)。
(2) B2D2的電子式是________________
(3) X可以使溴水褪色,該反應的離子方程式是________________________。
(4) 化合物M與化合物N的水溶液反應,若氧化劑與還原劑物質的量之比為1: 1,該反應的離子方程式是________
(5) 右圖是BE晶體的一個“晶胞結構”示意圖。下列說法正確的是________________。

A. 與B+距離相等且最近的E_共有6個
B. —個BE晶胞中含有1個B +和1個E_
C. 與B+距離相等且最近的B +有8個
D. 與B+距離相等且最近的構成的空間結構是正八面體
(6) 將原子序數介于B、C兩元素之間的單質、單質B與水反應所得的溶液構成原電池,負極的電極反應式是:O
查看答案和解析>>
科目:高中化學 來源:2010-2011學年海南省海口市高三下學期高考調研測試(二)化學試卷 題型:填空題
(20分)
(I)多項選擇題(6分)
下列說法中正確的是 。
A.丙烯分子中有8個σ鍵,1個π鍵
B.在SiO2晶體中,1個Si原子和2個O原子形成2個共價鍵
C.NF3的沸點比NH3的沸點低得多,是因為NH3分子間有氫鍵,NF3只有范德華力
D.NCl3和BC13分子中,中心原子都采用sp3雜化
E.在“冰→水→水蒸氣→氧氣和氫氣”的變化過程中,各階段被破壞的粒子間主要的相互作用依次是氫鍵、分子間作用力、極性鍵
(II)(14分)
人類在使用金屬的歷史進程中,經歷了銅、鐵、鋁之后,第四種將被廣泛應用的金屬被科學家預測是鈦(Ti),它被譽為“未來世紀的金屬”。試回答下列問題:
(1)Ti元素在元素周期表中的位置是第________周期第________族;其基態原子的電子排布式為________。
(2)在Ti的化合物中,可以呈現+2、+3、+4三種化合價,其中以+4價的Ti最為穩定。偏鈦酸鋇的熱穩定性好,介電常數高,在小型變壓器、話筒和擴音器中都有應用.偏鈦酸鋇晶體中晶胞的結構示意圖如圖所示,它的化學式是 ,其中Ti4+的氧配位數為 ,Ba2+的氧配位數為 ,

(3)常溫下的TiCl4是有刺激性臭味的無色透明液體,熔點-23.2℃,沸點136.2℃,所以TiCl4應是 化合物,其固體是 晶體。TiCl4在潮濕空氣中易揮發,水解而冒白煙,這是因為水解后有 生成。
(4)已知Ti3+可形成配位數為6的配合物,其空間構型為正八面體,如下圖1所示,我們通常可以用下圖2所示的方法來表示其空間構型(其中A表示配體,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空間構型也為八面體型,它有 種同分異構體,請在下圖方框中將其畫出。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com