
【題目】原電池是化學對人類的一項重大貢獻。某興趣小組為研究原電池原理,設計如圖裝置:

(1)a和b不連接時,燒杯中現象是 。
(2)a和b用導線連接,Cu極為原電池_________極(填“正”或“負”),
電極反應式為: ;溶液中H+移向____________
(填“Cu”或“Zn”)極。電池總反應式為: 。
若電解質溶液改為AgNO3溶液,當轉移0.2mol電子時,則理論上Cu片質量變化為___ ___g。
【答案】(1)鋅片逐漸溶解,鋅片上有氣泡冒出;
(2)正;2H++2e-=H2↑;Cu;Zn+H2SO4=ZnSO4+H2↑ ;21.6
【解析】
試題分析:(1)a和b不連接時,該裝置不構成原電池,鋅和氫離子發生置換反應,離子反應方程式為:Zn+2H+=Zn2++H2↑,因此實驗現象為鋅片逐漸溶解,鋅片上有氣泡冒出;
(2)a和b用導線連接,該裝置構成原電池,銅作正極,正極上氫離子得電子發生還原反應,電極反應式為2H++2e-=H2↑;鋅失電子發生氧化反應而作負極,放電時,電解質溶液中氫離子向正極銅電極移動,總反應式為Zn+H2SO4=ZnSO4+H2↑;鋅片減少的質量=![]() ×65g/mol=6.5g。
×65g/mol=6.5g。


科目:高中化學 來源: 題型:
【題目】(1)煤是寶貴的化石燃料,但是將煤直接作為燃料太浪費!可以通過煤的______獲得焦炭、煤焦油和出爐煤氣等產品。煤的氣化是指將煤在高溫下與水接觸轉變為可作為工業或民用燃料以及化工合成原料的煤氣,請寫出煤的氣化的化學反應方程式:_________________。
(2)把A1和Fe2O3組成的鋁熱劑充分反應后的固體分成兩等份,一份與足量的NaOH溶液反應生成標況下6.72升的氣體,另一份與足量的HCl溶液反應生成標況下17.92升的氣體。則鋁熱反應的方程式為____________________,原鋁熱劑中鋁為______克。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖中A~J分別代表相關反應的一種物質。已知A分解得到等物質的量的B、C、D,圖中有部分生成物未標出。請填寫以下空白:

(1)A中含有的化學鍵是________。
(2)寫出銅與J反應制取H的化學方程式:__________________________________________。
(3)寫出反應③的離子方程式:_________________________________________。
(4)寫出物質B的電子式:_______________;寫出物質E的電子式:_______________。
(5)在反應④中,當生成標況下22.4 L 物質G時,轉移電子數為________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學–選修2:化學與技術】工業上設計將VOSO4中的K2SO4、SiO2雜質除去并回收得到V2O5的流程如下:
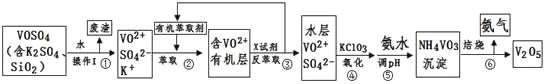
請回答下列問題:
(1)步驟①所得廢渣的成分是 (寫化學式),操作I的名稱 。
(2)步驟②、③的變化過程可簡化為(下式R表示VO2+,HA表示有機萃取劑):
R2(SO4)n(水層)+2nHA(有機層)![]() 2RAn(有機層)+nH2SO4 (水層)
2RAn(有機層)+nH2SO4 (水層)
②中萃取時必須加入適量堿,其原因是 。
③中X試劑為 。
(3)④的離子方程式為 。
(4)25℃時,取樣進行試驗分析,得到釩沉淀率和溶液pH之間關系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
釩沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
結合上表,在實際生產中,⑤中加入氨水,調節溶液的最佳pH為 。
若釩沉淀率為93.1%時不產生Fe(OH)3沉淀,則溶液中c(Fe3+)< 。
(已知:25℃時,Ksp[Fe(OH)3]=2.6×10-39)
(5)該工藝流程中,可以循環利用的物質有 和 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的氫化物NH3、N2H4等在工農業生產、航空航天等領域有廣泛應用。
(1)液氨作為一種潛在的清潔汽車燃料已越來越被研究人員重視。它在安全性、價格等方面較化石燃料和氫燃料有著較大的優勢。氨的燃燒實驗涉及下列兩個相關的反應:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H1
②4NH3(g)+6NO(g)=5N2(g)+6H2O(l) △H2
則反應 4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H= 。(請用含有△H1、△H2的式子表示)
(2)合成氨實驗中,在體積為3 L的恒容密閉容器中,投入4 mol N2和9 mol H2在一定條件下合成氨,平衡時僅改變溫度測得的數據如下表所示:
溫度(K) | 平衡時NH3的物質的量(mol) |
T1 | 2.4 |
T2 | 2.0 |
已知:破壞1 mol N2(g)和3 mol H2(g)中的化學鍵消耗的總能量小于破壞2 mol NH3(g)中的化學鍵消耗的能量。
①則T1 T2(填“>”、“<”或“=”)。
②在T2 K下,經過10min達到化學平衡狀態,則0~10min內H2的平均速率v(H2)= ,平衡時N2的轉化率α(N2)= 。
③下列圖像分別代表焓變(△H)、混合氣體平均相對分子質量(![]() )、N2體積分數φ(N2)和氣體密度(ρ)與反應時間的關系,其中正確且能表明該可逆反應達到平衡狀態的是 。
)、N2體積分數φ(N2)和氣體密度(ρ)與反應時間的關系,其中正確且能表明該可逆反應達到平衡狀態的是 。

(3)某N2H4(肼或聯氨)燃料電池(產生穩定、無污染的物質)原理如圖1所示。

①M區發生的電極反應式為 。
②用上述電池做電源,用圖2裝置電解飽和氯化鉀溶液(電極均為惰性電極),設飽和氯化鉀溶液體積為500mL,當溶液的pH值變為13時(在常溫下測定),若該燃料電池的能量利用率為80%,則需消耗N2H4的質量為 g(假設溶液電解前后體積不變)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某芳香烴A有如下轉化關系:
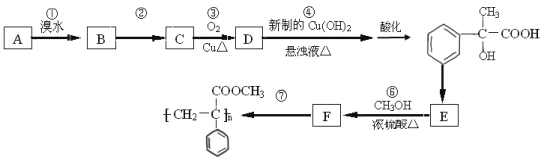
(1)寫出反應②和⑤的反應條件:② ;⑤ .
(2)寫出A的結構簡式: ;
(3)寫出反應④的化學方程式: .
(4)反應③的反應類型 .
(5)根據已學知識和獲取的信息,寫出以CH3COOH,![]() 為原料合成重要的化工產品
為原料合成重要的化工產品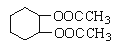 的路線流程圖(無機試劑任選)
的路線流程圖(無機試劑任選)
合成路線流程圖示例如下:
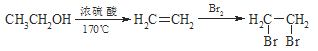
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據化學反應與能量轉化的相關知識,試回答下列問題:
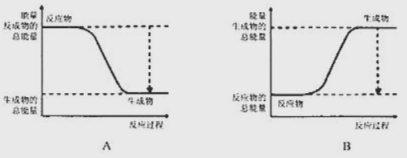
(1)已知![]() ,黑磷比白磷穩定,結構與石墨相似,下圖能正確表示該反正中能量變化的是___(填序號)。
,黑磷比白磷穩定,結構與石墨相似,下圖能正確表示該反正中能量變化的是___(填序號)。
(2)已知:氫氧燃料電池的總反應方程式為2H2O+O2=2H2O。在堿性條件下,通入氫氣一端的電極反應式為_________________。電路中每轉移0.2mol電子,標準狀況下消耗H2的體積是______L。
(3)已知斷開1mol N≡N鍵需要946kJ的能量,斷開1mol H—H鍵需要436kJ的能量,生成1moN—H鍵放出391kJ的能量,試計算生成2mol NH3時會______(填“放出”或“吸收”)______kJ能量。當在相同的條件下向容器中充入1molN2和3molH2時,它們反應對應的熱量______(填“大于”、“等于”或“小于”)你所計算出的值,原因是______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ.某實驗小組對H2O2的分解做了如下探究。下表是該實驗小組研究影響H2O2分解速率的因素時記錄的一組數據,將質量相同的粉末狀和塊狀的MnO2分別加入盛有15 ml 5%的H2O2溶液的大試管中,并用帶火星的木條測試,結果如下:
MnO2 | 觸摸試管情況 | 觀察結果 | 反應完成所需的時間 |
粉末狀 | 很燙 | 劇烈反應,帶火星的木條復燃 | 3.5min |
塊狀 | 微熱 | 反應較慢,火星紅亮但木條未復燃 | 30min |
(1)寫出上述實驗中發生反應的化學方程式: 。
(2)實驗結果表明,催化劑的催化效果與 有關。
Ⅱ.某反應在體積為5L的恒容密閉容器中進行, 在0-3分鐘內各物質的量的變化情況如右下圖所示(A,B,C均為氣體,且A氣體有顏色)。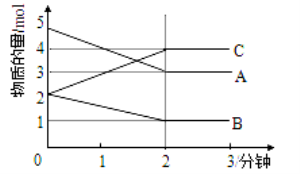
(3)該反應的的化學方程式為 。
(4)反應開始至2分鐘時,B的平均反應速率為 。
(5)能說明該反應已達到平衡狀態的是 。
a.v(A)= 2v(B) b.容器內各物質的物質的量相等
c.v逆(A)=v正(C) d.容器內氣體的顏色保持不變
(6)由圖求得平衡時A的轉化率為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.“低碳經濟”時代,科學家利用“組合轉化”等技術對CO2進行綜合利用。
(1) CO2和H2在一定條件下可以生成乙烯:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g) △H=akJ·mol-1已知:H2(g)的燃燒熱為285.8kJ·mol-1,CH2=CH2(g)的燃燒熱為1411.0kJ·mol-1,H2O(g)=H2O(l)
CH2=CH2(g)+4H2O(g) △H=akJ·mol-1已知:H2(g)的燃燒熱為285.8kJ·mol-1,CH2=CH2(g)的燃燒熱為1411.0kJ·mol-1,H2O(g)=H2O(l)
△H=-44.0kJ·mol-1,則a=______kJ·mol-1。
(2)上述生成乙烯的反應中,溫度對CO2的平衡轉化率及催化劑的催化效率影響如圖,下列有關說法不正確的是_______(填序號)

①溫度越高,催化劑的催化效率越高
②溫度低于250℃時,隨著溫度升高,乙烯的產率增大
③M點平衡常數比N點平衡常數大
④N點正反應速率一定大于M點正反應速率
⑤增大壓強可提高乙烯的體積分數
(3)2012年科學家根據光合作用原理研制出“人造樹葉”。右圖是“人造樹葉”的電化學模擬實驗裝置圖,該裝置能將H2O和CO2轉化為O2和有機物C3H8O。

陰極的電極反應式為::_________________________
II.為減輕大氣污染,可在汽車尾氣排放處加裝催化轉化裝置,反應方程式為:
2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。
2CO2(g)+N2(g)。
(4)上述反應使用等質量的某種催化劑時,溫度和催化劑的比表面積對化學反應速率的影響對比實驗如下表,c(NO)濃度隨時間(t)變化曲線如下圖:


①表中a=___________。
②實驗說明,該反應是__________反應(填“放熱”或“吸熱”)。
③若在500℃時,投料=1,NO的轉化率為80%,則此溫度時的平衡常數K=_____。
(5)使用電化學法也可處理NO的污染,裝置如右圖。已知電解池陰極室中溶液的pH在4~7之間,寫出陰極的電極反應式:__________。吸收池中除去NO的離子方程式為:__________________。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com