
如圖:燒瓶中充滿a氣體,滴管和燒杯中盛放足量b溶液,將滴管中溶液擠入燒瓶,打開止水夾f,能形成噴泉的是
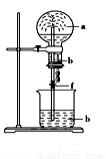
A. a是Cl2,b是飽和NaCl溶液
B. a是NO,b是H2O
C. a 是 HCl,b是AgNO3 溶液
D. a是CO2,b是飽和NaHCO3溶液
 通城學典默寫能手系列答案
通城學典默寫能手系列答案科目:高中化學 來源:2016-2017學年江西省南昌市高一上學期期末考試化學試卷(解析版) 題型:選擇題
下列溶液中通入大量的CO2氣體一定會產生渾濁現象的是( )
①氯化鈣溶液 ②澄清的石灰水 ③碳酸鈉溶液
④偏鋁酸鈉溶液 ⑤硅酸鈉溶液 ⑥次氯酸鈣溶液
A. ①②④⑤⑥ B. ②③④⑤⑥ C. ④⑤ D. ③④⑤
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省安慶市高一上學期期末考試化學試卷(解析版) 題型:填空題
有下列物質:
①氫氧化鈉固體 ②鋁絲 ③稀硫酸 ④飽和食鹽水 ⑤HCl
⑥Na2CO3.10H2O ⑦酒精 ⑧熔融的KCl ⑨明礬 ⑩石墨
(1)可導電的物質:____________________
(2)屬于電解質的:____________________
(3)屬于電解質,但不能導電的:____________________
(4)屬于非電解質的:____________________
(5)既不是電解質又不是非電解質的:____________________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年安徽省安慶市高一上學期期末考試化學試卷(解析版) 題型:選擇題
下列操作能達到實驗目的或不影響實驗的是
A. 容量瓶用水洗凈后,可不經干燥直接用于配制溶液
B. 向煮沸的1 mol/L NaOH溶液中滴加FeCl3飽和溶液制備Fe(OH)3膠體
C. 向溶液中滴加鹽酸酸化的氯化鋇,若有白色沉淀,說明溶液中含硫酸根
D. 蒸餾時應先加熱然后再通冷凝水
查看答案和解析>>
科目:高中化學 來源:湖南省長沙市2016-2017學年高一上學期期末考試化學試卷 題型:簡答題
焊接鋼鐵時常用的焊藥為氯化銨,其作用是消除焊接處的鐵銹。發生的反應體系中共有六種物質:NH4Cl、N2、Fe2O3、Fe 和 X。
(1)根據題意,可判斷出X是_____________(寫化學式)
(2)寫出并配平該反應的化學方程式,并用雙線橋標出電子轉移的方向和數目:________________。
(3)在反應 3BrF3+5H2O=HBrO3+Br2+9HF+O2 中,被氧化的元素是____________,當有5 mol水反應時,由H2O還原的BrF3為______________mol。
查看答案和解析>>
科目:高中化學 來源:湖南省長沙市2016-2017學年高一上學期期末考試化學試卷 題型:選擇題
過濾后的食鹽水仍含有可溶性的CaCl2、MgCl2、Na2SO4等雜質,通過如下幾個實驗步驟,可制得純凈的食鹽水:①加入稍過量的Na2CO3溶液;②加人稍過量的NaOH溶液:③加人稍過量的BaCl2溶液;④滴入稀鹽酸至無氣泡產生;⑤過濾。正確的操作順序是
A. ③②①⑤④ B. ①②③⑤④
C. ②③①④⑤ D. ③⑤②①④
查看答案和解析>>
科目:高中化學 來源:湖南省長沙市2016-2017學年高一上學期期末考試化學試卷 題型:選擇題
我國重點城市近年來已發布“空氣質量日報”。下列物質中不列入污染指數的是
A. 二氧化硫 B. 二氧化氮 C. 二氧化碳 D. 可吸人顆粒物
查看答案和解析>>
科目:高中化學 來源:2017屆云南省昆明市新課標高三月考卷(六)理綜化學試卷(解析版) 題型:簡答題
某學習小組利用反應:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O H2C2O4來探究“外界條件對化學反應速率的影響”。實驗時,先分別量取KMnO4酸性溶液、H2C2O4溶液,然后倒入大試管中迅速振蕩混合均勻,開始計時,通過測定褪色所需時間來判斷反應的快慢。
(1)該反應是溶液之間發生的不可逆反應,改變壓強對其反應速率的影響是______(填序號)。
A.可能明顯加快 B.可能明顯減慢 C.幾乎無影響,可以忽略
(2)甲同學設計了如下實驗
實驗編號 | H2C2O4溶液 | KMnO4溶液 | 溫度/℃ | ||
濃度(mol/L) | 體積(mL) | 濃度(mol/L) | 體積(mL) | ||
a | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
B | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
c | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
①探究溫度對化學反應速率影響的組合實驗編號是__________,可探究溫度對化學反應速率影響的實驗編號是__________。
②實驗a測得混合后溶液褪色的時間為40%,忽略混合前后 體積的微小變化,則這段時間內的平均反應速率v(KMnO4)=______。
(3)在其它條件相同的情況下,乙同學用不同濃度的KMnO4酸性溶液實驗,測得實驗數據如下表所示:
實驗編號 | 溫度℃ | H2C2O4溶液 | KMnO4酸性溶液 | 褪色的時間(min) | |||
濃度(mol/L) | 體積(mL) | 濃度(mol/L) | 體積(mL) | ||||
1 | 25 | 0.10 | 4 | 0.2 | 8 | t1 | |
2 | 25 | 0.010 | 4 | 0.2 | 8 | t2(t2<t3) | |
依據表中數據,_____(填“能”或“不能”)得出“溶液褪色所需時間越短,反應速率越快”的結論,理由是__________________。
(4)在實驗中,草酸(H2C2O4)溶液與KMnO4酸性溶液反應時,褪色總是先慢后快。
①同學們據此提出以下假設:
假設1:該反應為放熱反應
假設2:反應生成的Mn2+對該反應有催化作用
假設3:反應生成的K+或SO42-該反應有催化作用
丙同學認為假設3不合理,其理由是__________。
②丁同學用如下實驗證明假設2成立:在A和B兩支試管中分別加入4mL0.2mol·L-1草酸溶液,再在A試管中加入lmL0.1mol·L-1MnSO4溶液、B試管中加入1mL蒸餾水,然后在兩支試管中同時分別加入1mLO.1mol·L-1KMnO4酸性溶液,A試管溶液褪色的時間明顯早于B試管。在B試管中加入1mL蒸餾水的目的是:__。
③同學們認為不宜用MnCl2溶液代替MnSO4溶液對該反應進行催化探究,其原因是(用離子方程式表示)_______________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣東省揭陽市高二下學期第一次月考理科綜合化學試卷(解析版) 題型:推斷題
聚酯增塑劑廣泛應用于耐油電纜、煤氣管、防水卷材、電氣膠帶;耐油耐汽油的特殊制品等。聚酯增塑劑G及某醫藥中間體H的一種合成路線如下(部分反應條件略去):
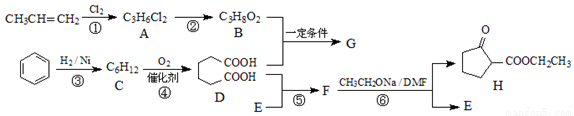
已知:
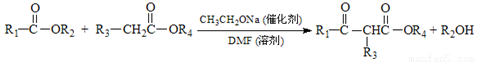
(1)B的名稱(系統命名)為___________________。
(2)若反應①的反應條件為光照,最先得到的氯代有機物結構簡式是_____________________。
(3)寫出下列反應的反應類型:反應②是________________,反應④是________________ 。
(4)寫出B與D反應生成G的反應方程式_________________________。
(5)甲苯的二氯代物產物的同分異構體有_________________種。
(6)利用以上合成路線的信息,以甲苯和乙醇為原料合成下面有機物(無機試劑任選)。
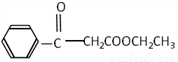
請寫出合成路線:________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com