
【題目】已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1=﹣Q1kJmol﹣1
2H2(g)+O2(g)=2H2O(g)ΔH=﹣Q2kJmol﹣1,
2H2(g)+O2(g)=2H2O(l) ΔH2=﹣Q3kJmol﹣1
常溫下,取體積比2∶3的甲烷和氫氣的混合氣體11.2 L(標準狀況下),經完全燃燒后恢復至室溫,則放出的熱量為( )
A.0.4Q1+0.15Q2B.0.2Q1+0.05Q2C.0.2Q1+0.15Q3D.0.2Q1+0.3Q2
【答案】C
【解析】
標準狀況下11.2L甲烷和氫氣混合氣體的物質的量為![]() =0.5mol,甲烷和氫氣的體積之比為2:3,所以甲烷的物質的量為:0.5mol×2/5=0.2mol,氫氣的物質的量為0.5mol-0.2mol=0.3mol,由CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-Q1 kJ/mol 可知,0.2mol甲烷燃燒放出的熱量為0.2mol×Q1 kJ/mol =0.2Q1 kJ,由2H2(g)+O2(g)=2H2O(l)△H3=-Q3 kJ/mol可知,0.3mol氫氣燃燒放出的熱量為0.3mol/2×Q3 kJ/mol =0.15Q3kJ,所以放出的熱量為0.2Q1kJ+0.15Q3kJ=(0.2Q1+0.15Q3)kJ。
=0.5mol,甲烷和氫氣的體積之比為2:3,所以甲烷的物質的量為:0.5mol×2/5=0.2mol,氫氣的物質的量為0.5mol-0.2mol=0.3mol,由CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H1=-Q1 kJ/mol 可知,0.2mol甲烷燃燒放出的熱量為0.2mol×Q1 kJ/mol =0.2Q1 kJ,由2H2(g)+O2(g)=2H2O(l)△H3=-Q3 kJ/mol可知,0.3mol氫氣燃燒放出的熱量為0.3mol/2×Q3 kJ/mol =0.15Q3kJ,所以放出的熱量為0.2Q1kJ+0.15Q3kJ=(0.2Q1+0.15Q3)kJ。
答案選C。


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源: 題型:
【題目】認真觀察下列裝置,回答下列問題:

(1)裝置B中PbO2上發生的電極反應方程式為___,鹽橋中K+移向___(填“裝置B”或“裝置C”)。
(2)裝置A中總反應的離子方程式為___。
(3)若裝置E中的目的是在Cu材料上鍍銀,則X為___,極板N的材料為___。
(4)裝置D中右側石墨電極反應式為:___;
(5)某種利用垃圾滲透液實現發電、環保二位一體結合的裝置示意圖如圖所示,當該裝置工作時,按要求填空:
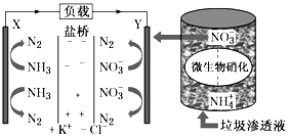
①電流由極___(填“X→Y”或“Y→X”),當電路中流過7.5mol電子時,共產生標準狀況下N2的體積為___;
②Y極發生的反應為:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是某同學探究Na2SO3溶液和鉻(VI)鹽溶液反應規律的實驗記錄,已知:Cr2O72-(橙色)+ H2O![]() 2CrO42-(黃色)+ 2H+
2CrO42-(黃色)+ 2H+
序號 | a | b | 現象 | |
| 1 | 2 mL 0.05 mol·L1 K2Cr2O7溶液(pH = 2) | 3滴飽和Na2SO3溶液(pH = 9) | 溶液變綠色(含Cr3+) |
2 | 2 mL 0.1 mol·L1 K2CrO4溶液(pH = 8) | 3滴飽和Na2SO3溶液 | 溶液沒有明顯變化 | |
3 | 2 mL飽和Na2SO3溶液 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液變黃色 | |
4 | 2 mL蒸餾水 | 3滴0.05 mol·L1 K2Cr2O7溶液 | 溶液變成淺橙色 |
下列說法不正確的是
A. 實驗1中的綠色溶液中含有SO42-
B. 實驗1、2的a溶液中所含的離子種類相同
C. 向實驗3溶液中繼續滴加過量硫酸可使溶液變為淺橙色
D. 實驗4的目的是排除稀釋對溶液顏色變化造成的影響
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據要求完成下列各小題。
(1)由銅片、鋅片和1L0.5mol/L的H2SO4(足量)組成的原電池中,若鋅片只發生電化學腐蝕,一段時間后某極產生3.36L(標準狀況)的氣體。請回答:
①負極是___(填“鋅”或“銅”),發生___反應(填“氧化”或“還原”)。

②假設反應后溶液體積不變,反應后溶液的pH為___(用對數表示)。
(2)如圖是某燃料電池的示意圖,請回答:
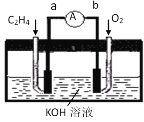
①在導線中電子流動方向為___(用a、b表示)。
②該燃料電池的負極反應式為___。
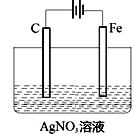
(3)如圖是電解未知濃度的硝酸銀溶液的示意圖,請根據要求答題。
①Fe電極叫做___極,C電極的反應式為___。
②當某電極的固體質量增重21.6g時,整個裝置共產生氣體(標準狀況下)體積2.24L,推斷該氣體的組成___(包括成分和體積)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在體積一定的密閉容器中給定物質A、B、C的量,在一定條件下發生反應建立的化學平衡:aA(g)+bB(g)xC(g),符合如圖所示的關系(C%表示平衡混合氣中產物C的百分含量,T表示溫度,p表示壓強)。在圖中,Y軸是指( )
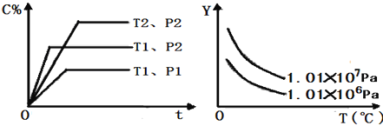
A.反應物A的百分含量B.平衡混合氣體中物質B的百分含量
C.平衡混合氣體的密度D.平衡混合氣體的平均摩爾質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,將3molA和1molB兩種氣體混合于固定容積為2L密閉容器中,發生如下反應:3A(g)+B(g)![]() xC(g)+2D(s)。2min末該反應達到平衡,生成0.6molD,并測得C的濃度為0.15mol/L。下列判斷正確的是
xC(g)+2D(s)。2min末該反應達到平衡,生成0.6molD,并測得C的濃度為0.15mol/L。下列判斷正確的是
A. 從開始到平衡A的平均反應速率為0.225mol/(Ls)
B. 從開始到平衡B的轉化率為60%
C. 此反應的化學平衡常數表達式K=c(C)c2(D)/c3(A)c(B)
D. 若混合氣體的密度不再改變時,該反應一定達到平衡狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知一定溫度下,X(g)+2Y(g) ![]() mZ(g);△H=-akJ/mol(a>0),現有甲、乙兩容積相等且固定的密閉容器,在保持該溫度下,向密閉容器甲中通入1molX和2molY,達到平衡狀態時,放出熱量bkJ;向密閉容器乙中通入2molX和4molY,達到平衡狀態時,放出熱量ckJ,且2b<c,則下列各值關系正確的是
mZ(g);△H=-akJ/mol(a>0),現有甲、乙兩容積相等且固定的密閉容器,在保持該溫度下,向密閉容器甲中通入1molX和2molY,達到平衡狀態時,放出熱量bkJ;向密閉容器乙中通入2molX和4molY,達到平衡狀態時,放出熱量ckJ,且2b<c,則下列各值關系正確的是
A. a=b B. 2a<c C. m<3 D. m>3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述中,錯誤的是( )
A.苯與濃硝酸、濃硫酸共熱并保持55-60℃反應生成硝基苯
B.乙苯能發生氧化反應,但不能發生還原反應
C.乙烯與溴的四氯化碳溶液反應生成1,2-二溴乙烷
D.苯乙烯在合適條件下催化加氫可生成乙基環己烷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列過程或現象與鹽類水解無關的是( )
A. 純堿溶液去油污 B. 加熱氯化鐵溶液顏色變深
C. 鐵在潮濕的環境中生銹 D. 濃硫化鈉溶液有臭味
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com