
| A. | 在常溫常壓下,11.2L N2含有的分子數為0.5NA | |
| B. | 在常溫常壓下,1mol 氖氣含有的原子數為2NA | |
| C. | 27g Al與足量的鹽酸反應失去的電子數為3NA | |
| D. | 在同溫同壓時,相同體積的任何氣體單質所含的原子數一定相同 |
分析 A、常溫常壓下,氣體摩爾體積大于22.4L/mol;
B、氦氣為單原子分子;
C、求出鋁的物質的量,然后根據反應后鋁元素為+3價來分析;
D、同溫同壓下,相同體積的任何氣體的物質的量相同,但單質氣體分為單原子分子,雙原子分子和多原子分子.
解答 解:A、常溫常壓下,氣體摩爾體積大于22.4L/mol,故11.2L氮氣的物質的量小于0.5mol,則分子個數小于0.5NA個,故A錯誤;
B、氦氣為單原子分子,故1mol氖氣中含1mol氖原子即NA個,故B錯誤;
C、27g鋁的物質的量為1mol,而反應后鋁元素為+3價,故1mol鋁失去3mol電子即3NA個,故C正確;
D、同溫同壓下,相同體積的任何氣體的物質的量相同,但單質氣體分為單原子分子,雙原子分子和多原子分子,故等物質的量的單質氣體中含有的原子個數不一定相同,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,掌握物質的量的計算公式和物質結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 應稱取NaOH的質量/g | 應選用容量瓶的規格/mL |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 乙苯催化脫氫制苯乙烯反應:
乙苯催化脫氫制苯乙烯反應: CH2CH3(g)$\stackrel{催化劑}{?}$
CH2CH3(g)$\stackrel{催化劑}{?}$ CH2═CH2(g)+H2(g)
CH2═CH2(g)+H2(g)| 化學鍵 | C-H | C-C | C=C | H-H |
| 鍵能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
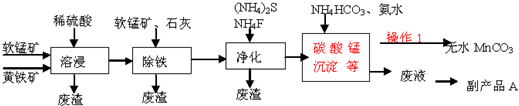
| Fe2+ | Fe3+ | Mn2+ | |
| 開始沉淀的pH | 7.5 | 3.2 | 8.8 |
| 完全沉淀的pH | 9.7 | 3.7 | 10.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 |
| 2 | C | O | F | |||||
| 3 | Na | Mg | P | S | Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室制備氫氧化鐵膠體:Fe3++3H2O $\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(膠體)+3H+ | |
| B. | 金屬銅與濃硝酸反應:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 向硫酸鋁溶液中滴加過量的氨水:Al3++4OH-═AlO22-+2H2O | |
| D. | 往KAl(SO4)2溶液中滴入Ba(OH)2溶液至沉淀的物質的量最大:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Mg2+、Fe3+、NO3-、SCN- | B. | Al3+、Fe2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HCO3- | D. | Na+、CH3COO-、NO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com