
 在密閉容器中,反應X2(g)+Y2(g)?2XY(g)△H<0達到甲平衡,僅改變某一條件后,達到乙平衡.對此過程的分析正確的是( )
在密閉容器中,反應X2(g)+Y2(g)?2XY(g)△H<0達到甲平衡,僅改變某一條件后,達到乙平衡.對此過程的分析正確的是( )| A. | 可能是減小了反應物的濃度,反應物X2轉化率一定減小 | |
| B. | 可能是加入了催化劑,反應物X2百分含量(X2%)將增大 | |
| C. | 可能是縮小了容器的體積,但該反應的平衡常數保持不變 | |
| D. | 可能是升高了溫度,該反應的平衡常數一定減小 |
分析 由反應X2(g)+Y2(g)?2XY(g),△H<0,則該反應為反應前后體積不變的反應,由圖可知改變某一條件后,達到乙平衡,達到平衡的時間短了,XY的含量降低了,說明反應速率加快,平衡向逆反應方向移動,據此分析.
解答 解:A、減小反應物濃度,化學反應速率減慢,故A錯誤;
B、加入正催化劑,正逆反應速率同等程度的增大,化學平衡不移動,故B錯誤;
C、反應X2(g)+Y2(g)?2XY(g)為反應前后體積不變的反應,若縮小了容器的體積即增大壓強,正逆反應速率同等程度的增大,但化學平衡不移動,故C錯誤;
D、由圖象可知乙的溫度大于甲的溫度,升高溫度化學平衡逆向移動,XY的含量減小,平衡常數一定減小,故D正確.
故選:D.
點評 本題考查化學反應速率、化學平衡與圖象的關系,明確影響因素及圖象中縱橫坐標的含義、點與線的含義是解答本題的關鍵.


 名題訓練系列答案
名題訓練系列答案 期末集結號系列答案
期末集結號系列答案科目:高中化學 來源: 題型:選擇題
| A. | 反應速率用于衡量化學反應進行的快慢 | |
| B. | 可逆反應達到化學平衡狀態時,正、逆反應速率都為0 | |
| C. | 決定反應速率的主要因素是反應物的性質 | |
| D. | 增大反應物濃度,提高反應溫度都能增大反應速率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 由于碘在酒精中的溶解度大,所以,可用酒精把碘水中的碘萃取出來 | |
| B. | 水的沸點是100℃,酒精的沸點是78.5℃,所以,可用加熱蒸餾方法使含水酒精變成無水酒精 | |
| C. | 氯化鈉的溶解度隨著溫度下降而減少,所以,用冷卻法從熱的含有少量硝酸鉀濃溶液中得到純凈的氯化鈉晶體 | |
| D. | 在實驗室中,通常采用加熱氯酸鉀和二氧化錳的混合物方法制取氧氣.我們可以用溶解.過濾的方法從反應產物中得到二氧化錳 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子核外電子層數越多,原子半徑越大 | |
| B. | 每一主族所含非金屬元素的種類可表示為︳族序數-2? | |
| C. | 根據泡利原理將氧元素基態原子的電子排布圖書寫為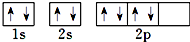 | |
| D. | C2H2分子中的碳采取sp2雜化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | x>y>z | B. | y>x>z | C. | z>x>y | D. | z>y>x |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1對 | B. | 2對 | C. | 3對 | D. | 4對 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 咖啡酸(如圖),存在于許多中藥,如野胡蘿卜、光葉水蘇、蕎麥等中.咖啡酸有止血作用.下列關于咖啡酸的說法不正確的是( )
咖啡酸(如圖),存在于許多中藥,如野胡蘿卜、光葉水蘇、蕎麥等中.咖啡酸有止血作用.下列關于咖啡酸的說法不正確的是( )| A. | 咖啡酸的分子式為C9H8O4 | |
| B. | 1mol咖啡酸可以和含4molBr2的濃溴水反應 | |
| C. | 1mol咖啡酸可以和3molNaOH反應 | |
| D. | 可以用高錳酸鉀檢驗出咖啡酸分子中含有碳碳雙鍵 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com