
【題目】
對羥基苯甲酸丁脂(俗稱尼泊金丁酯)可用作防腐劑,對酵母和霉菌有很強的抑制作用,工業上常用對羥基苯甲酸與丁醇在濃硫酸催化下進行酯化反應而制得,以下是某課題組開發的從廉價、易得的化工原料出發制備對羥基苯酸丁酯的合成路線:

已知以下信息:
通常在同一個碳原子上連有兩個羥基不穩定,易脫水形成羰基;D可與銀氨溶液反應生成銀鏡; F的核磁共振氫譜表明其有兩種不同化學環境的氫,且峰面積比為1∶1。回答下列問題:
(1)A的化學名稱為__________;
(2)由B生成C的化學反應萬程式為_____________________,該反應的類型為__________;
(3)D的結構簡式為__________;
(4)F的分子式為__________;
(5)G的結構簡式為__________;
(6)E的同分異構體中含有苯環且能發生銀鏡反應的共有__________種,其中核磁共振氫譜有三種不同化學環境的氫,且峰面積比為2∶2∶1的是_____________(寫結構簡式)。
【答案】 甲苯 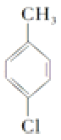 +2Cl2
+2Cl2 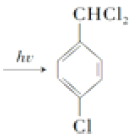 +2HCl 取代反應
+2HCl 取代反應 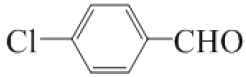 C7H4O3Na2
C7H4O3Na2 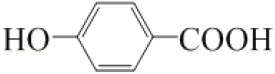 13
13 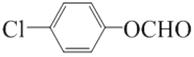
【解析】由A的分子式為C7H8,最終合成對羥基苯甲酸丁酯可知,A為甲苯![]() ,甲苯在鐵作催化劑條件下,苯環甲基對位上的H原子與氯氣發生取代反應生成B,B為
,甲苯在鐵作催化劑條件下,苯環甲基對位上的H原子與氯氣發生取代反應生成B,B為![]() ,結合已知信息可知,D中含有醛基,在光照條件下,B中甲基上的H原子與氯氣發生取代反應生成C,C為
,結合已知信息可知,D中含有醛基,在光照條件下,B中甲基上的H原子與氯氣發生取代反應生成C,C為![]() ,在氫氧化鈉水溶液中,C中甲基上的氯原子發生取代反應生成D, D為
,在氫氧化鈉水溶液中,C中甲基上的氯原子發生取代反應生成D, D為![]() ,D在催化劑條件下醛基被氧化生成E,E為
,D在催化劑條件下醛基被氧化生成E,E為![]() ,在堿性和高溫高壓的條件下,結合已知信息可知,苯環上的Cl原子被取代,同時與氫氧化鈉發生反應生成F,F為
,在堿性和高溫高壓的條件下,結合已知信息可知,苯環上的Cl原子被取代,同時與氫氧化鈉發生反應生成F,F為![]() ,F經酸化生成對羥基苯甲酸G
,F經酸化生成對羥基苯甲酸G![]() 。
。
(1). 由以上分析可知A的化學名稱為甲苯,故答案為:甲苯;
(2). B為![]() ,與氯氣在光照條件下發生取代反應生成
,與氯氣在光照條件下發生取代反應生成![]() ,方程式為
,方程式為![]() +2Cl2
+2Cl2  +2HCl,故答案為:
+2HCl,故答案為:![]() +2Cl2
+2Cl2  +2HCl;取代反應;
+2HCl;取代反應;
(3). 由以上分析可知D為![]() ,故答案為:
,故答案為:![]() ;
;
(4). F為![]() ,分子式為C7H4O3Na2,故答案為:C7H4O3Na2;
,分子式為C7H4O3Na2,故答案為:C7H4O3Na2;
(5). 由以上分析可知G為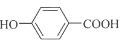 ;
;
(6). E為![]() ,同分異構體中含有苯環且能發生銀鏡反應,說明分子中含有醛基,若取代基為-OOCH、-Cl,有鄰、間、對三種結構,若取代基為-CHO、-OH、-Cl,當-CHO、-OH處于鄰位時,-Cl有4種位置,當-CHO、-OH處于間位時,-Cl有4種位置,當-CHO、-OH處于對位時,-Cl有2種位置,符合條件的同分異構體共有3+4+4+2=13種,其中核磁共振氫譜有三種不同化學環境的氫,且峰面積比為2∶2∶1的是
,同分異構體中含有苯環且能發生銀鏡反應,說明分子中含有醛基,若取代基為-OOCH、-Cl,有鄰、間、對三種結構,若取代基為-CHO、-OH、-Cl,當-CHO、-OH處于鄰位時,-Cl有4種位置,當-CHO、-OH處于間位時,-Cl有4種位置,當-CHO、-OH處于對位時,-Cl有2種位置,符合條件的同分異構體共有3+4+4+2=13種,其中核磁共振氫譜有三種不同化學環境的氫,且峰面積比為2∶2∶1的是![]() ,故答案為:13;
,故答案為:13;![]() 。
。


 三新快車金牌周周練系列答案
三新快車金牌周周練系列答案科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 將1mol Cl2 通入足量水中,溶液中HC1O、Cl-、ClO- 粒子數之和為2NA
B. 100g CaCO3晶體和100g KHCO3晶體中含有的離子數分別為2NA和3NA
C. 標準狀況下,4.48L NO 和2.24L O2 混合后,原子總數為0.6NA
D. 已知3BrF3 + 5H2O= HBrO3 + Br2 + 9HF + O2↑,若有5mol H2O 參加反應,則被水還原的BrF3分子數目為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】膠體區別于其他分散系的本質特征( )
A.膠體的分散質能通過濾紙空隙,而濁液的分散質不能
B.產生丁達爾現象
C.膠體在一定條件下能穩定存在
D.分散質粒子直徑在1~100nm之間
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高純碳酸錳在電子工業中有重要的應用,濕法浸出軟錳礦主要成分為MnO2,含少量Fe、Al、Mg等雜質元素)制備高純碳酸錳的實驗過程如下:
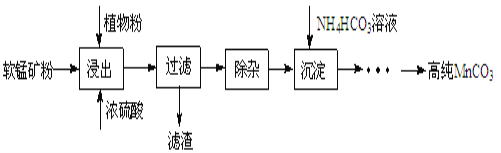
(1)浸出:浸出時溫度控制在90℃~95℃之間,并且要連續攪拌3小時,植物粉的作用是_____。
(2)除雜:①向浸出液中加入一定量的碳酸錳礦,調節浸出液的pH為3.5~5.5;
②再加入一定量的軟錳礦和雙氧水,過濾;
③…
操作①中使用碳酸錳調pH的優勢是_____;
操作②中加入雙氧水不僅能將Fe2+氧化為Fe3+,而且能提高軟錳礦的浸出率。寫出雙氧水提高軟錳礦浸出率的離子方程式_____。
(3)制備:在30℃~35℃下, 將碳酸氫銨溶液滴加到硫酸錳凈化液中,控制反應液的最終pH在6.5~7.0,得到MnCO3沉淀。溫度控制35℃以下的原因是_____;該反應的化學方程式為_____;生成的MnCO3沉淀需經充分洗滌,洗滌的操作方法是_____。
(4)計算:室溫下,Ksp(MnCO3)=1.8×10-11,Ksp(MgCO3)=2.6×10-5,已知離子濃度小于1.0×10-5mol·L-1時,表示該離子沉淀完全。若凈化液中的c(Mg2+)=10-2mol/L,試計算說明Mg2+的存在是否會影響MnCO3的純度。___________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有如下合成路線,甲經二步轉化為丙:
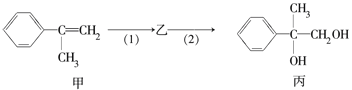
下列敘述錯誤的是
A. 甲和丙均可與酸性KMnO4溶液發生反應
B. 反應(1)的無機試劑是液溴,鐵作催化劑
C. 步驟(2)產物中可能含有未反應的甲,可用溴水檢驗是否含甲
D. 反應(2)屬于取代反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z 為原子序數 1~20 號內的元素,將 4.7g X 的最高價氧化物X2O溶于 95.3g 水中,所 得溶液濃度為 5.6% 。Y 元素原子與 X 元素原子的最外電子層電子數相同,12g Y 的氫氧化物恰好被0.75 mol/L 的鹽酸 400mL 所中和。Z、Y 的原子核外電子層數相同,16g ZO2氣體在標準狀況下的體積 為 5.6L。試求 X、Y、Z 元素名稱。X______________,Y_______________,Z____________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫恒容密閉容器中發生反應NH2COONH4(s)2NH3(g)+CO2(g),不能判斷該反應已達到化學平衡的是( )
A. v正(NH3)=2v逆(CO2) B. 密閉容器中混合氣體的平均摩爾質量不變
C. 密閉容器中混合氣體的密度不變 D. 密閉容器中總壓強不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是
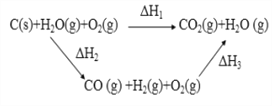
A. ΔH1=ΔH2+ΔH3
B. ΔH1<0 、 ΔH2>0 、 ΔH3<0
C. 將煤轉化為 H2(g) 和 CO(g)后燃燒比煤直接燃燒放出熱量多
D. 將煤轉化為水煤氣后再燃燒,從提高煤燃燒利用率看是得不償失
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com