
下列各反應中,生成物不隨反應條件或反應物的用量變化而變化的是( )
A.Na和O2
B.NaOH和CO2
C.AlCl3和氨水
D.NaAlO2和HCl
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2015-2016學年廣東省汕頭市高一下期末化學試卷(解析版) 題型:計算題
將9.6 g銅單質置于200 mL一定濃度的稀硝酸中,兩者恰好完全反應。假定溶液體積不變,請回答下列問題:(要求寫出計算過程)
(1)反應生成的氣體的體積(標況下);
(2)反應過程中轉移電子的物質的量;
(3)參加反應的稀硝酸的物質的量濃度。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣東省佛山市高二下期末化學試卷(解析版) 題型:選擇題
以動植物油脂為原料,在一定條件下制備生物柴油的化學原理如下:

下列敘述錯誤的是
A. 生物柴油可由再生資源制得
B.生物柴油是不同酯組成的混合物
C.該反應屬于油脂的皂化反應
D.“地溝油”可用于制備生物柴油
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高一上期末化學試卷(解析版) 題型:填空題
(14分)為確定某鋁熱劑(含氧化鐵Fe2O3和鋁)的組成,分別進行下列實驗。
(1)若取a g樣品,向其中加入足量的NaOH溶液,測得生成的氣體體積為6.72L(標準狀況)。反應的離子方程式是________ _____ ;樣品中鋁的質量是____ ___g。
(2)若另取a g樣品將其加熱引燃,恰好完全反應,該反應的化學方程式是________________,則a為________________ g。
(3)待(2)中反應產物冷卻后,加入足量鹽酸,反應的離子方程式為 和
,同時生成的氣體在標準狀況體積為 L。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高一上期末化學試卷(解析版) 題型:選擇題
下列離子能大量共存,而且加入AL后能產生氫氣的是( )
A.H+,Mg2+,Al3+,CO32-
B.Na+,Al3+,Cl-,Ba2+
C.OH-,Al3+,Cl-,NO3-
D.OH-,Ba2+,Cl-,NO3-
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高一上期末化學試卷(解析版) 題型:選擇題
下列說法中正確的是( )
A.航天飛機上的隔熱陶瓷瓦屬于優質合金材料
B.將少量CO2通入CaCl2溶液能生成白色沉淀
C.蔗糖中加入濃硫酸后出現發黑現象,說明濃硫酸具有吸水性
D.堿性氧化物一定是金屬氧化物,金屬氧化物不一定是堿性氧化物
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省五市十校教研教改共同體高二下期末化學試卷(解析版) 題型:選擇題
全釩液流電池足一種新型的綠色環保儲能電池。其電池總反應為:V3++VO2++H2O 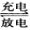 VO2++2H++V2+,下列說法正確的是
VO2++2H++V2+,下列說法正確的是
A.放電時正極反應為:VO2++2H++e-=VO2++H2O
B.充電時陰極反應為:V2+-e-=V3+
C.放電過程中電子由負極經外電路移向正極,再由正極經電解質溶液移向負極
D.充電過程中,H+由陰極區向陽極區遷移
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省、黃陂一中高二下期末化學試卷(解析版) 題型:填空題
A + B → X + Y + H2O(未配平,反應條件略去)是中學常見反應的化學方程式,請回答:
(1)若Y為黃綠色氣體:
①當 A、B的物質的量之比為1∶4且A為黑色固體時,該反應的離子方程式是
;
②當 A、B的物質的量之比為1∶6時,寫出該反應的化學方程式,并用雙線橋表示反應過程中的電子轉移:_________________________________________。
(2)若A為單質,B為無色油狀黏稠液體,當 A、B的物質的量之比為1∶2時,則A可能為______________,檢查其中刺激性氣體產物X的方法是____________________。
(3)常溫下A在B的濃溶液中會“鈍化”,且A可溶于X溶液中,若A為金屬單質,A和B以物質的量之比1∶4反應。過量的A和100mL,2mol/L的B溶液充分反應后,將溶液稀釋至500mL,溶液中陰離子的物質的量濃度為______ _______。
(4)若A、B、X、Y均為化合物,向A溶液中加入硝酸酸化的AgNO3溶液,產生白色沉淀;B的焰色為黃色,則A與B按物質的量之比1:4反應后,溶液中溶質的化學式為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高一下期末化學試卷(解析版) 題型:選擇題
在密閉容器中進行反應CH4(g)+H2O(g)  CO(g)+3H2(g);ΔH>0,測得c(CH4)隨反應時間(t)的變化如圖所示。下列判斷正確的是
CO(g)+3H2(g);ΔH>0,測得c(CH4)隨反應時間(t)的變化如圖所示。下列判斷正確的是
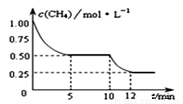
A.0到5 min內,v(H2)=0.1 mol·(L·min)-1
B.反應進行到12min時,CH4的轉化率為25%
C.恒溫下,縮小容器體積,平衡后H2濃度減小
D.10 min時,改變的外界條件可能是升高溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com