
| A. | 物質的量 | B. | 相對原子質量 | ||
| C. | 物質的摩爾質量 | D. | 12g12C中所含有的C原子數 |
分析 A、由公式n=$\frac{N}{{N}_{A}}$知,NA發生了變化,則n必發生變化;
B、相對原子質量只隨其標準的改變而改變,不隨阿伏加德羅常數的改變而改變;
C、由于n=$\frac{m}{M}$,M隨n的變化而變化;
D、只要物質的質量(或體積)一定,則構成它的粒子數一定.
解答 解:A、由公式n=$\frac{N}{{N}_{A}}$知,NA發生了變化,則n發生變化,故A錯誤;
B、相對原子質量有它自己的標準(12C原子質量的$\frac{1}{12}$),只隨其標準的改變而改變,不隨阿伏加德羅常數的改變而改變,故B正確;
C、由于n=$\frac{m}{M}$,而不論對NA如何規定,一定量的物質的質量是不變的,則M=n•m隨n的變化而變化,故C錯誤;
D、只要物質的質量(或體積)一定,則構成它的粒子數一定,不隨阿伏加德羅常數的改變而改變,故D正確.
故選BD.
點評 本題考查了阿伏伽德羅常數的計算與判斷,題目難度中等,涉及知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用基礎知識的能力,注意熟練掌握物質的量與阿伏伽德羅常數、摩爾質量等物理量之間的關系.


科目:高中化學 來源: 題型:選擇題
| A. | ②⑤ | B. | ①③⑥ | C. | ②③⑤ | D. | ①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入氫氧化鈉溶液并加熱,產生的氣體能使濕潤紅色石蕊試紙變藍,則一定有NH4+ | |
| B. | 加入氯化鋇有白色沉淀產生,再加鹽酸,沉淀不消失,該溶液一定有SO42- | |
| C. | 加入稀鹽酸,產生能使澄清石灰水變渾濁的無色氣體,則原溶液中一定有CO32- | |
| D. | 加入碳酸鈉溶液產生白色沉淀,再加鹽酸白色沉淀消失,則一定有Ca2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使酚酞變紅色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | c(AlO2-)=0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| D. | 水電離的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
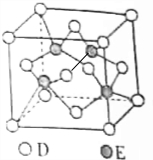 原子序數遞增的主族元素A、B、C、D、E,已知B的單質是生活中最常見的金屬之一,該元素與同主族元素A、D原子的核電荷數分別相差8和18,C元素的最高價氧化物的水化物屬于最強無機酸,E與D同周期,E的氣態基態原子第一電離能大于同周期相鄰主族元素.
原子序數遞增的主族元素A、B、C、D、E,已知B的單質是生活中最常見的金屬之一,該元素與同主族元素A、D原子的核電荷數分別相差8和18,C元素的最高價氧化物的水化物屬于最強無機酸,E與D同周期,E的氣態基態原子第一電離能大于同周期相鄰主族元素.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

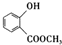 .
. +3NaOH$\stackrel{△}{→}$
+3NaOH$\stackrel{△}{→}$ +CH3COONa+CH3OH+H2O.
+CH3COONa+CH3OH+H2O. (寫出其中一種的結構簡式).
(寫出其中一種的結構簡式). )是一種重要的有機合成中間體.試寫出以苯、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用).
)是一種重要的有機合成中間體.試寫出以苯、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 犧牲陽極的陰極保護法利用的是原電池原理 | |
| B. | Fe2+能與[Fe(CN)6]3-反應生成帶有特征藍色的沉淀 | |
| C. | 電解質溶液的導電過程一定是電解質溶液的電解過程 | |
| D. | 如果在1.0L Na2CO3溶液中溶解0.010mol的BaSO4,則Na2CO3溶液的最初濃度不得低于0.24 mol/L[已知Ksp(BaSO4)=1.1×10-10; Ksp(BaCO3)=2.6×10-9] |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HI比HCl穩定 | |
| B. | HI比HCl熔、沸點高 | |
| C. | 溶于水時,HI比HCl更容易電離,所以氫碘酸是強酸 | |
| D. | 拆開等物質的量的HI和HCl,HI消耗的能量多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸鈉溶液中加入適量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等物質的量濃度的 ①NH4Cl溶液②(NH4)2SO4溶液 ③NH4HSO4溶液④(NH4)2CO3溶液中NH4+濃度的大小關系是 ②>④>①>③ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com