
Ⅰ.某化學興趣小組對下列三組物質進行研究:
A.HCl H2SO4 H2CO3 HNO3
B.溶液 水 懸濁液 膠體
C.Na2CO3 NaNO3 AgNO3 Ba(NO3)2
請你幫他們完善下列空白:
|
|
A |
B |
C |
|
分類標準 |
含氧酸 |
分散系 |
|
|
不屬于該類別的物質 |
|
|
Na2CO3 |
Ⅱ.現有下列物質:①鋁 ②氫氧化鐵膠體 ③氯化氫 ④SO2 ⑤NaHSO4 固體 ⑥Ba(OH)2固體 ⑦稀硫酸 ⑧醋酸 ⑨燒堿 ⑩熔融NaNO3
(1)按物質的分類方法填寫表格的空白處:(填編號)
|
分類標準 |
能導電的物質[ |
電解質 |
強電解質 |
|
屬于該類的物質 |
|
|
|
(2)①與⑨的溶液反應的離子方程式為
(3)用Fe(OH)3膠體進行下列實驗:
(a)將其裝入U形管內,用石墨作電極,接通直流電,通電一段時間后發現陰極附的顏色逐漸變 (填“深”或“淺”),這表明 。
(b)向其中逐滴加入過量稀硫酸溶液,現象是_______ _______;
(4)向Ba(OH)2溶液逐滴加入NaHSO4溶液至恰好不再生成沉淀為止,寫出此步的離子方程式 。
HCl(1分); 水(1分); 硝酸鹽(1分);
(1)(每題有多個并列的答案,有錯就不給分)
‚‡Š(1分); ƒ…†ˆ‰Š(1分); ƒ…†‰Š(1分);
(2)2Al+2OH¯+2H2O=2AlO2¯+3H2↑(2分);
(3)深(1分); 氫氧化鐵膠粒帶正電荷(1分);
‚先產生紅褐色沉淀(1分),后沉淀逐漸溶解,最終溶液呈黃色(1分);(本題全對得2分)
(4)Ba2++OHˉ+H++SO42ˉ=BaSO4↓+H2O(2分);
【解析】
試題分析: Ⅰ、HCl是無氧酸; 水是純凈物; 除了碳酸鈉都是硝酸鹽;
Ⅱ.(1)‚‡Š; ƒ…†ˆ‰Š; ƒ…†‰Š;
(2)2Al+2OH¯+2H2O=2AlO2¯+3H2↑;
①Fe(OH)3膠粒帶正電,通電時帶正電荷的粒子向陰極移動,陰極附的顏色逐漸變深;
②向膠體中加入少量電解質溶液時,電解質電離生成的陰離子SO42- 中和了 Fe(OH)3 膠粒所帶的正電荷,使膠粒聚集成較大的顆粒而形成紅褐色沉淀,隨著硫酸的加入,H+與Fe(OH)3發生反應Fe(OH)3+3H+=Fe3++3H2O,使沉淀溶解,故答案為:先出現紅褐色沉淀,后沉淀溶解為黃色溶液;電解質使Fe(OH)3膠體聚沉,隨著硫酸的加入,H+與Fe(OH)3發生反應Fe(OH)3+3H+=Fe3++3H2O,使沉淀溶解;
(4)Ba2++OHˉ+H++SO42ˉ=BaSO4↓+H2O。
考點:膠體的重要性質


 快樂小博士鞏固與提高系列答案
快樂小博士鞏固與提高系列答案科目:高中化學 來源: 題型:閱讀理解


查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| ||
| ||
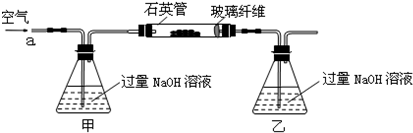
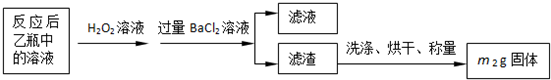
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
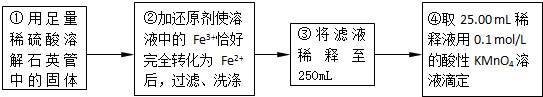
| 實驗次數 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液體積/mL | 25.00 | 25.03 | 24.97 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| ||
| ||


| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |

| 實驗次數 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液體積/mL | 26.42 | 25.05 | 24.95 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、硫酸銅溶液 | B、稀硝酸 | C、鹽酸 | D、硝酸銀溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 點燃 |
| 點燃 |
| 點燃 |
| 點燃 |
| 點燃 |
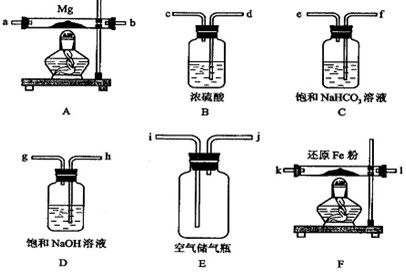
| △ |
| △ |
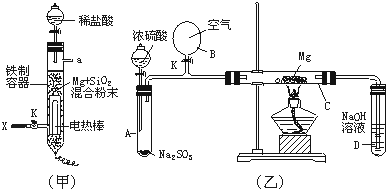
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com