
在密閉容器中進行如下反應:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始濃度分別為0.1mol/L、0.3mol/L、0.2mol/L,在一定條件下,當反應達到平衡時,各物質的濃度有可能是
2Z(g),已知X2、Y2、Z的起始濃度分別為0.1mol/L、0.3mol/L、0.2mol/L,在一定條件下,當反應達到平衡時,各物質的濃度有可能是
A.Z為0.3mol/L B.Y2為0.4mol/L
C.X2為0.2mol/L D.Z為0.4mol/L
科目:高中化學 來源:2015-2016學年河北省高二上第一次月考化學試卷(解析版) 題型:選擇題
在某溫度時,pH=3的某水溶液中c(OH-)=10-9 mol·L-1,現有該溫度下的四份溶液:①pH=2的CH3COOH;②0.01 mol·L-1的HCl;③pH=11的氨水;④pH=11的NaOH溶液。下列說法正確的是
A.①中水的電離程度最小,③中水的電離程度最大
B.若將②與④按照10∶1的體積比混合,混合溶液的pH﹤7
C.將四份溶液稀釋相同倍數后,溶液的pH:③>④>②>①
D.將四份溶液稀釋相同倍數后,溶液的pH:④>③>①>②
查看答案和解析>>
科目:高中化學 來源:2016屆江蘇省高三上學期10月月考化學試卷(解析版) 題型:實驗題
某課外活動小組設計了以下實驗驗證Ag與濃硝酸反應的過程中可能產生NO。其實驗流程圖如下:

(1)測定硝酸的物質的量反應結束后,從如圖裝置B中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示劑,滴定前后的滴定管中液面的位置如上圖所示。在B容器中生成硝酸的物質的量為______ mol,則Ag與濃硝酸反應過程中生成的NO2在標準狀況下的體積為___________mL。

(2)測定NO的體積
①從如圖所示的裝置中,你認為應選用________裝置進行Ag與濃硝酸反應實驗,選用的理由是_______。
②選用如圖所示儀器組合一套可用來測定生成NO體積的裝置,其合理的連接順序是__________(填各導管口編號)。
③在測定NO的體積時,若量筒中水的液面比集氣瓶的液面要低,此時應將量筒的位置_______(填“下降”或“升高”),以保證量筒中的液面與集氣瓶中的液面持平。
(3)氣體成分分析
若實驗測得NO的體積為112.0 mL(已折算到標準狀況),則Ag與濃硝酸反應的過程中______(填“有”或“沒有”)NO產生,作此判斷的依據是_________。
查看答案和解析>>
科目:高中化學 來源:2014-2015學年吉林省高二下期末化學試卷(解析版) 題型:填空題
(1~5小題每空2分,6小題3分,共17分)
以下是實驗室常用的部分儀器,請回答下列問題


(1)序號為⑥和⑩的儀器的名稱分別為________、________。
(2)在過濾操作中,必須用到上述儀器中的___(填序號),次外,上圖中還缺少的玻璃儀器 (填名稱)。
(3)能作反應容器且可直接加熱的儀器是上述中的________(填名稱)。
(4)儀器上標有溫度的是_______(填序號)。
(5)如圖是溫度計、量筒、滴定管的一部分,下述讀數(虛線刻度)及說法正確的是

A.①是量筒,讀數為2.5 mL
B.②是量筒,讀數為2.5 mL
C.③是滴定管,讀數為2.5 mL
D.②是溫度計,讀數是2.5 ℃
(6)丙同學想用如圖裝置以大理石和稀鹽酸反應制取CO2。教師指出,這需要太多的稀鹽酸,造成浪費。該同學選用了上述①~⑩中的一種儀器,加在裝置上,解決了這個問題。請你把該儀器畫在圖中合適的位置 。
。

查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二9月月考化學試卷(解析版) 題型:選擇題
X、Y、Z三種氣體,把a mol X與b mol Y充入一密閉容器中,發生反應X+2Y 2Z.達到平衡時,若它們的物質的量滿足:n(X)+n(Y)=n(Z),則Y的轉化率為
2Z.達到平衡時,若它們的物質的量滿足:n(X)+n(Y)=n(Z),則Y的轉化率為
A.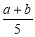 ×100% B.
×100% B.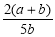 ×100%
×100%
C. ×100% D.
×100% D.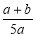 ×100%
×100%
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省富陽市高三上學期第二次質量檢測化學試卷(解析版) 題型:選擇題
化學是人類創造新物質的工具。下列各種物質的現代工業生產原理或過程的描述與事實不相符的是
A.用電解法制取Na、Mg、Al
B.電解熔融NaCl制Cl2
C.以硫或硫鐵礦為原料通過接觸法制硫酸
D.制硅:
查看答案和解析>>
科目:高中化學 來源:2016屆江西省九江市七校高三第一次聯考化學試卷(解析版) 題型:選擇題
設NA表示阿伏加德羅常數的數值,下列說法正確的是
A.1mol/L的Ca(ClO)2溶液中含ClO-數目為2NA
B.標準狀況下,22.4 L三氯甲烷的原子數約為4 NA個
C.體積分別為1.0L pH==2的鹽酸與硫酸溶液中氫離子數均為0.01NA
D.1 mol —OH與1 molOH-所含電子數均為9 NA
查看答案和解析>>
科目:高中化學 來源:2016屆福建省福州市高三上學期第二次質量檢測考試化學試卷(解析版) 題型:實驗題
(16分)輝銅礦(主要成分為Cu2S)經火法冶煉,可制得Cu和H2SO4,流程如下圖所示:
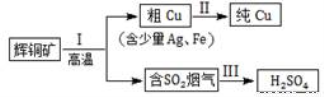
(1) Cu2S中Cu元素的化合價是 價。
(2)Ⅱ中,電解法精煉粗銅(含少量Ag、Fe),CuSO4溶液做電解質溶液:
①粗銅應與直流電源的 極(填“正”或“負”)相連。
②銅在陰極析出,而鐵以離子形式留在電解質溶液里的原因是 。
③電解一段時間后,溶液中Cu2+濃度 (填“減小”、“增大”、“不變”)。
(3)Ⅲ中,煙氣(主要含SO2、CO2)在較高溫度經下圖所示方法脫除SO2,并制得H2SO4。
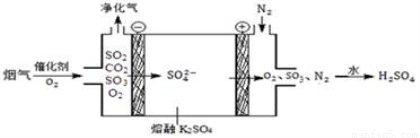
① 在陰極放電的物質是___________。
② 在陽極生成SO3的電極反應式是____________。
(4)檢測煙氣中SO2脫除率的步驟如下:
i.將一定量的凈化氣(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
ii.加入濃鹽酸,加熱溶液至無色無氣泡,再加入足量BaCl2溶液。
iii.過濾、洗滌、干燥,稱量沉淀質量。
①用離子方程式表示i中溴水的主要作用____________。
②若沉淀的質量越大,說明SO2的脫除率越____________(填“高”或“低”)。
(5)次磷酸(H3PO2)是一種精細磷化工產品,具有較強還原性。H3PO2是一元中強酸,寫出其電離方程式 ·
③NaH2PO2為_ (填“正鹽”或“酸式鹽”)其溶液顯 (填“弱酸性”、“中性”或“弱堿性”)。
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三上學期二調化學試卷(解析版) 題型:選擇題
在一定溫度下,某濃度的硝酸與金屬鋅反應生成N02和NO,兩者的物質的量之比為1:3,則要使1mol金屬鋅完全反應,反應過程中消耗此硝酸的物質的量為
A.2.4 mol B.2.6 mol C.2.8mol D.3.2 mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com