
| A. | AlCl3═Al3++Cl- | B. | Ca(OH)2═Ca2++(OH)2- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | Na2SO4═Na2++SO42- |
分析 A.電離方程式中電荷不守恒;
B.氫氧根離子符號錯誤;
C.Mg(NO3)2電離出1個鎂離子和2個硝酸根離子;
D.鈉離子符號錯誤.
解答 解:A.電離方程式中電荷不守恒,所以電離方程式為AlCl3═Al3++3Cl-,故A錯誤;
B.氫氧根離子符號錯誤,則氫氧化鈣的電離方程式為:Ca(OH)2═Ca2++2OH-,故B錯誤;
C.Mg(NO3)2電離出1個鎂離子和2個硝酸根離子,則電離方程式為:Mg(NO3)2═Mg2++2NO3-,故C正確;
D.鈉離子符號錯誤,硫酸鈉的電離方程式為Na2SO4═2Na++SO42-,故D錯誤.
故選C.
點評 本題考查電離方程式的書寫知識,注意強電解質在溶液中能完全電離,弱電解質部分電離,離子團在電離方程式中不能拆開,強酸的酸式根離子要拆開,弱酸的酸式根離子不能拆開,題目難度不大.


 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 豆腐、肉凍、果凍的生產 | B. | 工廠中設置的靜電除塵裝置 | ||
| C. | 河流入海口處三角洲的形成 | D. | 大氣污染 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
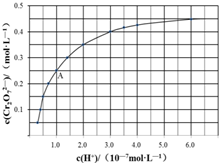 元素鉻(Cr)在溶液中主要以Cr3+(藍紫色)、Cr(OH)4-(綠色)、Cr2O72-(橙紅色)、CrO42-(黃色)等形式存在,Cr(OH)3為難溶于水的灰藍色固體,回答下列問題:
元素鉻(Cr)在溶液中主要以Cr3+(藍紫色)、Cr(OH)4-(綠色)、Cr2O72-(橙紅色)、CrO42-(黃色)等形式存在,Cr(OH)3為難溶于水的灰藍色固體,回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com