
【題目】下列關于元素周期表的敘述中不正確的是( )
A.第IIA族中無非金屬元素
B.第IA族元素單質均能與水反應生成H2
C.0族中無金屬元素
D.金屬元素的種類比非金屬元素多
科目:高中化學 來源: 題型:
【題目】CoCl2·6H2O是一種飼料營養強化劑。以含鈷廢料(含少量Fe、Al等雜質)制取CoCl2·6H2O的一種新工藝流程如圖:
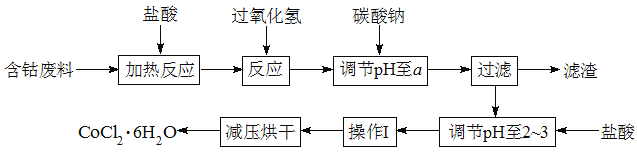
已知:
①鈷與鹽酸反應的化學方程式為:Co+2HCl=CoCl2+H2↑
②CoCl2·6H2O熔點86℃,易溶于水、乙醚等;常溫下穩定無毒,加熱至110 ~120℃時,失去結晶水變成有毒的無水氯化鈷。
③物質的熔沸點隨壓強降低而降低
④乙醚沸點為34.6℃
⑤部分陽離子以氫氧化物形式沉淀時溶液的pH見下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
開始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)在上述工藝中,用“鹽酸”代替原工藝中“鹽酸與硝酸的混酸”直接溶解含鈷廢料,從環保角度分析其主要優點為_______________________。
(2)加入碳酸鈉調節pH至a ,a的范圍是____________________________。
(3)操作Ⅰ包含3個實驗基本操作,它們依次是_____________、______________和過濾。
(4)制得的CoCl2·6H2O在烘干時需減壓烘干的原因是____________________________。
(5)在實驗室,為了從上述產品中獲得純凈的CoCl2·6H2O,通常先將產品溶解在乙醚中,通過過濾除去不溶性雜質后,再進行_________(填操作名稱)。
(6)為測定產品中CoCl2·6H2O含量,某同學將一定量的樣品溶于水,再向其中加入足量的AgNO3溶液,過濾,并將沉淀烘干后稱量其質量。通過計算發現產品中CoCl2·6H2O的質量分數大于100%,其原因可能是______________。(答出一個原因即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應:2NO2![]() 2NO+O2在恒容容器中進行,達到平衡狀態的標志是
2NO+O2在恒容容器中進行,達到平衡狀態的標志是
①單位時間內生成n molO2,的同時生成2n molNO2
②單位時間內生成n molO2的同時生成2n molNO
③用NO2、NO、O2的物質的量濃度變化表示的反應速率之比為2:2:1的狀態
④混合氣體的顏色不再改變的狀態
⑤混合氣體的密度不再改變的狀態
⑥混合氣體的平均相對分子質量不再改變的狀態
A. ①④⑥ B. ②③⑤ C. ①③④ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組對某品牌牙膏中摩擦劑的成分及其含量進行以下探究:
查得資料:該牙膏摩擦劑由碳酸鈣、氫氧化鋁組成;牙膏中其它成分遇到鹽酸時無氣體生成。利用下圖所示裝置(夾持儀器略去),對該牙膏樣品中碳酸鈣的含量進行定量測定。
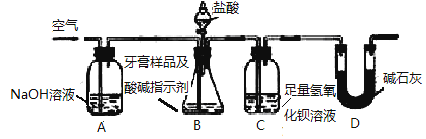
(1)C中反應生成BaCO3的化學方程式是____________________
(2)裝置D的作用是______________________
(3)實驗過程中需持續緩緩通入空氣。其作用除了可攪拌B、C中的反應物外,還有:___________________
(4)下列各項措施中,不能提高測定準確度的是______(填標號)。
a.在加入鹽酸之前,應排凈裝置內的CO2氣體
b.滴加鹽酸不宜過快
c.在A→B之間增添盛有濃硫酸的洗氣裝置
d.在B→C之間增添盛有飽和碳酸氫鈉溶液的洗氣裝置
(5)實驗中準確稱取10.00g樣品三份,進行三次測定,測得BaCO3平均質量為3.94g 。則樣品中碳酸鈣的質量分數為_________
(6)有人認為不必測定C中生成的BaCO3質量,只要測定裝置C在吸收CO2前后的質量差,一樣可以確定碳酸鈣的質量分數。實驗證明按此方法測定的結果明顯偏高,原因是_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與社會、技術、環境、生活密切相關,下列有關說法中錯誤的是
A. 石油裂解、煤的干餾和納米銀粒子的聚集都是化學變化
B. 天然氣、沼氣都是比較清潔的能源,它們的主要成分都是烴類
C. 碘酒、84消毒液、75%的酒精都可用于消毒
D. 高純硅廣泛應用于太陽能電池和計算機芯片
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫時,向一定量的硫酸銅溶液中滴加pH="11" 的氨水,當Cu2+完全沉淀時,消耗氨水的體積為V,下列說法正確的是(已知Ksp[Cu(OH)2] = 2.2×10-20)( )
A. 若將氨水加水稀釋,則稀釋過程中,c(NH4+)/c(NH3H2O)始終保持增大
B. 滴加過程中,當溶液中c(Cu2+) = 2.2×10-2 mol/L 時,溶液的pH = 9
C. 滴加過程中,當溶液的pH =" 7" 時,溶液中2c(NH4+)= c(SO42-)
D. 若滴加pH =" 11" 的NaOH 溶液,Cu2+完全沉淀時消耗溶液的體積小于V
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z都是氣體,反應前X、Y的物質的量之比是1:2,在一定條件下可逆反應X+2Y2Z達到平衡時,測得反應物總的物質的量等于生成物總的物質的量,則平衡時X的轉化率是( )
A. 80% B. 20% C. 40% D. 60%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com