
【題目】下列物質中,能導電的電解質是( )
A. 鋁絲 B. 熔融的MgCl2 C. NaCl溶液 D. 酒精
科目:高中化學 來源: 題型:
【題目】通過圖像分析影響化學平衡移動的因素,某溫度下,在密閉容器中SO2、O2、SO3三種氣態物質建立化學平衡后,改變條件對反應2SO2(g)+O2(g) 2SO3(g) ΔH<0的正、逆反應速率的影響如圖所示:

①加催化劑對反應速率影響的圖像是___(填字母,下同),平衡____移動。
②升高溫度對反應速率影響的圖像是___,平衡向____方向(填“正反應”或“逆反應”,下同)移動。
③增大反應容器體積對反應速率影響的圖像是___,平衡向____方向移動。
④增大O2的濃度對反應速率影響的圖像是___,平衡向____方向移動。
⑤上述①到④中的外界條件,使得單位體積內活化分子百分數增大的是___(填序號)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在2L容器中3種物質間進行反應,X、Y、Z的物質的量隨時間的變化曲線如圖。其中X、Y、Z都為氣體,反應在t1min時到達平衡,如圖所示,下列說法正確的是( )

A. 該反應的化學方程式是2X=3Y+Z
B. 已知1molX完全反應要吸收46kJ的熱量,則至t1min時,該反應吸收的熱量為36.8kJ·mol-1
C. 在此t1min時間內,用Y表示反應的平均速率v(Y)為0.6mol/(L·min)
D. 在相同狀態下,反應前的壓強是反應后的0.75倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(12分)現有一定量含有Na2O雜質的Na2O2試樣,用下圖的實驗裝置測定Na2O2試樣的純度。(可供選用的反應物只有CaCO3固體、6 mol/L鹽酸、6 mol/L硫酸和蒸餾水)
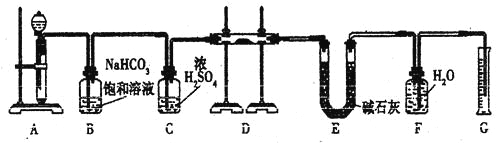
回答下列問題:
(1)裝置A中液體試劑選用 ,理由是 。
(2)裝置B的作用是 。
裝置C的作用是 。
裝置E中堿石灰的作用是 。
(3)裝置D中發生反應的化學方程式是 。
(4)若開始時測得樣品的質量為2.0 g,反應結束后測得氣體體積為224 mL(標準狀況),則Na2O2試樣的純度為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了確定某鋁熱劑(含氧化鐵和鋁)的組成,分別進行下列實驗。
(1)若取a g樣品,向其中加入足量的氫氧化鈉溶液,測得生成的氣體為b L(標況)。反應的離子方程式為_______________,樣品中鋁的物質的量為_____________(用含b的代數式表示)。
(2)若取a g樣品,在高溫下能恰好完全反應,該反應的化學方程式為________________,樣品中氧化鐵與鋁的質量比為_________________(用含a 、b的代數式表示)。
(3)待(2)中反應產物冷卻后,往其中加入足量的鹽酸,測得生成的氣體體積為c L(標況),則該氣體與(1)中所得的氣體的體積比c∶b=______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時在10 mL 0.1mol·L—1Na2CO3溶液中逐滴加入0.1 mol·L—1HCl溶液20 mL,溶液中部分含碳微粒的物質的量隨溶液pH的變化如圖所示。下列說法正確的是( )

A. 0.1 mol·L—1Na2CO3溶液中c(Na+)+c(H+)=c(OH—)+c(CO32—)+c(HCO3—)
B. 當加入10mL鹽酸時,所得混合溶液pH>7
C. 當pH=8時,c(Na+)=c(CO32—)+c(HCO3—)+c(H2CO3)
D. 在M點:c(CO32—)=c(HCO3—)>c(Na+)>c(OH—)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,在體積為3 L的密閉容器中反應CO(g)+ 2H2(g)![]() CH3OH(g)達到化學平衡狀態。
CH3OH(g)達到化學平衡狀態。
(1)反應的平衡常數表達式K=_____________;根據下圖,升高溫度,K值將__________(填“增大”、“減小”或“不變”)。

(2)500℃時,從反應開始到達到化學平衡,以H2的濃度變化表示的化學反應速率是______(用nB、tB表示)。
(3)判斷該可逆反應達到化學平衡狀態的標志是______ (填字母)。
a.v生成(CH3OH)= v消耗(CO) b.混合氣體的密度不再改變
c.混合氣體的平均相對分子質量不再改變 d.CO、H2、CH3OH的濃度均不再變化
(4)300℃時,將容器的容積壓縮到原來的1/2,在其他條件不變的情況下,對平衡體系產生的影響是(填字母)______________。
a.c(H2)減少 b.正反應速率加快,逆反應速率減慢
c.CH3OH 的物質的量增加 d.重新平衡時c(H2)/ c(CH3OH)減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水合肼是無色、有強還原性的液體,實驗室制備水合肼的原理為:CO(NH2)2+2NaOH+NaClO==Na2CO3+N2H4·H2O+NaCl 據此,某學生設計了下列實驗。
(制備NaClO溶液)

實驗裝置如圖甲所示(部分夾持裝置已省略)已知:3NaClO![]() 2NaCl+NaClO3
2NaCl+NaClO3
(1)請寫出肼的電子式_________________。
(2)配制30%NaOH溶液時,所需玻璃儀器除量筒外還有________________。
(3)裝置I中發生的化學反應方程式是 ____________________________;Ⅱ中用冰水浴控制溫度在30℃以下,其主要目的是______________________________。
(制取水合肼)
實驗裝置如圖乙所示。
(4)儀器B的名稱為_________;反應過程中,如果分液漏斗中溶液的滴速過快,部分N2H4·H2O參與A中反應并產生大量氮氣,請寫出該反應的化學反應方程式__________。
(5)充分反應后,加熱蒸餾A內的溶液即可得到水合肼的粗產品。若在蒸餾剛剛開始的時候忘記添加沸石,應該采取的操作是_____________________。
(測定肼的含量)
稱取餾分0.2500g,加水配成20.00mL溶液,在一定條件下,以淀粉溶液做指示劑,用0.1500 mol·L-1的I2溶液滴定。
已知:N2H4·H2O+2I2==N2↑+4HI+H2O
①滴定終點時的現象為______________________________。
②實驗測得消耗I2溶液的平均值為20.00 mL,餾分中N2H4.H2O的質量分數為______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com