
| 實驗序號 | 體積V/mL | ||||
| K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
| ② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
| ③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
分析 (1)慢反應中有I2生成,使溶液變藍色,而快反應中消耗I2,慢反應決定反應速率;
(2)實驗目的是探究反應物濃度對化學反應速率的影響,由表中數據可知,KI溶液、Na2S2O3溶液用量相等,應是探究K2S2O8濃度對反應速率的影響,保持溶液總體積相等.
解答 解:(1)慢反應中有I2生成,使溶液變藍色,而快反應中消耗I2,慢反應決定反應速率,當溶液中的 Na2S2O3耗盡后,碘才能與淀粉作用顯示藍色;
故答案為:Na2S2O3;
(2)實驗目的是探究反應物濃度對化學反應速率的影響,由表中數據可知,KI溶液、Na2S2O3溶液用量相等,應是探究K2S2O8濃度對反應速率的影響,保持溶液總體積相等,即其他條件不變,只改變反應物K2S2O8濃度,從而才達到對照實驗目的,故Vx=10.0mL-8.0mL=2.0mL,
故答案為:2.0;保證溶液總體積不變,即其他條件不變,只改變反應物K2S2O8濃度,從而才達到對照實驗目的.
點評 本題考查了影響反應速率的因素、反應機理的探究,題目難道不大,側重于考查學生的分析能力和應用能力,解答時須注意實驗的原理以及數據的對比.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | Cu+2H2SO4(濃) $\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+2SO2↑+2H2O | |
| B. | Cu+4NHO3(濃)=Cu(NO3)2+2NO2↑+2H2O | |
| C. | CH2=CH2+Br2→CH2Br-CH2Br | |
| D. | 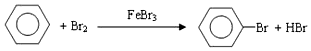 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等于0.6mol | B. | 等于1mol | ||
| C. | 大于0.6mol小于1mol | D. | 小于0.6mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,22.4 L CCl4、CO2含有的分子數為NA | |
| B. | 通常狀況下,NA個CO2分子占有的體積約為22.4 L | |
| C. | 常溫常壓下,1.06 g Na2CO3含有的Na+離子數為0.02NA | |
| D. | 物質的量濃度為0.5 mol/L的MgCl2溶液中,含有Cl-個數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一個化學反應是否能在常溫下發生與該反應的△H值的大小沒有必然聯系 | |
| B. | 中和熱△H=-57.3 kJ•mol-1,所以1.00 L 1.00 mol•L-1 H2SO4與稀的NaOH溶液恰好完全反應放出57.3 kJ的熱量 | |
| C. | 用等體積的0.50 mol•L-1鹽酸、0.55 mol•L-1 NaOH溶液進行中和熱測定的實驗,會使測得的值偏大 | |
| D. | 在101 kPa時,1 mol CH4完全燃燒生成CO2和水蒸氣放出的熱量就是CH4的燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 膠體與溶液本質區別是有無丁達爾效應 | |
| B. | 均一穩定的分散系只有溶液 | |
| C. | 只有膠狀物質如膠水、果凍才能稱為膠體 | |
| D. | 一束平行光線照射Fe(OH)3膠體時,從側面可以看到一條光亮通路 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸與氫氧化鈉溶液反應:H++OH-═H2O | |
| B. | 碳酸鈣與稀硝酸的反應:CO32-+2H+═CO2+H2O | |
| C. | 銅與稀硫酸反應:Cu+2H+═Cu2++H2↑ | |
| D. | 氯氣與氫氧化鈉溶液反應:Cl2+OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
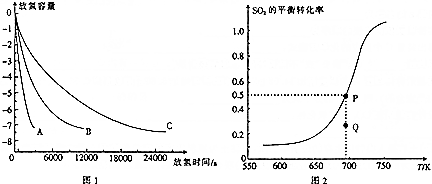
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com