
【題目】室溫時,向 20 mL 0.1 mol·L 1 的兩種酸 HA、HB 中分別滴加0.1 mol·L 1 NaOH 溶液, 其 pH 變化分別對應下圖中的 I、II。下列說法不正確的是( )
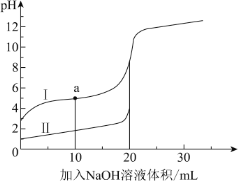
A.向 NaA 溶液中滴加 HB 可產生 HA
B.滴加 NaOH 溶液至 pH=7 時,兩種溶液中 c(A-)=c(B-)
C.a 點,溶液中微粒濃度:c(A-) > c(Na+)
D.滴加 20 mL NaOH 溶液時,I 中 H2O 的電離程度大于 II 中
【答案】B
【解析】
A. 由圖可知,0.1 mol·L1 HB溶液的pH小于等濃度的HA溶液,說明HB的酸性強于HA,由強酸制弱酸的原理可知,向NaA 溶液中滴加 HB 可產生 HA,A正確;
B. 由于HB的酸性強于HA,等濃度的HB溶液和HA溶液中,滴加NaOH溶液 pH=7 時,消耗NaOH溶液的體積不同,溶液中c(Na+)不同,則兩種溶液中 c(A-)一定不等于c(B-),B錯誤;
C. a點為等濃度的HA和NaA混合液,溶液呈酸性,說明HA的電離大于NaA的水解,溶液中微粒濃度:c(A-)>c(Na+),C正確;
D. 滴加 20 mL NaOH 溶液時,等濃度的HB溶液和HA溶液均恰好完全反應生成NaB和NaA,由于HB的酸性強于HA,則NaA的水解程度大于NaB,Ⅰ中H2O的電離程度大于Ⅱ中,D正確;
故答案為B。


科目:高中化學 來源: 題型:
【題目】電導率是衡量電解質溶液導電能力大小的物理量,根據溶液電導率變化可以確定滴定反應的終點。在一定溫度下,用0.1mol/LKOH溶液分別滴定體積均為20mL、濃度均為0.1mol/L的鹽酸和醋酸溶液,滴定曲線如圖所示。下列有關判斷正確的是
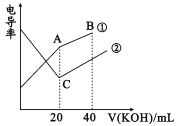
A. B點的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A點的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C點水電離的c(OH-)大于A點水電離的c(OH-)
D. A、B、C三點溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】粉煤灰是燃煤產生的重要污染物,主要成分有Al2O3、Fe2O3、Fe3O4和SiO2等物質。綜合利用粉煤灰不僅能夠防止環境污染,還能獲得納米Fe2O3等重要物質。
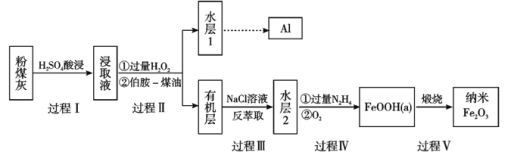
已知:
i)伯胺R-NH2能與Fe3+反應:3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的產物。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的產物。
ii)Fe3+在水溶液中能與Cl-反應:Fe3++6Cl-![]() [FeCl6]3-,回答下列問題:
[FeCl6]3-,回答下列問題:
(1)過程I對煤粉灰進行酸浸過濾后,濾渣的主要成分是_____________。
(2)寫出過程Ⅱ加入過量H2O2發生的離子方程式_____________。加入伯胺-煤油對浸取液進行分離,該操作的名稱是_____________。
(3)從化學平衡角度解釋過程Ⅲ利用NaCl溶液進行反萃取的原理_____________。
(4)過程Ⅳ中過量的N2H4將水層2中[FeCl6]3-轉化為Fe2+,得到的Fe2+再被O2氧化為FeOOH,其中第一步的離子方程式為4[FeCl6]3-+5N2H4=4Fe2++N2+4N2H5++24Cl-,該反應中氧化劑與還原劑的物質的量之比為_______________。
(5)在常壓用納米Fe2O3電化學法合成氨的裝置如圖所示。已知電解液為熔融NaOH-KOH,納米Fe2O3在陰極發生電極反應分兩步進行:
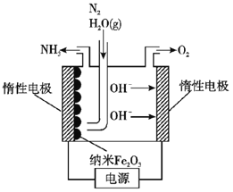
第一步:Fe2O3+3H2O+6e-=2Fe+6OH-;
第二步:2Fe+N2+3H2O=Fe2O3+2NH3。
則該電解池發生總反應的化學方程式為___________________________________,納米Fe2O3在電解過程中所起的作用是___________________________________。
(6)某特殊的磁流體材料,其化學式通式為KxFeO2(其組成可理解為aK2O·bFeO·cFe2O3),若x平均值為1.3,則磁流體中Fe3+和Fe2+的質量之比為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨和聯氨(N2H4)是氮的兩種常見化合物,在科學技術和生產中有重要的應用。
根據題意完成下列計算:
(1)聯氨用亞硝酸氧化生成氮的另一種氫化物,該氫化物的相對分子質量為43.0,其中氮原子的質量分數為0.977,計算確定該氫化物的分子式___________。該氫化物受撞擊則完全分解為氮氣和氫氣。4.30 g該氫化物受撞擊后產生的氣體在標準狀況下的體積為___________L。
(2)聯氨和四氧化二氮可用作火箭推進劑,聯氨是燃料,四氧化二氮作氧化劑,反應產物是氮氣和水。
由聯氨和四氧化二氮組成的火箭推進劑完全反應生成72.0 kg水,計算推進劑中聯氨的質量___________。
(3)氨的水溶液可用于吸收NO與NO2混合氣體,反應方程式為6NO+ 4NH3=5N2+6H2O,6NO2+ 8NH3=7N2+12H2O;NO與NO2混合氣體180 mol被8.90×103g氨水(質量分數0.300)完全吸收,產生156 mol氮氣。吸收后氨水密度為0.980 g/cm3。計算:①該混合氣體中NO與NO2的體積比____________。②吸收后氨水的物質的量濃度_______________(答案保留1位小數)。
(4)氨和二氧化碳反應可生成尿素CO(NH2)2。尿素在一定條件下會失去氨而縮合,如兩分子尿素失去一分子氨形成二聚物:
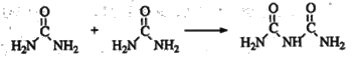 +NH3
+NH3
已知常壓下120 mol CO(NH2)2在熔融狀態發生縮合反應,失去80 mol NH3,生成二聚物(C2H5N3O2)和三聚物。測得縮合產物中二聚物的物質的量分數為0.60,推算縮合產物中各縮合物的物質的量之比__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒溫恒容的密閉容器中通入一定量的A、B,發生反應A(g)+2B(g)![]() 3C(g)。如圖是A的反應速率v(A)隨時間變化的示意圖。下列說法正確的是( )
3C(g)。如圖是A的反應速率v(A)隨時間變化的示意圖。下列說法正確的是( )

A.反應物A的濃度:a點小于b點
B.該反應的某種生成物可能對反應起催化作用
C.曲線上的c、d兩點都表示達到平衡狀態
D.A的平均反應速率:ab段大于bc段
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新冠疫情期間某同學嘗試在家自制含氯消毒劑。用兩根鉛筆芯(C1 和C2)、電源適配器和水瓶組裝如圖所示的裝置。接通電源觀察到:C1 周圍產生細小氣泡,C2 周圍無明顯現象;持續通電一段時間后,C2 周圍產生細小氣泡。此時停止通電,拔出電極,旋緊瓶塞,振蕩搖勻,制備成功。關于該實驗的說法不正確的是

A.C1電極產生氣泡原因:![]()
B.可以用兩根鐵釘代替鉛筆芯完成實驗
C.自制消毒劑的總反應為:NaCl+H2O ![]() NaClO+H2↑
NaClO+H2↑
D.實驗過程中要注意控制電壓、開窗通風、導出氫氣,確保安全
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,四種均為0.1molL﹣1的溶液,其pH如下表所示,下列關系不正確的是( )
序號 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaHCO3 |
|
pH | 7.0 | 7.0 | 8.4 | 9.9 |
A.酸性:H2CO3>![]()
B.水電離產生的c(H+):①=②
C.溶液③中:c(HCO3-)+c(CO32-)+c(H2CO3)= 0.1molL﹣1
D.溶液④中:c(Na+)>c(![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年我國大力加強溫室氣體CO2催化氫化合成甲醇技術的工業化生產研究,實現可持續發展。
(1)已知:CO2(g)+H2(g)![]() H2O(g) +CO(g) ΔH1= + 41.1 kJmol-1 CO(g)+2H2(g)
H2O(g) +CO(g) ΔH1= + 41.1 kJmol-1 CO(g)+2H2(g)![]() CH3OH(g) ΔH2=-90.0 kJmol-1
CH3OH(g) ΔH2=-90.0 kJmol-1
寫出CO2催化氫化合成甲醇的熱化學方程式:_________________________________。
(2)為提高CH3OH產率,理論上應采用的條件是_______________________(填字母)。
A.高溫高壓 B.低溫低壓 C.高溫低壓 D.低溫高壓
(3)250℃、在恒容密閉容器中由CO2(g)催化氫化合成CH3OH(g),下圖為不同投料比[n(H2)/n(CO2)]時某反應物X 平衡轉化率變化曲線。

① 反應物X 是_____(填“CO2”或“H2”)。
② 判斷依據是_____。
(4)250℃、在體積為 2.0L 的恒容密閉容器中加入6mol H2、2mol CO2和催化劑,10min 時反應達到平衡,測得 c(CH3OH) = 0.75 mol·L-1。
① 前 10min 的平均反應速率 v(H2)=_____mol·L-1·min-1。
② 經計算化學平衡常數 K =_____________________。
③ 催化劑和反應條件與反應物轉化率和產物的選擇性有高度相關。控制相同投料比和相同反應時間,四組實驗數據如下:
實驗編號 | 溫度(K) | 催化劑 | CO2轉化率(%) | 甲醇選擇性(%) |
A | 543 | Cu/ZnO 納米棒 | 12.3 | 42.3 |
B | 543 | Cu/ZnO 納米片 | 11.9 | 72.7 |
C | 553 | Cu/ZnO 納米棒 | 15.3 | 39.1 |
D | 553 | Cu/ZnO 納米片 | 12.0 | 70.6 |
(注:甲醇選擇性是指的是轉化的CO2中生成甲醇的百分含量)
根據上表所給數據,用CO2生產甲醇的最優選項為_____(填字母)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將4 mol A氣體和2 mol B氣體在2 L的容器中混合并在一定條件下發生如下反應:2A(氣)+B(氣)![]() 2C(氣)。若經2 s(秒)后測得C的濃度為0.6 mol·L-1,現有下列幾種說法:
2C(氣)。若經2 s(秒)后測得C的濃度為0.6 mol·L-1,現有下列幾種說法:
①用物質A表示的反應平均速率為0.3 mol·L-1·s-1
②用物質B表示的反應的平均速率為0.6 mol·L-1·s-1
③2s時物質A的轉化率為70%
④2s時物質B的濃度為0.7 mol·L-1
其中正確的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com