
分析 根據混合物、電解質、非電解質、非金屬單質、堿類物質的定義判斷;根據物質導電的原因判斷.
混合物:含有的物質有多種;
能導電的物質必須有自由電子或離子;
非電解質:在水溶液里或熔融狀態下都不導電的化合物;
堿:在水溶液里,電離出的陰離子全部是氫氧根離子的化合物.
解答 解:A蔗糖(C12H22O11)不能導電,屬于化合物,是非電解質;
B碘的酒精溶液不能導電,屬于混合物,既不是電解質也不是非電解質;
C純堿不能導電,溶于水或熔融狀態下能導電,屬于電解質;
D燒堿不能導電,溶于水或熔融狀態下能導電,屬于電解質;
E二氧化碳不能導電,其溶于水能導電的原因是生成了碳酸,碳酸導電,屬于非電解質;
F石墨能導電,是非金屬單質,既不是電解質也不是非電解質;
G硫酸鋁溶液能導電,屬于混合物,既不是電解質也不是非電解質;故答案為:①BG; ②D; ③CD; ④FG.
點評 本題考查了混合物與純凈物、電解質與非電解質的區別,側重考查學生的辨別能力;知道:能導電的物質不一定是電解質,如金屬單質;電解質不一定導電,如氯化鈉晶體.


科目:高中化學 來源: 題型:解答題

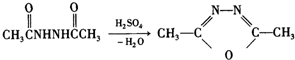
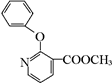 +H2N-NH2→
+H2N-NH2→ ,
, ,
,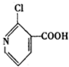 有多種同分異構體,其中符合下列條件的同分異構體共有4種.
有多種同分異構體,其中符合下列條件的同分異構體共有4種.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 發生了顏色變化的一定是化學變化 | |
| B. | 有氣泡產生或固體析出的變化一定是化學變化 | |
| C. | 用糯米、酒曲和水制成甜酒釀一定是化學變化 | |
| D. | 氧化還原反應中肯定有一種元素被氧化,而另一種元素被還原 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在氧化還原反應中,非金屬單質一定是氧化劑 | |
| B. | 某元素從化合態變為游離態時,該元素一定被還原 | |
| C. | 金屬陽離子被還原不一定得到金屬單質 | |
| D. | 氧化還原反應中所有元素的化合價都發生變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
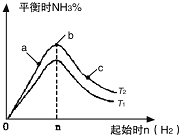 利用N2和H2可以實現NH3的工業合成,而氨又可以進一步制備硝酸.
利用N2和H2可以實現NH3的工業合成,而氨又可以進一步制備硝酸.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
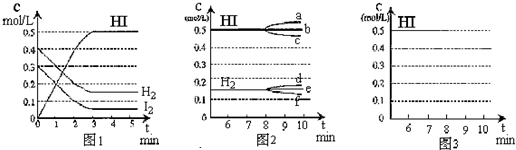
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①⑥③⑥⑤⑥ | B. | ②⑥③⑥⑤⑥ | C. | ①⑥④⑥⑤⑥ | D. | ②⑥④⑥⑤⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com