
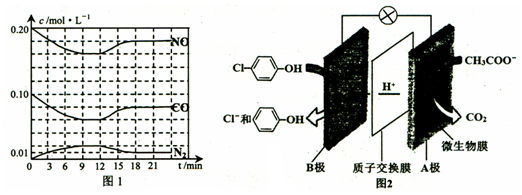
 )的酸性廢水;可利用微生物電池法除去,其原理如圖2所示.
)的酸性廢水;可利用微生物電池法除去,其原理如圖2所示. -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-.
-OH+Cl-.分析 Ⅰ.(1)依據圖象讀出平衡濃度,結合平衡常數概念計算平衡常數;
(2)12min后反應物濃度增大,生成物濃度減小,說明平衡逆向進行;
(3)根據濃度商和平衡常數比較判斷反應進行的方向;
Ⅱ.(4)根據原電池中陽離子的移動方向確定正負極;
(5)B為負極,發生氧化反應;
(6)由電極反應式結合電子得失守恒來計算.
解答 解Ⅰ.(1):依據圖象分析,第一次達到平衡時時平衡狀態下物質的濃度為c(NO)=0.16mol/L,c(CO)=0.06mol/L,c(N2)=0.02mol/L,c(CO2)=0.04mol/L,反應的平衡常數K=$\frac{c({N}_{2}){c}^{2}(C{O}_{2})}{{c}^{2}(NO){c}^{2}(CO)}$=$\frac{0.02×0.04×0.04}{0.16×0.16×0.06×0.06}$=0.347L•mol-1;
故答案為:0.347L•mol-1;
(2)12min后反應物濃度增大,生成物濃度減小,說明平衡逆向進行,反應是放熱反應,升溫改變符合圖象變化;
故答案為:升溫;因反應速率加快且反應逆向移動,對放熱反應而言,改變條件為升溫;
(3)24min時,各物質的濃度為c(NO)=0.18mol/L,c(CO)=0.08mol/L,c(N2)=0.01mol/L,c(CO2)=0.02mol/L,反應的平衡常數K=$\frac{0.01×0.0{2}^{2}}{0.1{8}^{2}×0.0{8}^{2}}$=0.019,
若保持溫度不變,此時再向容器中充入CO、N2各0.060mol,c(NO)=0.18mol/L,c(CO)=0.14mol/L,c(N2)=0.07mol/L,c(CO2)=0.02mol/L,濃度商計算Qc=$\frac{0.07×0.0{2}^{2}}{0.1{8}^{2}×0.1{4}^{2}}$=0.044>K,平衡逆向進行,
故答案為:逆向;
Ⅱ(4)原電池中氫離子的移動方向是從負極流向正極,所以B是電池的正極,A位電池的負極,
故答案為:負;
(5)A為負極,發生氧化反應,電極方程式為CH3COO--8e-+2H2O=2CO2+7H+,B為正極,正極上發生得電子的還原反應:Cl- -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-,
-OH+Cl-,
故答案為:Cl- -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-;
-OH+Cl-;
(6)由圖2可知,B極即正極反應為:Cl- -OH+2e-+H+═
-OH+2e-+H+═ -OH+Cl-,B極區溶液體積為1L,pH從4變到1,故△n(H+)=0.1mol,則知B極得0.2mol電子,
-OH+Cl-,B極區溶液體積為1L,pH從4變到1,故△n(H+)=0.1mol,則知B極得0.2mol電子,
根據正負極得失電子數相等可知,負極失去的電子數也為0.2mol,根據負極反應:CH3COO--8e-+2H2O=2CO2+7H+,可知,處理掉的乙酸鈉的物質的量為$\frac{0.2}{8}$mol,故質量為:$\frac{0.2}{8}$×82g/mol=2.05g.
故答案為:2.05g.
點評 本題為綜合題,考查了化學平衡常數的計算及應用、影響化學平衡移動的因素、原電池工作原理,題目難度中等,注意原電池的計算依據正極得到電子數目等于負極失去電子數目.


科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1NaOH溶液:K+、Na+、SO42-、CO32- | |
| B. | 能與鋁反應放出氫氣的溶液中:K+、SO42-、NO3-、NH4+ | |
| C. | 0.1 mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Y單質能溶于X元素的最高價氧化物的水化物 | |
| B. | W2能與H2Z發生置換反應 | |
| C. | 離子半徑由大到小:Z2->X+>Y3+>W2- | |
| D. | W、X形成兩種離子化合物,陰、陽離子個數比一定是1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH值都為4的稀鹽酸和NH4Cl溶液中,水的電離程度相同 | |
| B. | 濃度均為0.1mol/L的醋酸和NaOH溶液等體積混合后:lg[$\frac{c({H}^{+})}{c(O{H}^{-})}$]=0 | |
| C. | 在含濃度都為0.01mol/L的Cl-、CrO42-的混合溶液中滴加AgNO3溶液,先出現沉淀的是AgCl.[已知:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12] | |
| D. | 濃度均為0.1mol/L的NH4Cl和CH3COONH4溶液中,c(NH4+)相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
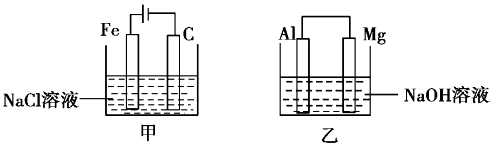
| A. | 甲裝置中有沉淀生成,乙裝置中Mg電極上有氣泡生成 | |
| B. | 反應后,甲裝置中溶液的質量增大,乙裝置中溶液的質量減小 | |
| C. | 電極反應式:甲中陽極Fe-2e-=Fe2+,乙中負極Mg-2e-=Mg2+ | |
| D. | 反應后甲中溶液的pH減小,乙中溶液的pH增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
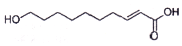 王漿酸是蜂王漿中特有的一種不飽和脂肪酸,在自然界中只有蜂王漿中才含有這種物質.其結構簡式如圖:下列有關干漿酸的結構與性質的說法正確的是( )
王漿酸是蜂王漿中特有的一種不飽和脂肪酸,在自然界中只有蜂王漿中才含有這種物質.其結構簡式如圖:下列有關干漿酸的結構與性質的說法正確的是( )| A. | 含有兩種官能團 | |
| B. | 與足里NaOH反應生成Cl0H18O3Na2 | |
| C. | 能發生加成反應,氧化反應、取代反應、加聚反應 | |
| D. | 能使Br/CCl4溶液、酸性KMnO4溶液褪色,褪色原理相同 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com