
 C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、
C(g)+D(g)過程中的能量變化如右圖所示,判斷該反應△H 0(填“>”、“<”、

科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
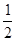 O2(g) = H2O(g) ΔH1=a kJ·mol-1?
O2(g) = H2O(g) ΔH1=a kJ·mol-1?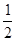 O2(g) = H2O(l) ΔH2=b kJ·mol-1??
O2(g) = H2O(l) ΔH2=b kJ·mol-1??| 化學鍵 | H-H | N-H | N≡N |
| 鍵能/kJ·mol-1 | 436 | 391 | 945 |
 2NH3(g) △H=a kJ·mol-1。試根據表中所列鍵能數據估算a 的值: (寫出 + 或-)。
2NH3(g) △H=a kJ·mol-1。試根據表中所列鍵能數據估算a 的值: (寫出 + 或-)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 (g)+1/2O
(g)+1/2O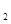 (g)=CO(g)+2H
(g)=CO(g)+2H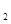 (g)
(g)  H1=-35.6kJ·mol
H1=-35.6kJ·mol
 (g)+2O
(g)+2O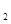 (g)=CO2(g)+2H2O(g)
(g)=CO2(g)+2H2O(g)  H2=-890.3kJ·mol
H2=-890.3kJ·mol
 (g)+CO
(g)+CO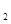 (g)=2CO(g)+2H
(g)=2CO(g)+2H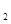 (g)
(g)  H3=247.3kJ·mol
H3=247.3kJ·mol
| 時間/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/( mol ·/L-1) | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
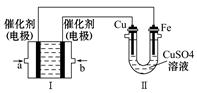
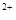 的物質的量濃度 。
的物質的量濃度 。查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 O2(g)=
O2(g)= P4O10(s) △H=-738.5kJ·mol-1
P4O10(s) △H=-738.5kJ·mol-1 查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.△H=-1141.8 kJ·mol-1 | B.△H=+260.4kJ·mol-1 |
| C.△H=+441.8 kJ·mol-1 | D.△H=-260.4 kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 (g)+3H
(g)+3H (g)="==" 2NH
(g)="==" 2NH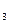 (g) △H= -92.4kJ/mol,則斷裂 1 mol N≡N鍵需要吸收的熱量為( )
(g) △H= -92.4kJ/mol,則斷裂 1 mol N≡N鍵需要吸收的熱量為( )| A.431 kJ | B.649kJ | C.945.6kJ | D.869 kJ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com