
| 元素 | 相關信息 |
| X | X的基態原子L層電子數是K層電子數的2倍 |
| Y | Y的基態原子最外層電子排布式為:nsnnpn+2 |
| Z | Z存在質量數為23,中子數為12的核素 |
| W | W有多種化合價,其白色氫氧化物在空氣中會迅速變成灰綠色,最后變成紅褐色 |
分析 X、Y、Z、W是元素周期表前四周期中的常見元素,X的基態原子L層電子數是K層電子數的2倍,所以X基態原子核外有6個電子,則X是C元素;
Y的基態原子最外層電子排布式為:nsnnpn+2,s能級上最多排2個電子,且p能級上還有電子,所以n為2,則Y的基態原子最外層電子排布式為:2s22p4,所以Y是O元素;
Z存在質量數為23,中子數為12的核素,則其質子數是11,所以Z是Na元素;
W有多種化合價,其白色氫氧化物在空氣中會迅速變成灰綠色,最后變成紅褐色,氫氧化亞鐵在空氣中會迅速變成灰綠色,最后變成紅褐色氫氧化鐵,所以W是Fe,據此進行解答.
解答 解:X、Y、Z、W是元素周期表前四周期中的常見元素,X的基態原子L層電子數是K層電子數的2倍,所以X基態原子核外有6個電子,則X是C元素;Y的基態原子最外層電子排布式為:nsnnpn+2,s能級上最多排2個電子,且p能級上還有電子,所以n為2,則Y的基態原子最外層電子排布式為:2s22p4,所以Y是O元素;Z存在質量數為23,中子數為12的核素,則其質子數是11,所以Z是Na元素;W有多種化合價,其白色氫氧化物在空氣中會迅速變成灰綠色,最后變成紅褐色,氫氧化亞鐵在空氣中會迅速變成灰綠色,最后變成紅褐色氫氧化鐵,所以W是Fe元素,
(1)同周期隨原子序數增大,元素電負性增大,故C的電負性比O的小,
故答案為:小;
(2)W為鐵元素,它的基態原子核外電子排布式為:1s22s22p63s23p63d64s2,則價電子排布式是3d64s2;
Z2Y2與XY2分別為Na2O2、CO2,二者反應生成碳酸鈉和氧氣,反應的化學方程式為:2Na2O2+2CO2═2Na2CO3+O2;1mol過氧化鈉與二氧化碳完全反應生成0.5mol氧氣,轉移了1mol電子,轉移的電子數目為NA(或6.02×1023),
故答案為:3d64s2; 2Na2O2+2CO2═2Na2CO3+O2;NA(或6.02×1023);
(3)X、Y分別為C、O元素,與C、O元素形成的一種分子與該無機陰離子在水溶液中反應的離子方程式為:CO2+CO32-+H2O═2HCO3-,
故答案為:CO2+CO32-+H2O═2HCO3-;
(4)X為C元素,Y為Si元素,二者形成的化合物分別為甲烷、SiH4,二者形成的晶體都是分子晶體,相對分子質量越大,分子間作用力越強,其沸點越高,則沸點較高的為SiH4,
故答案為:SiH4.
點評 本題考查了位置結構與性質關系的應用,題目難度中等,推斷元素為解答關鍵,注意熟練掌握原子結構與元素周期律、元素周期表的關系,試題培養了學生的分析、理解能力及靈活應用能力.


科目:高中化學 來源: 題型:選擇題
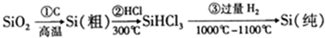 ,下列說法正確的是( )
,下列說法正確的是( )| A. | 步驟①的化學方程式為:SiO2+C$\frac{\underline{\;高溫\;}}{\;}$Si+CO2↑ | |
| B. | 步驟①②③中每生成或反應1mol Si,轉移2mol電子 | |
| C. | 二氧化硅能與氫氟酸反應,而硅不能與氫氟酸反應 | |
| D. | SiHCl3(沸點33.0℃)中含有少量的SiCl4(沸點67.6℃),通過蒸餾(或分餾)可提純SiHCl3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
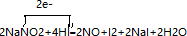 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
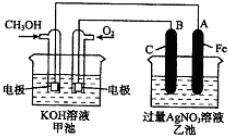
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將pH=3和pH=5的硫酸溶液等體積混合,所得溶液的pH約為3.3 | |
| B. | 1 L 0.5 mo1•L-1稀硫酸與1 L 1 mo1•L-1NaOH溶液混合反應放出57.3 kJ的熱量,則表示中和熱的熱化學方程式為: H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(1),△H=-114.6 kJ•mo1-l | |
| C. | 已知室溫時,0.1 mol•L-1某一元酸HA的電離平衡常數約為1×10-7,則該酸的電離度為0.01% | |
| D. | 已知常溫下Ag2CrO4的Ksp=1.12×10-12.將等體積的2×10-4mol•L-1 AgNO3溶液和2×10-4 mol•L-1 K2CrO4溶液混合,則有Ag2CrO4沉淀產生 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.01mol•L-1 H2SO4 | B. | pH=2的H2SO4溶液 | ||
| C. | c(OH-)=10-13mol•L-1 | D. | pH=1溶液加水稀釋1倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 陰離子的還原性:Z>Y>X | B. | 單質的非金屬性:X>Y>Z | ||
| C. | 氣態氫化物的穩定性:X<Y<Z | D. | 原子原子半徑:X>Y>Z |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com