
【題目】下列說法中正確的是( )
A. 烯中C=C的鍵能是乙烷中C-C的鍵能的2倍
B. 氮氣分子中含有1個s鍵和2個p鍵
C. N-O鍵的極性比C-O鍵的極性大
D. NH4+中4個N-H鍵的鍵能不相同
【答案】B
【解析】
A.碳碳雙鍵的鍵能大于碳碳單鍵的鍵能,小于碳碳單鍵的鍵能的2倍;
B.單鍵中只有![]() 鍵,雙鍵中有一個
鍵,雙鍵中有一個![]() 鍵和一個
鍵和一個![]() 鍵,三鍵中有一個
鍵,三鍵中有一個![]() 鍵和兩個
鍵和兩個![]() 鍵;
鍵;
C. 形成共價鍵的兩個原子對電子的吸引能力差別越大,共價鍵的極性就越強;
D.銨根離子中存在四個N-H共價鍵,這四個共價鍵采用sp3雜化。
有機化合物中,碳原子與碳原子的原子軌道之間以“肩并肩”的方式形成p鍵的重疊程度要比以“頭碰頭”的方式形成s鍵的重疊程度小得多。兩個碳原子之間形成的s鍵比p鍵牢固,s鍵的鍵能大于p鍵,
A.乙烯中兩個碳原子間存在一個s鍵和一個p鍵,乙烷中兩個碳原子間存在一個s鍵,乙烯中C=C的鍵能應當大于乙烷中C-C的鍵能且小于乙烷中C-C的鍵能的2倍,故A錯誤;
B.氮氣分子中有三個共價鍵,1個s鍵和2個p鍵,故B正確;
C.形成共價鍵的兩個原子對電子的吸引能力差別越大,共價鍵的極性就越強;N原子與O原子吸電子能力的差值小于C與O吸電子能力的差值,N-O鍵的極性比C-O鍵的極性小,故C錯誤;
D.在NH4+中參與成鍵的8個電子分布在原子最外層的4個能量相等的sp3雜化軌道中,4個N-H鍵的鍵能鍵長鍵角都相等,故D錯誤;
綜上所述,本題選B。


 中考解讀考點精練系列答案
中考解讀考點精練系列答案 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案科目:高中化學 來源: 題型:
【題目】含第VA族的磷、砷(As)等元素的化合物在研究和生產中有許多重要用途。回答下列問題:
(1)基態P原子的核外電子排布式為____,有____個未成對電子。
(2)常溫下PCl5是一種白色晶體,其立方晶系晶體結構模型如圖甲所示,由A、B兩種微粒構成。將其加熱至148℃熔化,形成一種能導電的熔體。已知A、B兩種微粒分別與CC14、SF6互為等電子體,則A為____,其中心原子雜化軌道類型為____,B為____。
(3)PO43-的空間構型為____,其等電子體有____(請寫出一種)。
(4)砷化鎵屬于第三代半導體,它能直接將電能轉變為光能,砷化鎵燈泡壽命是普通燈泡的100倍,而耗能只有其10%。推廣砷化鎵等發光二極管(LED)照明,是節能減排的有效舉措。已知砷化鎵的晶胞結構如圖乙,晶胞參數a= 565pm。
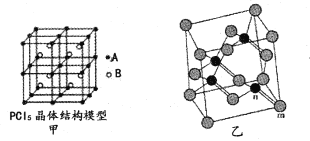
①砷化鎵的化學式為____,鎵原子的配位數為____。
②砷化鎵的晶胞密度=____g/cm3(列式并計算,精確到小數點后兩位),m位置Ga原子與n位置As原子之間的距離為____pm(列式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應不屬于四種基本反應類型,但屬于氧化還原反應的是( )
A.Fe+CuSO4=FeSO4+Cu
B.AgNO3+NaCl=AgCl↓+NaNO3
C.Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將 0.2mol MnO2和 50mL 12molL﹣1濃鹽酸混合后緩緩加熱,反應完全后,再向溶液中加入足量 AgNO3溶液,生成 AgCl 沉淀的物質的量為(不考慮鹽酸的揮發)( )
A. 大于 0.3 mol,小于 0.6 mol B. 等于 0.3 mol
C. 小于 0.3 mol D. 大于 0.6 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】完成下列化學用語:
(1)畫出 O2﹣結構示意圖:_____,某種核素質量數 37,中子數 20,其原子符號:_____
(2)寫出實驗室制氯氣的化學方程式:______________________
(3)工廠里常用濃氨水來檢驗氯氣管道是否泄漏,其原理為:8NH3+3Cl2=6NH4Cl+N2,請用雙線橋表示其電子轉移的方向和數目__________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,向20mL0.1 mol/L H2R溶液中滴加0.1 mol/LNaOH溶液,溶液的pH隨NaOH溶液體積的變化如圖所示。已知pKa=﹣lgKa,二元弱酸H2R的pKa1=1.89,pKa2=7.21。下列有關說法錯誤的是

A. 溶液的導電性:點a弱于點b
B. 離子濃度c(R2-):點c小于點d
C. H2R + R2-=2HR-平衡常數>105,反應趨于完全
D. 點b時,y<7且![]() <1
<1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在盛有稀硫酸的燒杯中放入用導線連接的電極X、Y,外電路中電子流向如圖所示。下列關于該裝置的判斷正確的是( )

A.外電路的電流方向為X→外電路→Y
B.若兩電極分別為Fe和石墨棒,則X為Fe,Y為石墨棒
C.X極上發生的是還原反應,Y極上發生的是氧化反應
D.溶液中陽離子向X極移動,陰離子向Y極移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定量純凈的氨基甲酸銨置于密閉真空恒容容器中(固體試樣體積忽略不計),在恒定溫度下使其達到分解平衡:NH2COONH4(s)![]() 2NH3(g)+CO2(g) △H = + a kJ·mol-l。能判斷該分解反應已經達到化學平衡的是( )
2NH3(g)+CO2(g) △H = + a kJ·mol-l。能判斷該分解反應已經達到化學平衡的是( )
A. v(NH3)=2v(CO2) B. 密閉容器中NH3體積分數不變
C. 反應吸收a kJ熱量 D. 密閉容器中混合氣體的密度不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究氮氧化物與懸浮在大氣中海鹽粒子的相互作用時,同溫度下涉及如下反應:
①2NO(g)+Cl2(g)![]() 2ClNO(g) ΔH1<0,平衡常數為K1;
2ClNO(g) ΔH1<0,平衡常數為K1;
②2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) ΔH2<0,平衡常數為K2。
NaNO3(s)+ClNO(g) ΔH2<0,平衡常數為K2。
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常數K=___________________(用K1、K2表示)。ΔH3=___________(用ΔH1、ΔH2表示)。
2NaNO3(s)+2NO(g)+Cl2(g) ΔH3,平衡常數K=___________________(用K1、K2表示)。ΔH3=___________(用ΔH1、ΔH2表示)。
(2)為研究不同條件對反應①的影響,在恒溫條件下,向2 L恒容密閉容器中加入0.2 mol NO和0.1 mol Cl2,10 min時反應①達到平衡。測得10 min內v(ClNO)=7.5×10-3mol·L-1·min-1,則平衡后n(Cl2)=__________mol,NO的轉化率α1=___________。其他條件保持不變,反應①在恒壓條件下進行,平衡時NO的轉化率為α2,α1____α2(填“>”“<”或“=”),平衡常數K1______________(填“增大”“減小”或“不變”)。若要使K1減小,可采用的措施是___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com