
【題目】已知物質A~I之間的轉化關系符合下圖所示.其中A、C、F、G、I為常見固體且焰色反應均為黃色;A為海水中主要溶質,B為常溫下常見液體;E為黃綠色氣體,H是無色無味且能使澄清石灰水變渾濁的氣體.
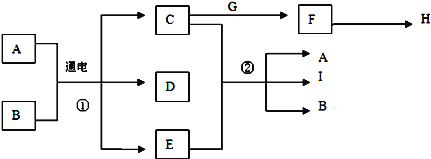
試回答下列問題:
(1)D的化學式為__________。
(2)反應①的化學方程式為:____________________________。
(3)反應②的離子方程式為:____________________________。
(4)寫出鎂條在H氣體中燃燒的反應方程式為:___________________________。
(5)G在水中的電離方程式_____________________________。
(6)在A、I和B的混合物中加入稀硫酸,有黃綠色氣體產生,寫出該反應的化學方程式_____。
【答案】H2 2NaCl+ 2H2O ![]() H2↑ + Cl2↑ + 2NaOH Cl2 + 2OH- == Cl- + ClO- + H2O 2Mg +CO2
H2↑ + Cl2↑ + 2NaOH Cl2 + 2OH- == Cl- + ClO- + H2O 2Mg +CO2![]() 2MgO+C NaHCO3 = Na+ +HCO3- NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O
2MgO+C NaHCO3 = Na+ +HCO3- NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O
【解析】
A、C、F、G、I為常見固體且焰色反應均為黃色,說明均有鈉元素,A為海水中主要溶質,則A為NaCl,B為常溫下常見液體,則B為H2O;E為黃綠色氣體,則E為Cl2,H是無色無味且能使澄清石灰水變渾濁的氣體,則H為CO2,根據題中各物質轉化關系,電解食鹽水得C、D、E,C中含有鈉元素,則C為NaOH,則D為H2,C與E反應生成A、I、B,則I為NaClO,C、F、G均含有鈉元素,F能產生二氧化碳,則G為NaHCO3,F為Na2CO3。(1)D的化學式為H2;(2)反應①的化學方程式為:2NaCl+ 2H2O ![]() H2↑ + Cl2↑ + 2NaOH;(3)反應②的離子方程式為:Cl2 + 2OH- == Cl- + ClO- + H2O;(4)鎂條在CO2氣體中燃燒的反應方程式為:2Mg +CO2
H2↑ + Cl2↑ + 2NaOH;(3)反應②的離子方程式為:Cl2 + 2OH- == Cl- + ClO- + H2O;(4)鎂條在CO2氣體中燃燒的反應方程式為:2Mg +CO2![]() 2MgO+C;(5)G為NaHCO3,在水中的電離方程式為:NaHCO3 = Na+ +HCO3-;(6)在A、I和B的混合物中加入稀硫酸,有黃綠色氣體產生,反應的化學方程式為:NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O。
2MgO+C;(5)G為NaHCO3,在水中的電離方程式為:NaHCO3 = Na+ +HCO3-;(6)在A、I和B的混合物中加入稀硫酸,有黃綠色氣體產生,反應的化學方程式為:NaCl+NaClO+H2SO4== Cl2↑+ Na2SO4+ H2O。


科目:高中化學 來源: 題型:
【題目】下圖表示細胞中四種有機化合物的組成及主要功能。回答下列問題:
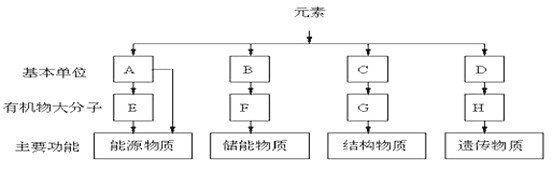
(1)圖中的基本單位A是_________。利用A合成的E主要分布在人和動物的_________中,當人和動物血液中的A低于正常含量時,一些細胞中的E便分解產生A及時補充。
(2)與圖中的E相比,F是細胞內更良好的儲能物質,原因是其分子中氧的含量________,而氫的含量_________。分布在內臟器官周圍的F還具有_________的作用,可以保護內臟器官。
(3)圖中的C在生物體中約有20種,其中有一部分在人體細胞不能合成,必須從外界環境中直接獲取,這部分C叫做_________。由C通過__________的方式結合在一起形成G,C分子之間通過_________(用化學結構簡式表示)連接。
(4)圖中H的中文名稱是_________,煙草葉肉細胞的H徹底水解的產物是___________________________________________________________。
(5)上述生物大分子都以____________為骨架。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某工廠用提取粗鹽后的鹽鹵(主要成分為MgCl2)制備金屬鎂,其工藝流程如下,下列說法中,錯誤的是( )
![]()
A. 操作①發生的反應為非氧化還原反應
B. 若在實驗室進行操作①只需要漏斗和燒杯兩種玻璃儀器
C. 操作②是蒸發濃縮結晶
D. 在整個制備過程中,未發生置換反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)配平下列離子方程式:______
Ce3++ H2O2+ H2O === Ce(OH)4↓+_______H+
(2)已知某待測液由Ag+、Mg2+、K+、Ba2+、NH4+、NO3-中的若干種離子組成,進行如下實驗:
第一步:加入過量的稀鹽酸,有白色沉淀生成。
第二步:過濾,在濾液中加入過量的稀硫酸,又有白色沉淀生成。
第三步:再過濾,取少量濾液,逐漸滴入NaOH溶液至溶液呈堿性,在此過程中沒有沉淀和氣體產生,加熱該溶液,可產生使濕潤的紅色石蕊試紙變藍色的氣體。
根據實驗現象回答:
①寫出第三步加熱該溶液后,有氣體生成的反應的離子方程式:_________________;
②待測液中一定含有_______和NO3-離子,一定不含有_________離子,還有一種離子不能確定其是否存在,要檢驗這種離子的實驗方法是(填寫實驗名稱)___________。
③往含等物質的量CO32-和HCO3-的溶液中滴入HCl溶液,下列表示產生的氣體在標準狀況下的體積與加入的HCl溶液體積關系圖正確的是_________。
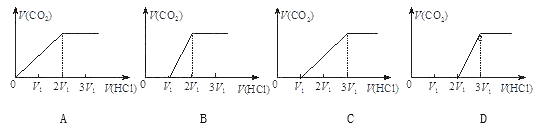
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】aLCO2氣體通過足量Na2O2后,所得氣體再與bLNO混合時,可得到cL氣體(氣體體積均在相同狀況下測定),下列表達式中,錯誤的是( )
A. 若a則c<![]() (a+b) B. 若a則c>
(a+b) B. 若a則c>![]() (a+b)
(a+b)
C. 若a>b則c=![]() (a+b) D. 若a=b則c=
(a+b) D. 若a=b則c=![]() (a+b)
(a+b)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列分子或離子中中心原子價層電子對幾何構型為四面體且分子或離子空間構型為V形的是( )
A. NH B. PH3 C. OF2 D. H3O+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Ⅰ、有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I﹣、NO3﹣、CO32﹣、SO42﹣、AlO2﹣,取該溶液進行以下實驗:
(1)取pH試紙檢驗,溶液呈酸性,可以排除______________的存在.
(2)取出部分溶液,加入少量CCl4及數滴新制氯水,經振蕩后CCl4呈紫紅色,可以排除_______存在.
(3)另取出部分溶液逐漸加入NaOH溶液,使溶液從酸性逐漸變為堿性,反應過程中均無沉淀產生,則又可排除____________的存在.
(4)取出部分上述堿性溶液加Na2CO3溶液后,有白色沉淀生成,證明有_______的存在,又可以排除__________的存在.
(5)根據上述實驗事實可以確定,該溶液中肯定存在的離子是____________,還不能確定是否存在的離子是_______________.
Ⅱ、某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定條件下可實現下圖所示的物質之間的變化:
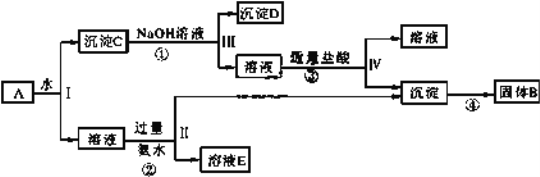
據此回答下列問題:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中對于溶液和沉淀的分離采取的方法是__________。
(2)根據上述框圖反應關系,寫出下列B、C、D 所含物質的化學式(提示:可為混合物)。
固體 B_________;沉淀 C__________;沉淀 D _________;
(3)寫出①、②反應離子方程式。
①___________________________________________;
②___________________________________________;
(4)步驟③較難操作,如何將實驗方案進行改進?________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com