
【題目】為了測定某草酸(H2C2O4)溶液的濃度,進行如下實驗:
取25.00mL某草酸溶液置于錐形瓶內,加入適量稀H2SO4后,用濃度為0.10molL-1的KMnO4溶液滴定到終點,所發生的反應為:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O試回答:
(1)實驗中,標準液KMnO4溶液應裝在________式滴定管中,因為_____________;
(2)實驗中眼睛注視_________________,直至滴定終點;判斷到達終點的現象是___________________________________________ ;
(3)若實驗所用KMnO4溶液體積為21.00mL,則草酸溶液的濃度為_______________;
(4)實驗中,下列操作(其它操作均正確),會對所測草酸濃度有什么影響?(填偏大、偏小、無影響)
A.滴定前仰視刻度,滴定后俯視刻度________________________;
B.錐形瓶在盛放待測液前未干燥,有少量蒸餾水______________________________;
C.滴定過程中搖動錐形瓶,不慎將瓶內的溶液濺出一部分______________________。
【答案】酸高錳酸鉀具有強氧化性錐形瓶內溶液顏色變化錐形瓶內溶液顏色恰好由無色變為紫紅色,且半分鐘內顏色不恢復0.21 molL-1偏小無影響偏小
【解析】
(1)KMnO4溶液具有強氧化性,可以腐蝕橡皮管,故KMnO4溶液應裝在酸式滴定管中;
(2)滴定時,左手控制滴定管活塞,右手搖動錐形瓶,眼睛注視溶液顏色的變化;KMnO4溶液呈紫色,草酸反應完畢,滴入最后一滴KMnO4溶液,錐形瓶內溶液顏色恰好由無色變為紫紅色,且半分鐘內顏色不恢復;
(3)2KMnO4~~~~~~5H2C2O4
2 5
0.10×21.00×10-3mol 0.025×cmol
![]() ,解得:c=0.21 molL-1;
,解得:c=0.21 molL-1;
(4)A、滴定前仰視,讀數偏大,滴定后俯視,讀數偏小,所得差值偏小,所以測定結果偏小;B.錐形瓶在盛放待測液前未干燥,有少量蒸餾水,對測定結果無影響;C.滴定過程中搖動錐形瓶,不慎將瓶內的溶液濺出一部分,則待測液的體積減少,消耗標準液的體積減少,測定結果偏小。


科目:高中化學 來源: 題型:
【題目】在下列各說法中,正確的是
A. 對于2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反應中充入1mol SO2和足量的氧氣反應時,放出的熱量一定是Q/2 kJ
2SO3(g) ΔH=-Q kJ·mol-1,(Q>0),若反應中充入1mol SO2和足量的氧氣反應時,放出的熱量一定是Q/2 kJ
B. 熱化學方程式中的化學計量數不能用分數表示
C. Zn(s)+H2SO4(aq) ===ZnSO4(aq)+H2(g) ΔH<0,該反應的化學能可以轉化為電能
D. ΔH的大小與熱化學方程式的化學計量數無關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下向10mLpH=3的醋酸溶液中加入水稀釋后,下列說法正確的是( )
A. 溶液中導電粒子的數目增加,導電性增強
B. 醋酸的電離程度增大,pH增大
C. 再加入10mLpH=11NaOH溶液,混合液pH>7
D. 溶液中c(CH3COO—)/c(CH3COOH)c(OH—)變小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】發展煤化工是推動山西能源革命的重要力量,煤的干餾是煤化工的一種重要途徑。
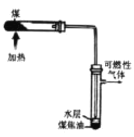
(1)煤的干餾屬于_____________變化(填“物理”或“化學”)。
(2)煤干餾后得到的固體物質主要是___________,得到的可燃性氣體中的一種成分是___________。
(3)煤焦油中含有苯, 用苯制硝基苯的化學方程式是_________,該反應類型屬于_________。
(4)煤焦油經過分餾可以得到萘(![]() ),其分子式是_____________.
),其分子式是_____________.
(5) 為證明上圖實驗中得到的水層含有氨,可進行的實驗操作是_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】足量鋅與濃H2SO4充分在加熱下反應生成會SO2和H2的混合氣體;鋅和稀硫酸反應只有H2生成。現有甲乙兩研究小組分別實驗探究:
甲研究小組按下圖實驗驗證鋅與濃硫酸反應生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL 18.5mol·L-1的濃硫酸,經過一段時間反應,Zn完全溶解
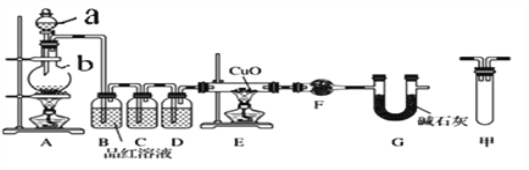
(1)填寫儀器名稱:a_______________。
(2)寫出裝置A中生成能使品紅溶液褪色的化學反應方程式:_________________。
(3)裝置D中加入的試劑是__________。
(4)U型管G的作用為______________。
(5)有同學認為A、B間應增加圖中的甲裝置,該裝置的作用為__________。
(6)證明反應生成SO2和H2的實驗現象是_________________。
(7)若A中生成標準狀況下的氣體33.6L,將A反應后的溶液稀釋到1L,測得溶液中H+的濃度為0.1 mol·L-1,則稀釋液中SO42-的物質的量濃度是_________ mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中充入1 molH2和1molI2,壓強為p(Pa),并在一定溫度下使其發生反應H2(g)+I2(g) ![]() 2HI(g),下列說法正確的是
2HI(g),下列說法正確的是
A. 保持容器容積不變,向其中加入1molH2,化學反應速率不變
B. 保持容器容積不變,向其中加入1molAr,化學反應速率增大
C. 保持容器內氣體壓強不變,向其中加入1molAr,化學反應速率不變
D. 保持容器內氣體壓強不變,向其中加入1molH2(g)和1molI2(g),化學反應速率不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關熱化學方程式的敘述中,正確的是( )
A. 含20.0gNaOH的稀溶液與足量的稀硫酸完全中和,放出28.7kJ的熱量,則表示中和熱的熱化學方程式為2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) △H=-114.8kJ·mol-1
B. 已知熱化學方程式:SO2(g)+![]() O2(g)
O2(g)![]() SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為196.64kJ
SO3(g) △H=-98.32kJ·mol-1,在容器中充入2molSO2和1molO2充分反應,最終放出的熱量為196.64kJ
C. 已知2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,則H2的燃燒熱為241.8kJ·mol-1
D. 已知石墨轉化為金剛石為吸熱,那么石墨比金剛石穩定
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com