
【題目】研究CO2在海洋中的轉移和歸宿,是當今海洋科學研究的前沿領域。
(1)溶于海水的CO2主要以4種無機碳形式存在,其中HCO3-占95%,寫出CO2溶于水產生HCO3-的方程式:_____________。
(2)在海洋循環中,通過如圖所示的途徑固碳。

①寫出鈣化作用的離子方程式:_____________。
②同位素示蹤法證實光合作用釋放出的O2只來自于H2O,用18O標記物質的光合作用的化學方程式如下,將其補充完整:_____________+_____________=(CH2O)x+x18O2+xH2O,_____________
(3)海水中溶解無機碳占海水總碳的95%以上,其準確測量是研究海洋碳循環的基礎,測量溶解無機碳,可采用如下方法:
①氣提、吸收CO2,用N2從酸化后的海水中吹出CO2并用堿液吸收(裝置示意圖如圖所示),將虛線框中的裝置補充完整并標出所用試劑。_____________

②滴定。將吸收液洗后的無機碳轉化為NaHCO3,再用xmol/LHCl溶液滴定,消耗ymLHCl溶液,海水中溶解無機碳的濃度=_____________mol/L。
【答案】CO2+H2O![]() H2CO3,H2CO3
H2CO3,H2CO3![]() HCO3-+H+ Ca2++2HCO3-=CaCO3↓+CO2↑+H2O xCO2 2xH218O
HCO3-+H+ Ca2++2HCO3-=CaCO3↓+CO2↑+H2O xCO2 2xH218O 
![]()
【解析】
(1)CO2溶于水生成碳酸,碳酸是弱電解質,在水中部分發生電離;
(2)①由圖可知,鈣化作用過程是碳酸氫根離子轉化生成碳酸鈣,據此書寫離子方程式;
②光合作用是CO2與水在太陽光作用下,在葉綠體中反應生成有機物、放出氧氣的過程,氧氣來源于水中的氧;
(3)①需從酸化后的海水中吹出二氧化碳,那么就需要滴加稀酸酸化,且裝置應從長管進氮氣,從短導管吹出二氧化碳;
②依據原理NaHCO3+HCl=NaCl+CO2↑+H2O 。
(1)溶于海水的CO2與水結合生成碳酸,碳酸電離生成碳酸氫根離子HCO3-,故CO2溶于水產生HCO3-的方程式:CO2+H2O![]() H2CO3,H2CO3
H2CO3,H2CO3![]() HCO3-+H+ ;
HCO3-+H+ ;
(2)①反應物中含有碳酸氫根離子,生成物為碳酸鈣,依據元素守恒、電荷守恒得出離子方程式為:Ca2++2HCO3-=CaCO3↓+CO2↑+H2O;
②光合作用產生的氧氣來源于水,即水中的氧原子采用示蹤法標記為18O,依據元素守恒配平方程式, xCO2+2xH218O=(CH2O)x+x18O2+xH2O ;
(3)①酸化海水,可以使用試劑:稀硫酸、利用分液漏斗滴加,長管進氣,短管出氣,故裝置為 ;
;
②滴定過程中發生的反應為NaHCO3+HCl=NaCl+CO2↑+H2O,故n(NaHCO3)=n(HCl)=xmol/L×y×10-3L,根據C守恒,海水中溶解無機碳的濃度=![]() =
=![]() mol
mol![]() L-1。
L-1。


科目:高中化學 來源: 題型:
【題目】W、X、Y、Z為短周期原子序數依次增大的主族元素,其原子序數之和為30,W與X、Y、Z都能形成共價化合物,Y、W形成的常見化合物溶于水顯堿性,Z、W形成的化合物溶于水顯酸性,四種元素形成的某種化合物的結構式為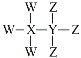 。下列說法錯誤的是
。下列說法錯誤的是
A.X為硼元素或碳元素
B.Y不屬于第ⅣA族元素
C.W與Y、Z分別形成的常見化合物能反應生成鹽
D.最高價氧化物對應的水化物的酸性:Z>Y
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】茶葉中含有多種有益于人體健康的有機成分及鈣、鐵等微量金屬元素,某化學研究性學習小組設計方案用以檢驗某品牌茶葉中鐵元素的存在并測定鈣元素的質量分數(已知CaC2O4為白色沉淀物質)。首先取200g茶葉樣品進行如圖操作:
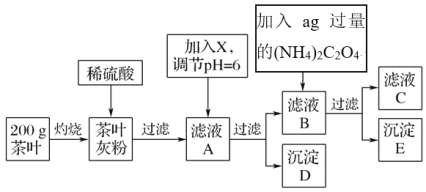
已知:①文獻資料顯示:某些金屬離子的氫氧化物完全沉淀時的pH為:Ca(OH)2:13,Fe(OH)3:4.1
②(NH4)2C2O4溶液顯酸性。
(1)實驗前要先將茶葉樣品高溫灼燒為灰粉,需要用到的實驗儀器有酒精燈、三腳架、玻璃棒、泥三角________,其主要目的是___________________。
A.蒸發皿 B.坩堝C.石棉網
(2)從濾液A→沉淀D的過程中需要加入的物質X可以選擇________。
A.CaO B.Ca(OH)2C.NH3·H2O
(3)用酸性KMnO4標準溶液滴定濾液C時發生的反應為:5C2O42-+2MnO4-+16H+===10CO2↑+2Mn2++8H2O。將濾液C稀釋至250mL,取25.00mL溶液,用硫酸酸化后,用0.10mol·L-1的KMnO4標準溶液滴定,終點時消耗KMnO4溶液體積如表所示:
編號 | KMnO4溶液體積/mL |
1 | 19.98 |
2 | 22.00 |
3 | 20.02 |
①此步操作過程中需要用到圖示中哪些儀器________
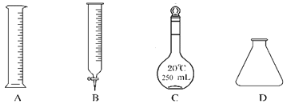
②滴定達到終點時的現象是__________________________。
③為保證實驗精確度,沉淀D及E需要分別洗滌,并將洗滌液轉移回母液中,若不洗滌沉淀D,會使測定的鈣元素的含量________(偏低、偏高、無影響,下同),若不洗滌沉淀E,會使測定的鈣元素的含量________。
④原茶葉中鈣元素的質量分數為________。(用含a的代數式表示,已知(NH4)2C2O4的摩爾質量為124g·mol-1)。
(4)可以通過檢驗濾液A來驗證該品牌茶葉中是否含有鐵元素,所加試劑及實驗現象是_______________、________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
鉀和碘的相關化合物在化工、醫藥、材料等領域有著廣泛的應用。回答下列問題:
(1)元素K的焰色反應呈紫紅色,其中紫色對應的輻射波長為_______nm(填標號)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基態K原子中,核外電子占據的最高能層的符號是_________,占據該能層電子的電子云輪廓圖形狀為___________。K和Cr屬于同一周期,且核外最外層電子構型相同,但金屬K的熔點、沸點等都比金屬Cr低,原因是___________________________。
(3)X射線衍射測定等發現,I3AsF6中存在I3+離子。I3+離子的幾何構型為_____________,中心原子的雜化形式為________________。
(4)KIO3晶體是一種性能良好的非線性光學材料,具有鈣鈦礦型的立體結構,邊長為a=0.446nm,晶胞中K、I、O分別處于頂角、體心、面心位置,如圖所示。K與O間的最短距離為______nm,與K緊鄰的O個數為__________。
(5)在KIO3晶胞結構的另一種表示中,I處于各頂角位置,則K處于______位置,O處于______位置。
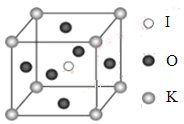
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組在驗證反應“Fe+2Ag+=Fe2++2Ag”的實驗中檢測到Fe3+,發現和探究過程如下。
向硝酸酸化的0.05 mol·L-1硝酸銀溶液(pH≈2)中加入過量鐵粉,攪拌后靜置,燒杯底部有黑色固體,溶液呈黃色。
(1)檢驗產物
①取少量黑色固體,洗滌后,_______(填操作和現象),證明黑色固體中含有Ag。
②取上層清液,滴加K3[Fe(CN)6]溶液,產生藍色沉淀,說明溶液中含有_______________。
(2)針對“溶液呈黃色”,甲認為溶液中有Fe3+,乙認為鐵粉過量時不可能有Fe3+,乙依據的原理是___________________(用離子方程式表示)。針對兩種觀點繼續實驗:
①取上層清液,滴加KSCN溶液,溶液變紅,證實了甲的猜測。同時發現有白色沉淀產生,且溶液顏色變淺、沉淀量多少與取樣時間有關,對比實驗記錄如下:
序號 | 取樣時間/min | 現象 |
ⅰ | 3 | 產生大量白色沉淀;溶液呈紅色 |
ⅱ | 30 | 產生白色沉淀;較3 min時量少;溶液紅色較3 min時加深 |
ⅲ | 120 | 產生白色沉淀;較30 min時量少;溶液紅色較30 min時變淺 |
(資料:Ag+與SCN-生成白色沉淀AgSCN)
② 對Fe3+產生的原因作出如下假設:
假設a:可能是鐵粉表面有氧化層,能產生Fe3+;
假設b:空氣中存在O2,由于________(用離子方程式表示),可產生Fe3+;
假設c:酸性溶液中NO3-具有氧化性,可產生Fe3+;
假設d:根據_______現象,判斷溶液中存在Ag+,可產生Fe3+。
③ 下列實驗Ⅰ可證實假設a、b、c不是產生Fe3+的主要原因。實驗Ⅱ可證實假設d成立。
實驗Ⅰ:向硝酸酸化的________溶液(pH≈2)中加入過量鐵粉,攪拌后靜置,不同時間取上層清液滴加KSCN溶液,3 min時溶液呈淺紅色,30 min后溶液幾乎無色。
實驗Ⅱ:裝置如圖。其中甲溶液是________,操作及現象是________________。
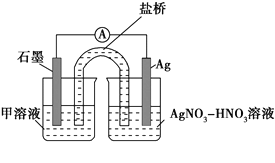
(3)根據實驗現象,結合方程式推測實驗ⅰ~ⅲ中Fe3+濃度變化的原因:______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化亞銅(CuCl)廣泛應用于化工、印染、電鍍等行業。CuCl難溶于醇和水,可溶于氯離子濃度較大的體系,在潮濕空氣中易水解氧化。以海綿銅(主要成分是Cu和少量CuO)為原料,采用硝酸銨氧化分解技術生產CuCl的工藝過程如下:
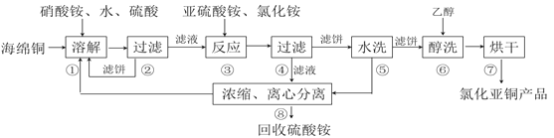
回答下列問題:
(1)步驟①中得到的氧化產物是_________,溶解溫度應控制在60~70度,原因是__________。
(2)寫出步驟③中主要反應的離子方程式___________。
(3)步驟⑤包括用pH=2的酸洗、水洗兩步操作,酸洗采用的酸是_________(寫名稱)。
(4)上述工藝中,步驟⑥不能省略,理由是______________________________。
(5)步驟②、④、⑤、⑧都要進行固液分離。工業上常用的固液分離設備有__________(填字母)
A.分餾塔 | B.離心機 | C.反應釜 | D.框式壓濾機 |
(6)準確稱取所制備的氯化亞銅樣品m g,將其置于若兩的FeCl3溶液中,待樣品完全溶解后,加入適量稀硫酸,用a mol/L的K2Cr2O7溶液滴定到終點,消耗K2Cr2O7溶液b mL,反應中Cr2O72-被還原為Cr3+,樣品中CuCl的質量分數為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有一瓶氣體為NH3,氣體的物質的量為0.2mol。
①氣體的質量為______,氣體中含氫原子的物質的量為____ mol。
②氣體中所含分子數為_____。
③氣體在標準狀況下的體積為______。
④將氣體甲完全溶解于水中形成500mL溶液,所得溶液溶質的物質的量濃度為______ molL-1。
⑤將④中所得溶液取出100mL,加水稀釋至1000ml,所得溶液溶質的物質的量濃度為 ______ molL-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化硫的催化氧化原理為![]() ,反應混合體系在平衡狀態時SO3的百分含量與溫度的關系如下圖所示。下列說法錯誤的是( )
,反應混合體系在平衡狀態時SO3的百分含量與溫度的關系如下圖所示。下列說法錯誤的是( )
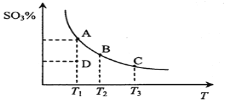
A.在D點時v正<v逆
B.反應2SO2(g)+O2(g) ![]() 2SO3(g) △H<0
2SO3(g) △H<0
C.若B、C點的平衡常數分別為KB、KC,則KB> KC
D.恒溫恒壓下向平衡體系中通入氦氣,平衡向左移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有A、B、C三種氣體,A是密度最小的氣體,B在通常情況下呈黃綠色,純凈的A可以在B中安靜地燃燒生成C。把氣體B通入到適量石灰乳中可以得到白色渾濁物D。請據此回答下列問題:
(1)寫出下列各反應的化學方程式
①純凈的A在B中安靜地燃燒生成C_______________
②將氣體B通入到水中:__________。
③將氣體B通入到NaOH溶液中:_______________________
④將氣體B通入到適量石灰乳中:_______________________
(2)把三種氣體分別通入酸性硝酸銀溶液中,出現白色沉淀的氣體是________(用字母表示)。
(3)將白色渾濁物D溶于水得到澄清溶液,分別取適量該澄清液兩份。
①向第一份中滴加碳酸鈉溶液觀察到出現沉淀,發生反應的化學方程式為______________、________。
②向第二份溶液中滴加硝酸酸化的硝酸銀溶液,會觀察到____________(填現象)。
③白色渾濁物D因具有漂白性又稱為______________,該物質在空氣中容易變質的原因為_______________(用化學方程式表示)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com