
在標準狀況下,將V L A氣體(摩爾質量為M g·mol-1)溶于0.1 L水中,所得溶液的密度為ρ g·cm-3,則此溶液的物質的量濃度(mol·L-1)為
A.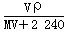 B.
B.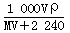
C.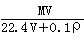 D.1 000VρM(MV+2 240)
D.1 000VρM(MV+2 240)
科目:高中化學 來源:2016-2017學年貴州省高一上期中化學卷(解析版) 題型:選擇題
下列反應一定屬于氧化還原反應的是( )
A.分解反應 B.復分解反應 C.化合反應 D.置換反應
查看答案和解析>>
科目:高中化學 來源:2017屆湖南省長株潭岳益五市十校高三12月聯考化學卷(解析版) 題型:選擇題
設NA為阿伏伽德羅常數的值。下列說法正確的是( )
A.0.1 mol?L— 1的MgCl2溶液中含Cl—的數目為0.2NA
1的MgCl2溶液中含Cl—的數目為0.2NA
B.100g質量分數為46%的乙醇水溶液中氧原子數為4 NA
C.標準狀況下,11.2 L CCl4中含C—Cl鍵的數目為2NA
D.20 ml 2mol? L—1 H2O2完全分解,轉移的電子數為0.08NA
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省培優聯盟高三冬季聯賽化學試卷(解析版) 題型:實驗題
實驗室里用下圖所示儀器和藥品制取純凈的無水氯化鐵。圖中A、B、C、D、E、F表示玻璃管接口,接口的彎曲和伸長部分未畫出,其中⑤、⑥所用為雙孔塞,
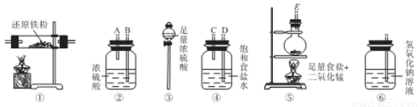
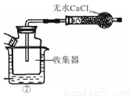
根據要求回答下列問題:
(1)如果規定氣體從左向右流動,上述各儀器裝置的正確連接順序是(填裝置的序號):
③→______→______→_______→_______→_______。
(2)裝置④的作用是_______________。
(3)實驗開始時,應首先______________;實驗結束時,應先熄滅裝置__________處的酒精燈。該實驗條件下生成的氯化鐵呈煙狀,且易水解,為便于收集,需要在__________和__________(填裝置序號)之間增加裝置⑦,該裝置中燒杯里的液體可以是___________。
(4)在裝置⑤的燒瓶中,發生反應的化學方程式為__________________。
(5)可用離子交換和滴定的方法測定FeCl3的純度:稱取0.68g的FeCl3樣品,溶解后先進行陽離子交換預處理,再通過含有飽和OH―的陰離子交換柱,使Cl―和OH―發生交換。交換完成后,流出溶液中的OH―用0.4000 mol/L的鹽酸滴定,滴至終點時消耗鹽酸30.00 mL。則該樣品中FeCl3的質量分數為___________%。
(6)設計一個簡單實驗,證明裝置①的硬質玻璃管中有少量的鐵未能與Cl2發生反應(寫出實驗操作及相關實驗現象)_________________。
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省培優聯盟高三冬季聯賽化學試卷(解析版) 題型:選擇題
化學科學與技術是改進生活、改善環境.促進發展的關鍵。下列說法正確的是 ( )
A.普通玻璃、氮化硅陶瓷、水晶飾物都是硅酸鹽制品
B.“乙醇汽油”的主要成分都是可再生能源
C.堿石灰、硫酸銅、硅膠都可用作食品干燥劑
D.“天宮”系列飛船使用的碳纖維材料、光導纖維都是新型無機非金屬材料
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省分校高一上期中化學卷(解析版) 題型:選擇題
R、X、Y和Z是四種元素,其常見化合價均為+2價,且X2+ 與單質R不反應;X2++Z  X+Z2+;Y+Z2+
X+Z2+;Y+Z2+  Y2++Z。這四種離子被還原成0價時表現的氧化性大小符合
Y2++Z。這四種離子被還原成0價時表現的氧化性大小符合
A.R2+>X2+>Z2+>Y2+ B.X2+>R2+>Y2+>Z2+
C.Y2+>Z2+>R2+>X2+ D.Z2+>X2+>R2+>Y2+
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省分校高一上期中化學卷(解析版) 題型:選擇題
下列說法正確的是(NA表示阿伏加德羅常數)
A.273℃、1個標準大氣壓下,NA個H2分子所占體積約為22.4L
B.2.3克金屬鈉變成離子時失去的電子數目為NA
C.1L、1 mol·L-1的氯化鐵溶液制成膠體,膠粒數目為NA
D.常溫常壓下,32克臭氧所含的氧原子數目為2NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省分校高二上期中化學卷(解析版) 題型:選擇題
下列化合物分別與鐵粉及液溴的混合物反應,苯環上的氫原子被取代生成的一溴代物只
有一種同分異構體的是( )
A. 乙苯 B. 1,3,5-三甲基苯
C. 1,2,4-三甲基苯 D. 1,2,3-三甲基苯
查看答案和解析>>
科目:高中化學 來源:2017四川省自貢市高三第一次診斷考試化學試卷(解析版) 題型:推斷題
已知由短周期常見元素形成的純凈物A、B、C、D轉化關系如圖1瑣事,物質A與物質B之間的反應不再溶液中進行。

若A為金屬單質,C是淡黃色固體,D是一元強堿。
①物質B是__________(填化學式)。
②化合物C的電子式為_________;化合物D中所含化學鍵的類型是_________。
③在常溫下,向PH=a的醋酸溶液中加入等體積pH=b的D溶液,且a+b=14,則充分反應后,所得溶液中各種離子的濃度由大到小的順序是:__________.
(2)若A為非金屬單質,C是有色氣體,D是一元強酸.
①B為__________(填化學式)。
②化合物C與H2O反應化學方程式___________,氧化劑與還原劑的量比為_________。
(3)某同學用圖2裝置完成有關探究實驗。
Ⅰ試管中發生反應的離子方程式為__________。
Ⅱ試管中觀察到__________的實驗現象時,說明NO2能溶于濃硫酸中,濃硫酸不能干燥NO2。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com