
下列實驗方法正確的是
| A.除去NaCl溶液中的Cl2,可加入酒精后分液 |
| B.滴定管用蒸餾水洗凈后,直接裝入標準濃度的溶液滴定 |
| C.用排水法收集稀HNO3和Cu反應產生的NO氣體 |
| D.用KSCN溶液和氯水鑒別FeCl3溶液中是否含有FeCl2 |
科目:高中化學 來源: 題型:單選題
已知:Ki1(H2CO3)> Ki1(H2S)。現有以下試劑:鹽酸、醋酸、苯酚、碳酸鈣、醋酸鈉溶液、硫化鈉溶液,用下圖所示裝置進行下列實驗,無法達到實驗目的的是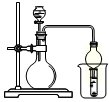
| A.比較醋酸、苯酚、碳酸的酸性 |
| B.比較鹽酸、醋酸、碳酸的酸性 |
| C.比較醋酸、氫硫酸、碳酸的酸性 |
| D.比較鹽酸、碳酸、氫硫酸的酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
2012年冬天,我國城市空氣污染狀況受到人們的強烈關注。在空氣質量報告中,SO2的指數是衡量空氣質量好壞的重要指標。為了測定空氣中的SO2含量,有三位同學分別采用了以下三種測定方法。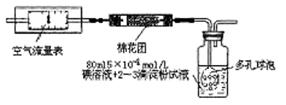
I.氧化還原法:甲同學根據化學反應原理SO2+I2+2H2O=H2SO4+2HI設計了如下圖所示的裝置進行實驗:
(1)該實驗需80ml濃度為5×10-4mol/L的碘
溶液,甲同學應選擇 ml的容量瓶進行配制。
(2)廣口瓶中使用多孔球泡的目的是 。
(3)在甲同學所配碘溶液濃度準確,并且量取藥品及 實驗過程中各種讀數均無錯誤的情況下,利用上述裝置所測定的SO2含量仍然比實際含量低,請分析其中可能的原因(至少寫兩種原因)
II.重量法:乙同學擬用實驗室常用儀器組成簡易裝置測定空氣中的SO2含量。實驗操作過下:
按如下實驗裝置圖安裝好儀器,在廣口瓶中盛放足量的H2O2水溶液,用規格為20ml的針筒抽氣100次,使空氣中的SO2被H2O2水溶液充分吸收(SO2+H2O2=H2SO4)。在吸收后的水溶液中加入足量的BaCl2溶液,生成白色沉淀(H2SO4+BaCl2=BaSO4↓+2HCl),經過濾、洗滌、干燥等步驟后進行稱量,得白色固體0.18mg。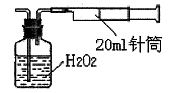
(4)取樣處空氣中SO2含量為 mg/L(精確到0.001)。
(5)現查閱資料知,常溫下BaSO3的Ksp為5.48×10-7,飽和亞硫酸溶液中c(SO32-)=6.3×10-8mol/L。有同學認為以上實驗不必用H2O2吸收SO2,直接用0.lmol/L BaCl2溶液來吸收SO2即可產生沉淀,你認為這樣做 (填“正確”或“不正確”),請利用以上數據簡述理由 。
III.儀器法:丙同學直接使用一種SO2濃度智能監測儀測定空氣中的SO2含量,這種監測儀是利用電化學原理,根據電池產生電流的強度來準確測量SO2濃度的。該電池總的化學反應原理為:2SO2+O2+2H2O=2H2SO4。
(6)請寫出該電池負極的電極反應式: 。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列實驗方法和解釋或結論都正確的是
| | 實驗目的 | 實驗方法 | 解釋或結論 |
| A | 檢驗CH2=CH-CHO中含碳碳雙鍵 | 將丙烯醛溶液滴入溴水中,溴水褪色 | 丙烯醛中碳碳雙鍵與溴單質發生了加成反應 |
| B | 確認某無機酸濃溶液的溶質 | 用蘸有濃氨水的玻璃棒放于試劑瓶口,有大量白煙 | 該無機酸一定為鹽酸 |
| C | 鑒別一份紅棕色氣體成分 | 濕潤的淀粉碘化鉀試紙插入氣體中,試紙變藍 | 該氣體一定為Br2 |
| D | 探究高級脂肪酸甘油酯水解的條件 | 高級脂肪酸甘油酯中加入NaOH溶液加熱后不再分層 | 高級脂肪酸甘油酯發生皂化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列實驗裝置是探究銅絲與過量濃硫酸的反應,下列敘述正確的是 ( )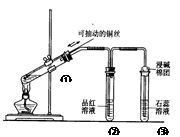
| A.上下移動①中銅絲可控制SO2的量 |
| B.②中品紅溶液不褪色 |
| C.③中石蕊溶液變藍色 |
| D.為確認CuSO4生成,向①中加水,觀察溶液顏色 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列化學實驗或操作能夠達到目的的是
| A.為鑒別KCl、AlCl3和MgCl2溶液,分別向三種溶液中滴加NaOH溶液至過量 |
| B.欲除去蛋白質溶液中的NaCl而又不改變其性質,可加入適量BaCl2溶液后過濾 |
| C.測氯水的pH,可用玻璃棒蘸取氯水點在pH試紙上,待其變色后和標準比色卡比較 |
| D.為了證明焦爐氣中含有氫氣,可將焦爐氣通過灼熱的氧化銅粉末,看黑色粉末是否變紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
過氧化鎂(MgO2)易溶于稀酸,溶于酸后產生過氧化氫,在醫學上可作為解酸劑等。過氧化鎂產品中常會混有少量MgO,實驗室可通過多種方案測定樣品中過氧化鎂的含量。 
(1)某研究小組擬用右圖裝置測定一定質量的樣品中過氧化鎂的含量。
①實驗前需進行的操作是 .稀鹽酸中加入少量FeCl3溶液的作用是 。
②用恒壓分液漏斗的優點有:使分液漏斗中的溶液順利滴下; 。
③實驗終了時,待恢復至室溫,先 ,再平視刻度線讀數。
(2)實驗室還可通過下列兩種方案測定樣品中過氧化鎂的含量:
方案I:取a g樣品,加入足量稀鹽酸,充分反應后再加入 NaOH溶液至Mg2+沉淀完全,過濾、洗滌后,將濾渣充分灼燒,最終得到b g固體。
方案Ⅱ:稱取0.1 g樣品置于碘量瓶中,加入15 mL0.6 mol/LKI溶液和足量鹽酸,搖勻后在暗處靜置5 min,然后用0.1 mol/L Na2S2O3溶液滴定,滴定到終點時共消耗VmL Na2S2O3溶液。(已知:I2+2Na2S2O3= Na2S4O6+2NaI)
①已知常溫下Ksp[Mg(OH)2]=l×10-11。為使方案I中Mg2+完全沉淀[即溶液中c(Mg2+)≤l ×10-5mol/L],溶液的pH至少應調至 。方案I中過氧化鎂的質量分數為 (用含a、b的表達式表示)。
②方案Ⅱ中滴定前需加入少量 作指示劑;樣品中過氧化鎂的質量分數為 (用含V的表達式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
菠菜營養豐富,長期以來民間流傳著“菠菜不能與豆腐同食”的說法。某學校化學興趣小組的同學擬通過實驗探究:菠菜是否含有草酸類物質?草酸又有哪些性質?通過上網查詢,獲得以下資料:草酸又名乙二酸,其酸性比乙酸稍強,草酸及其鹽具有較強的還原性,草酸晶體(H2C2O4·2H2O)的熔點為100.1℃,在175℃時受熱分解,草酸鈣是難溶于水的白色固體。
他們設計的實驗步驟如下:
1.將菠菜在少量開水中煮沸2~3 min,冷卻后濾去菠菜,得濾液(含有少量 雜質)。向濾液中加入足量Ca(OH)2溶液,然后再加入足量CH3COOH溶液,觀察現象。
雜質)。向濾液中加入足量Ca(OH)2溶液,然后再加入足量CH3COOH溶液,觀察現象。
2.用草酸晶體(H2C2O4·2H2O)做以下實驗:
請回答以下問題:
(1)步驟1中加入CH3COOH溶液的作用: 。
(2)A處應選擇 (填“Ⅰ”或“Ⅱ”),在做實驗之前,應先 。
(3)實驗2過程中觀察到C、E裝置中的溶液均變渾濁,且D裝置中黑色粉末變為紅色,寫出A中草酸晶體(H2C2O4·2H2O)發生反應的化學方程式: ,裝置B的作用是 。
(4)為使實驗結論更加嚴密和安全,在以上所連接的裝置C、D間還需依次添加裝有 、 、 (液體試劑)的洗氣瓶,此外指出上述裝置中的不足之處還有 。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列關于各實驗裝置圖的敘述中正確的是( )

| A.裝置①:構成鋅—銅原電池 |
| B.裝置②:除去Cl2中含有的少量HCl |
| C.裝置③:驗證溴乙烷發生消去反應生成烯烴 |
| D.裝置④:由實驗現象推知酸性強弱順序為CH3COOH>H2CO3>C6H5OH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com