(2008?廣東)銅在自然界存在于多種礦石中,如:
| 礦石名稱 |
黃銅礦 |
斑銅礦 |
輝銅礦 |
孔雀石 |
| 主要成分 |
CuFeS2 |
Cu5FeS4 |
Cu2S |
CuCO3?Cu(OH)2 |
①上表所列銅化合物中,銅的質量百分含量最高的是
Cu2S
Cu2S
.
②工業上以黃銅礦為原料.采用火法溶煉工藝生產銅.該工藝的中間過程會發生反應:2Cu
2O+Cu
2S
6Cu+SO
2↑,反應的氧化劑是
Cu2O,Cu2S
Cu2O,Cu2S
.
③SO
2尾氣直接排放到大氣中造成環境污染的后果是
二氧化硫是有毒氣體,二氧化硫溶于水后形成酸性溶液,隨雨水降下,就可能形成酸雨
二氧化硫是有毒氣體,二氧化硫溶于水后形成酸性溶液,隨雨水降下,就可能形成酸雨
;處理該尾氣可得到有價值的化學品,寫出其中1種酸和1種鹽的名稱
硫酸,硫酸銨.
硫酸,硫酸銨.
.
④黃銅礦熔煉后得到的粗銅含少量Fe、Ag、Au等金屬雜質,需進一步采用電解法精制.請簡述粗銅電解得到精銅的原理:
粗銅電解得到精銅的原理:電解池中,粗銅作陽極,精銅作陰極,電解質為硫酸銅溶液.陽極上發生氧化反應,Cu失去電子,使Cu單質變為Cu 2+進入溶液中Cu-e-═Cu 2+;陰極上發生還原反應,Cu 2+得到電子在陰極上析出Cu單質,Cu 2++e-═Cu,從而達到精制Cu的目的.
粗銅電解得到精銅的原理:電解池中,粗銅作陽極,精銅作陰極,電解質為硫酸銅溶液.陽極上發生氧化反應,Cu失去電子,使Cu單質變為Cu 2+進入溶液中Cu-e-═Cu 2+;陰極上發生還原反應,Cu 2+得到電子在陰極上析出Cu單質,Cu 2++e-═Cu,從而達到精制Cu的目的.
.
⑤下表中,對陳述Ⅰ、Ⅱ的正確性及其有無因果關系的判斷都正確的是
AD
AD
(填字母).
| 選項 |
陳述Ⅰ |
陳述Ⅱ |
判斷 |
| A |
銅綠的主成分是堿酸銅 |
可用稀鹽酸除銅器表面的銅綠 |
Ⅰ對;Ⅱ對;有 |
| B |
銅表易形成致密的氧化膜 |
銅容器可以盛放濃硫酸 |
Ⅰ對;Ⅱ對;有 |
| C |
鐵比銅活潑 |
例在銅板上的鐵釘在潮濕空氣中不易生銹 |
Ⅰ對;Ⅱ對;有 |
| D |
藍色硫酸銅晶體受熱轉化為白色硫酸銅粉末是物理變化 |
硫酸銅溶液可用作游泳池的消毒劑 |
Ⅰ錯;Ⅱ對;無 |



 時刻準備著暑假作業原子能出版社系列答案
時刻準備著暑假作業原子能出版社系列答案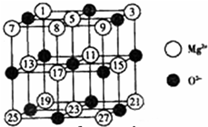 (2008?廣東)鎂、銅等金屬離子是人體內多種酶的輔因子.工業上從海水中提取鎂時,先制備無水氯化鎂,然后將其熔融電解,得到金屬鎂.
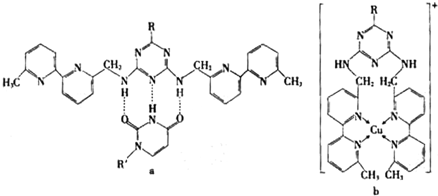
(2008?廣東)鎂、銅等金屬離子是人體內多種酶的輔因子.工業上從海水中提取鎂時,先制備無水氯化鎂,然后將其熔融電解,得到金屬鎂.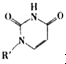 或Cu(I)(I表示化合價為+1)時,分別形成a和b:
或Cu(I)(I表示化合價為+1)時,分別形成a和b: