
| A.6.72 L | B.11.2 L | C.22.4 L | D.4.48 L |
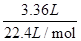 =0.15mol,根據電子轉移守恒可知n(Al)=
=0.15mol,根據電子轉移守恒可知n(Al)=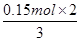 =0.1mol,故金屬鋁的質量為0.1mol×27g/mol=2.7g,金屬鋁提供電子的量是0.3mol。由題意可知,向反應后的溶液中加入過量NaOH溶液后,鋁離子全部轉化為偏鋁酸根離子,不會出現沉淀,反應后產生19.4g氫氧化鎂、氫氧化鐵沉淀的,沉淀中氫氧根的質量為19.4g-(11.9g-2.7g)=10.2g,物質的量n(OH-)=
=0.1mol,故金屬鋁的質量為0.1mol×27g/mol=2.7g,金屬鋁提供電子的量是0.3mol。由題意可知,向反應后的溶液中加入過量NaOH溶液后,鋁離子全部轉化為偏鋁酸根離子,不會出現沉淀,反應后產生19.4g氫氧化鎂、氫氧化鐵沉淀的,沉淀中氫氧根的質量為19.4g-(11.9g-2.7g)=10.2g,物質的量n(OH-)=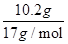 =0.6mol。反應中金屬鐵、銅提供的電子的物質的量等于生成堿的氫氧根離子的物質的量即0.6mol。將合金溶于過量稀硝酸中,分別生成Al3+、Fe3+、Cu2+離子,根據電子守恒,金屬共提供電子的物質的量為0.6+0.3=0.9mol,令NO的物質的量為xmol,根據電子轉移守恒有(5-2)×xmol=0.9mol,解得x=0.3,所以生成的NO的體積為0.3mol×22.4L/mol=6.72L,故A正確。
=0.6mol。反應中金屬鐵、銅提供的電子的物質的量等于生成堿的氫氧根離子的物質的量即0.6mol。將合金溶于過量稀硝酸中,分別生成Al3+、Fe3+、Cu2+離子,根據電子守恒,金屬共提供電子的物質的量為0.6+0.3=0.9mol,令NO的物質的量為xmol,根據電子轉移守恒有(5-2)×xmol=0.9mol,解得x=0.3,所以生成的NO的體積為0.3mol×22.4L/mol=6.72L,故A正確。

 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:不詳 題型:填空題
 Fe(OH)3+5OH-]
Fe(OH)3+5OH-]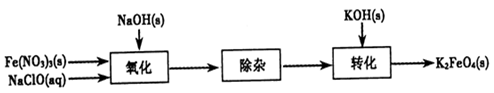
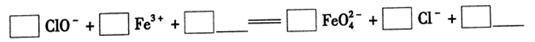
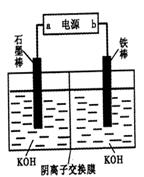
 4Fe(OH)3+8OH-+3O2。實驗測得K2FeO4溶液濃度與溫度和pH的關系分別如下圖所示:
4Fe(OH)3+8OH-+3O2。實驗測得K2FeO4溶液濃度與溫度和pH的關系分別如下圖所示: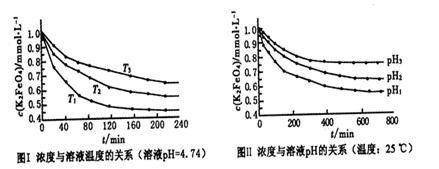
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 Fe3O4+S4O62-+2H2O,有關說法正確的是
Fe3O4+S4O62-+2H2O,有關說法正確的是| A.每轉移1.5mol電子,有1.125mol Fe2+被氧化 |
| B.x = 2 |
| C.Fe2+、S2O32-都是還原劑 |
| D.每生成1mol Fe3O4,轉移電子2mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2H2↑+O2↑,下列有關判斷正確的是
2H2↑+O2↑,下列有關判斷正確的是| A.氧化劑是氫元素 |
| B.還原產物是O2 |
| C.H2O既有氧化性也有還原性 |
| D.2molH2O反應,轉移了8mol電子 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.生成1 mol N2,電子轉移總數為3NA | B.生成1 mol N2,電子轉移總數為5NA |
| C.溶解1 mol Zn,電子轉移總數為2NA | D.溶解1 mol Zn,電子轉移總數為4NA |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CO(NH2)2 (l) + H2O (l)。
CO(NH2)2 (l) + H2O (l)。 ,右圖是氨碳比(x)與CO2平衡轉化率(α)的關系。α隨著x增大而增大的原因是___________。
,右圖是氨碳比(x)與CO2平衡轉化率(α)的關系。α隨著x增大而增大的原因是___________。
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.氯酸鉀是還原劑 |
| B.反應中消耗3molP時,轉移電子的物質的量為15mol |
| C.KCl既是氧化產物,又是還原產物 |
| D.發令時產生的白煙只是KC1固體顆粒 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.4 mo1 | B.5 mo1 | C.6 mo1 | D.7 mo1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com