
分析 燃燒反應為放熱反應,△H<0,根據4.4g丙烷完全燃燒放出的熱量計算44g即1mol丙烷完全燃燒放出的熱量,進而書寫熱化學方程式;
(1)根據蓋斯定律來判斷兩種途徑放熱之間的關系;
(2)該反應屬于吸熱反應,反應物具有的總能量小于生成物的總能量;需要吸收能量,所以反應條件為加熱;
(3)途徑I:①C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=-a kJ•mol-1
途徑II:②C3H8(g)═C3H6(g)+H2(g)△H=+b kJ•mol-1
③2C3H6(g)+9O2(g)═6CO2(g)+6H2O(l)△H=-c kJ•mol-1
④2H2(g)+O2 (g)═2H2O(l)△H=-d kJ•mol-1 反應①=反應②+反應③×$\frac{1}{2}$+反應④×$\frac{1}{2}$,據蓋斯定律來判斷各步反應之間的關系.
解答 解:4.4g丙烷完全燃燒放出akJ能量,則1mol丙烷完全燃燒生成CO2氣體和液態水放出的熱量為10akJ,
則丙烷燃燒的熱化學方程式為C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-10akJ/mol,
故答案為:C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-10akJ/mol;
(1)根據蓋斯定律,煤作為燃料不管是一步完成還是分兩步完成,反應物和產物的焓值是一定的,所以兩途徑的焓變值一樣,放出的熱量一樣,
故答案為:等于;
(2)由于C3H8(g)═C3H6(g)+H2(g) 的反應中△H>0,該反應是吸熱反應,反應物具有的總能量小于生成物的總能量,需要吸收能量,反應條件是加熱,
故答案為:小于;吸收;加熱;
(3)所以-a=b+$\frac{1}{2}$(-c-d),所以b=-a+$\frac{1}{2}$(c+d),2b=c+d-2a,
故答案為:2b=c+d-2a.
點評 本題考查學生蓋斯定律的應用以及反應吸放熱與反應物、生成物能量之間的關系,可以根據所學知識進行回答,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ①④⑤ | C. | ③④⑤ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
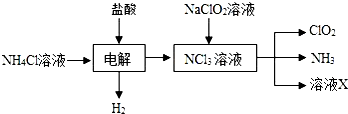

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 選項 | 不純物質(雜質) | 除雜試劑或分離方法 | 必用儀器 |
| A | 碘水 | 四氯化碳 萃取 | 分液漏斗 |
| B | 一氧化碳(二氧化碳) | 澄清石灰水 洗氣 | 洗氣瓶 |
| C | 硝酸鉀(氯化鈉) | 直接蒸發結晶 | 蒸發皿 |
| D | 乙醇(水) | 生石灰 蒸餾 | 蒸餾燒瓶 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電離平衡逆向移動 | B. | c(OH-)增大 | ||
| C. | 電離平衡常數增大 | D. | n(OH-)增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 反應時間/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反應在t1 min內的平均速率為v(H2)=0.40/t1 mol•L-1•min-1 | |
| B. | 保持其他條件不變,起始時向容器中充入0.60 mol CO和1.20 mol H2O,達到平衡時n(CO2)=0.40 mol | |
| C. | 保持其他條件不變,向平衡體系中再通入0.20 mol H2O,與原平衡相比,達到新平衡時CO轉化率增大,H2O的體積分數減小 | |
| D. | 溫度升至800℃,上述反應平衡常數為0.64,則正反應為吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某研究小組向2L密閉容器中加入一定量的固體A和氣體B發生反應:
某研究小組向2L密閉容器中加入一定量的固體A和氣體B發生反應:時間(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 每生成16 mol N2轉移30 mol電子 | |
| B. | NaN3中N元素被還原 | |
| C. | N2既是氧化劑又是還原劑 | |
| D. | 還原產物與氧化產物質量之比為1:15 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com