
【題目】短周期原子序數依次遞增的A、B、C、D、E、F六種元素,已知B原子最外層電子數是A原子次外層電子數的3倍,是D原子最外層電子數的2倍;C原子內層電子總數是最外層電子數10倍;A、B、D三種元素的原子最外層電子數之和為13;A和B原子最外層電子數之和與D和F原子最外層電子數之和相等;D和E是相鄰兩種元素。回答下列問題:
(1)E元素的名稱: ;其在元素周期表中的位置是 。
(2)AB2的結構式 ;B的氫化物中原子個數比1:1化合物的電子式 。
(3)A和E元素的最高價含氧酸的酸性較強的是 ;(填化學式)
(4)B、C、D、F四種元素原子半徑由大到小的順序是 (填元素符號),離子半徑最小的是 (填離子符號)。
(5)A、B、C三種元素組成原子個數比為nA:nB:nC=1:3:2的化合物,將足量AB2通入該化合物溶液中反應的離子方程式是 。
(6)短周期元素M與D元素位于不同主族,根據對角線規則二者某些性質相似。將M的最高價氧化物溶于C的最高價氧化物對應的水化物溶液中,發生反應的離子方程式為 。
(7)E和F形成的化合物X在高溫條件下可以被氫氣還原,工業上常用此反應制取高純度的單質E,寫出該化學反應的方程式 。
【答案】(14分)(1)硅;第三周期第IV族;(2)C=O=C;![]() ;(3)H2CO3;
;(3)H2CO3;
(4)Na>Al>Cl>O;Al3+;(5)CO2+CO32-+2H2O=2HCO3-;
(6)BeO+2OH-=BeO22-+H2O;(7)SiCl4+2H2Si+4HCl↑。
【解析】試題分析:已知B原子最外層電子數是A原子次外層電子數的3倍,是D原子最外層電子數的2倍,說明B元素最外層電子數為6,D原子最外層電子數為3,A的次外層電子數為2;C原子內層電子總數是最外層電子數10倍,則C為Na;A、B、D三種元素的原子最外層電子數之和為13,則A的最外層為13-6-3=4,所以A的核外電子數為2+4=6為C元素;A和B原子最外層電子數與D和F原子最外層電子數之和相等,則F的最外層為7,F的原子序數最大,應為Cl元素;D和E是相鄰兩種元素,D原子最外層電子數為3,所以D為Al元素,E為Si元素;B元素最外層電子數為6,且原子序數比Na,則為O元素,綜上可知:A為C元素,B為O元素,C為Na元素,D為Al元素,E為Si元素,F為Cl元素。(1)已知E為Si元素,則其其在元素周期表中的位置是第三周期第IV族;(2)AB2是CO2,其結構式是O=C=O;B的氫化物中原子個數比1:1化合物是H2O2,其電子式是![]() ;(3)A和E元素的非金屬性C>Si,所以二者最高價含氧酸的酸性較強的是H2CO3;(4)同一周期的元素,原子序數越大,原子半徑越小,不同周期的元素,原子核外電子層數越多,原子半徑越大,所以B、C、D、F四種元素原子半徑由大到小的順序是Na>Al>Cl>O;,對于電子層結構相同的離子來說,核電荷數越大,離子半徑就越小,因此上述元素形成的離子中,離子半徑最小的是Al3+;(5)由A、B、C三種元素組成原子個數比nA:nB:nC=1:3:2的化合物為Na2CO3,將足量CO2通入該化合物溶液中反應產生NaHCO3,反應的離子方程式是CO2+CO32-+2H2O=2HCO3-;(6)短周期元素M與D元素位于不同主族,根據對角線規則二者某些性質相似。將M的最高價氧化物溶于C的最高價氧化物對應的水化物溶液中,則M是Be元素,M的最高價氧化物BeO與NaOH溶液發生反應的離子方程式為BeO+2OH-=BeO22-+H2O;(7)E和F形成的化合物X是SiCl4,在高溫條件下可以被氫氣還原產生Si單質及HCl,工業上常用此反應制取高純度的單質E,該化學反應的方程式SiCl4+2H2Si+4HCl↑。
;(3)A和E元素的非金屬性C>Si,所以二者最高價含氧酸的酸性較強的是H2CO3;(4)同一周期的元素,原子序數越大,原子半徑越小,不同周期的元素,原子核外電子層數越多,原子半徑越大,所以B、C、D、F四種元素原子半徑由大到小的順序是Na>Al>Cl>O;,對于電子層結構相同的離子來說,核電荷數越大,離子半徑就越小,因此上述元素形成的離子中,離子半徑最小的是Al3+;(5)由A、B、C三種元素組成原子個數比nA:nB:nC=1:3:2的化合物為Na2CO3,將足量CO2通入該化合物溶液中反應產生NaHCO3,反應的離子方程式是CO2+CO32-+2H2O=2HCO3-;(6)短周期元素M與D元素位于不同主族,根據對角線規則二者某些性質相似。將M的最高價氧化物溶于C的最高價氧化物對應的水化物溶液中,則M是Be元素,M的最高價氧化物BeO與NaOH溶液發生反應的離子方程式為BeO+2OH-=BeO22-+H2O;(7)E和F形成的化合物X是SiCl4,在高溫條件下可以被氫氣還原產生Si單質及HCl,工業上常用此反應制取高純度的單質E,該化學反應的方程式SiCl4+2H2Si+4HCl↑。


科目:高中化學 來源: 題型:
【題目】在下列物質的溶液中分別加入一定量Na2O2的固體,不會出現渾濁想象的是
A..飽和Na2CO3溶液 B.Ca(HCO3)2稀溶液 C.Na2SO3稀溶液 D.飽和FeCl3溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為測定某有機化合物A的結構,進行如下實驗:
I.分子式的確定:
(1)將一定量有機物A置于氧氣流中充分燃燒,實驗測得:生成3.6g H2O和8.8g CO2,消耗氧氣5.6L(標準狀況下),則該物質中各元素的原子個數比是_______________。
(2)用質譜儀測定該有機化合物的相對分子質量,得到如圖①所示質譜圖,由此確定該物質的分子式是______________。
(3)根據價鍵理論,預測A的可能結構有________種。
II.結構式的確定:
(4)核磁共振氫譜能對有機物分子中不同化學環境的氫原子給出不同的峰值(信號),根據峰值(信號)可以確定分子中氫原子的種類和數目。例如:甲基氯甲基醚(ClCH2OCH3)有兩種氫原子如圖②。經測定,有機物A的核磁共振氫譜示意圖如圖③,則A的結構簡式為_________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)用惰性電極電解CuSO4溶液(如圖的裝置),
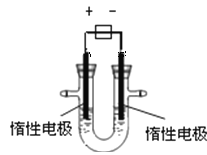
該過程中電解池電極反應式為是陽極: , 陰極: 。
(2)若電解池中裝入足量溶液,當陰極增重3.2g時,停止通電,此時陽極產生氣體的體積(標準狀況)為 (假設氣體全部逸出)。
(3)欲使電解液恢復到起始狀態,應向溶液中加入適量的
A.CuSO4 B.H2O C.CuO D.CuSO4·5H2O
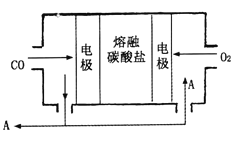
(4)用Na2CO3熔融鹽作電解質,CO、O2為原料組成的新型電池的研究取得了重大突破。該電池示意圖如右:負極電極反應式為_________________________,為了使該燃料電池長時間穩定運行,電池的電解質組成應保持穩定,電池工作時必須有部分A物質參加循環。A物質的化學式為__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組為了探究醋酸的電離情況,進行了如下實驗。
探究濃度對醋酸電離程度的影響
用pH計測定25 ℃時不同濃度的醋酸的pH,其結果如下:
醋酸濃度/(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列問題:
(1)寫出醋酸的電離方程式:___________________________________________。
(2)醋酸溶液中存在的微粒有________________________________________。
(3)根據表中數據,可以得出醋酸是弱電解質的結論,你認為得出此結論的依據是________________________________________________________________________。
(4)從表中的數據,還可以得出另一結論:隨著醋酸濃度的減小,醋酸的電離程度將(填“增大”、“減小”或“不變”)__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室中某些氣體的制取、收集及尾氣處理裝置如圖所示(省略夾持和凈化裝置)。僅用此裝置和表中提供的物質完成相關實驗,最合理的選項是( )

選項 | a中的物質 | b中的物質 | c中收集的氣體 | d中的物質 |
A | 濃氨水 | CaO | NH3 | H2O |
B | 濃硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 稀硫酸 | CaCO3[ | CO2 | NaOH溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com