
| A. | 根據氣體的相對分子質量,不可以比較相同狀況下氣體密度的大小 | |
| B. | 根據甲烷和乙烷的熔點,不能比較二者晶體中的分子間作用力的大小 | |
| C. | 比較同主族金屬元素原子半徑的大小,可以推斷元素的金屬性強弱 | |
| D. | 根據液體密度的大小,可以判斷液體的揮發性的強弱 |
分析 A.相同條件下,氣體摩爾體積相等,根據ρ=$\frac{M}{{V}_{m}}$判斷密度與相對分子質量關系;
B.分子晶體中,分子晶體的熔沸點與分子間作用力成正比;
C.同一周期元素,原子半徑隨著原子序數增大而減小,元素的金屬性隨著原子序數增大而減弱;
D.液體的揮發性與沸點有關.
解答 解:A.相同條件下,氣體摩爾體積相等,根據ρ=$\frac{M}{{V}_{m}}$知,相同條件下摩爾質量與密度成正比,故A錯誤;
B.分子晶體中,分子晶體的熔沸點與分子間作用力成正比,甲烷和乙烷都是分子晶體,可以通過其熔點比較二者晶體中的分子間作用力的大小,故B錯誤;
C.同一周期元素,原子半徑隨著原子序數增大而減小,元素的金屬性隨著原子序數增大而減弱,所以比較同周期金屬元素原子半徑的大小,可以推斷元素的金屬性強弱,故C正確;
D.液體的揮發性與沸點有關,沸點越低,越易揮發,液體物質揮發性與密度無關,故D錯誤;
故選C.
點評 本題考查較綜合,涉及摩爾質量與密度關系、分子晶體熔沸點影響因素、元素周期律等知識點,明確各個物理量之間關系是解本題關鍵,注意:分子晶體熔沸點與分子間作用力及氫鍵有關,與化學鍵強弱無關,易錯選項是BD.


科目:高中化學 來源: 題型:選擇題
| A. | 降低溫度可加快該反應速率 | |
| B. | 加入合適的催化劑可提高該反應速率 | |
| C. | 達到平衡時,v(正)=v(逆)=0 | |
| D. | 達到平衡時,H2O2轉化率為100% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度,v(正)增大,v(逆)減小 | |
| B. | 增加C的量,反應速率增大,轉化率增大 | |
| C. | 恒溫恒壓,再充入N2,平衡不發生移動 | |
| D. | 恒溫恒容,再充入CO,最終逆反應速率增大,正反應速率也增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石油分餾可得到汽油、煤油和柴油等產品 | |
| B. | 石油的催化重整可得到芳香烴 | |
| C. | 石油裂解主要是為了得到更多的汽油 | |
| D. | 煤、石油、天然氣是不可再生的一次能源 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2的生成速率與NH3的分解速率相等 | |
| B. | 單位時間內生成nmolN2的同時生成3nmolH2 | |
| C. | N2、H2、NH3的濃度不再發生變化 | |
| D. | N2、H2、NH3的物質的量之比為1:3:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
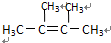 .
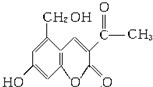
.
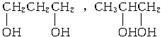
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
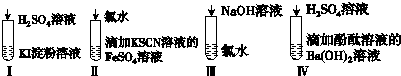
| 選項 | 現象 | 離子方程式 |
| A | I在空氣中放置一段時間后,溶液呈藍色 | 4I-+O2+2H2O═2I2+4OH- |
| B | II溶液由淺綠色變為紅色 | Fe2++Cl2═Fe3++2Cl- Fe3++3SCN-═Fe(SCN)3 |
| C | III溶液 顏色無變化 | Cl2+2OH-═Cl-+ClO-+H2O |
| D | IV有白色沉淀生成,溶液由紅色變無色 | Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com