
���}Ŀ������98%�ĝ�����(g��1.84g��cm��3)���Ƴɝ�Ȟ�0.5mol��L��1��ϡ����500ml��
(1)�x�õ���Ҫ�x���У�
��__________����__________����__________����____________����____________��
(2)Ո�����и������������_����̖���ڙM���ϡ�
A������Ͳ��ȡ��H2SO4 |
B��������u�� |
C�����z�^�ιܼ����sˮ���̶Ⱦ� |
D��ϴ�����Ãx�� |
E��ϡጝ�H2SO4
F������Һ�D(zhu��n)������ƿ
��������_���������______________________��
(3)��Ҫ�ش����І��}��
�������������w�e��____________mL��
������������15mL��20mL��50mL����Ͳ���x��____________mL����Ͳ��ã���ȡ�r�l(f��)�F(xi��n)��Ͳ���Ƀ���ˮϴ����ֱ����ȡ��ʹ?ji��)�?/span>__________(��ƫ��������ƫ���������oӰ���)
�����������؟�����(n��i)������ע��ʢˮ�ğ����У����ò��������������Ŀ����____________���������^������Һ�w�R���Y(ji��)����ʹ?ji��)���?/span>____________��
�����D(zhu��n)������ƿǰ������Һ�w��____________����t��ʹ?ji��)���?/span>____________����ϴ������Ͳ�����2��3�Σ�ϴ��ҺҲҪ�D(zhu��n)������ƿ����t��ʹ?ji��)�?/span>____________��
�����ݕr���ʹ��Һ��Һ���c�̶Ⱦ����У�����ҕ��ʹ?ji��)�?/span>____________����ҕ�tʹ?ji��)�?/span>___________��
���𰸡���1����Ͳ ���� ������ ����ƿ��500ml�� �z�^�ι� ��2��AEFDCB ��3����13.6
��15 ��ʹ�������r�ؔUɢ���� ����s���Ҝأ��ߣ�ƫ�ͣ����ߣ���
��������ԇ�}��������1���������E��Ӌ�㡢��ȡ��ϡጡ�ϴ�졢���ݡ��u��Ȳ�����һ������Ͳ��ȡ�����ᣬ�ڟ�����ϡጣ�������Ͳ��ȡˮ��������������ò��������裮��s���D(zhu��n)�Ƶ�500mL����ƿ�У����ò�����������ϴ�������������2��3�Σ�����ϴ��Һ��������ƿ�У���ˮ��Һ����x�̶Ⱦ�1��2cm�r�������z�^�ιܵμӣ��������u����������x������Ͳ����������������500mL����ƿ���z�^�ιܣ�
��2������(j��)���Ʋ��E��Ӌ�㡢��ȡ��ϡጡ���s����Һ��ϴ�졢���ݡ��u���bƿ��֪���_�IJ�������ǣ�AEFDCB��
��3��������������|(zh��)������Ȟ�c=![]() =
=![]() =18.4mol/L���O��Ҫ�ĝ������~�w�e��VmL������(j��)��Һϡጶ���C��V��=CϡVϡ��֪��18.4mol/L��VmL=0.5molL-1��500mL�����V=13.6mL��
=18.4mol/L���O��Ҫ�ĝ������~�w�e��VmL������(j��)��Һϡጶ���C��V��=CϡVϡ��֪��18.4mol/L��VmL=0.5molL-1��500mL�����V=13.6mL��
������(j��)�����������ԭ�t������(j��)��Ҫ��ȡ�ĝ�������w�e��13.6mL��֪�x��15mL��Ͳ��
�����������؟�����(n��i)������ע��ʢˮ�ğ����У����ò��������������Ŀ����ʹ�������r�ؔUɢ���������^������Һ�w�R�����t�������|(zh��)�p�٣��Y(ji��)����ʹ?ji��)��ƫ�ͣ?/span>
�����D(zhu��n)������ƿǰ������Һ�w����s���Ҝأ���t�ضȽ��ͺ���Һ�w�e�pС����ʹ?ji��)��ƫ�ߣ���ϴ������Ͳ����?/span>2��3�Σ�ϴ��ҺҲҪ�D(zhu��n)������ƿ����t���|(zh��)�p�٣���ʹ?ji��)��ƫ�͡?/span>
�����ݕr���ʹ��Һ��Һ���c�̶Ⱦ����У�����ҕ��ʹҺ����ڵĿ��ģ����ƫ�ߣ��t��ˮ����ƫ���ˣ�������Һ�ĝ�ȕ�ƫ�͡�


 �n�n�����Kϵ�д�
�n�n�����Kϵ�д� �����ЌW�n�r���I(y��)ϵ�д�
�����ЌW�n�r���I(y��)ϵ�д� ��������n�r��Ӗϵ�д�
��������n�r��Ӗϵ�д� �㽭���n�����SĿ�˜y�u�n�r��Ӗϵ�д�
�㽭���n�����SĿ�˜y�u�n�r��Ӗϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���^����������Ҫ����������߀ԭ����������������������Ư�ȡ�ij���W�dȤС�Mͬ�W.���@���^�������_չ���{(di��o)���о��c��
I.�{(di��o)��
(1)�^�����䳣����������������Ư�ȷ������Ҫԭ���� ��
(2)�Ƃ��^������Ŀǰ��õ����һ�������������Ҫ�^�̿������D��ʾ�����^�����cPd����ͬ���õ����|(zh��)�� (�����Q����

��.����(w��n)���Ԍ���о�
��3������̽���ضȡ����������l���� H2O2�ķֽ����ʵ�Ӱ푣�ij�dȤС�Mͬ�W�OӋ���������M������(sh��)��(j��)�ѽ�(j��ng)����������С�
��̖ | T/X | H202��ʼ���/moL�� L-1 | FeCl3��ʼ���/ moL�� L-1 moL�� L-1L-1 |
I | 20 | 1.0 | |
II | 50 | 1.0 | 0 |
III | 50 | 0.1 |
�����I�����о�___________���ֽ����ʵ�Ӱ푣�����������о��������ֽ����ʵ�Ӱ푣��t�������H2O2��ʼ��ȑ��� moL�� L-1��
�����M����зֽ������������� (�̖����
III.�^�����京���Č��y��
�dȤС�Mͬ�W��0.100 0 moL��L-1���Ը��i��⛘˜���Һ�ζ�ԇ�����^������ĺ���������ԭ��� 2MnO4- +5H2O2 +6H+ =2Mn2+ +8H2O+5O2��
��4���ζ����_�K�c�ĬF(xi��n)����_ ��
��5������Һ����ȡ25.00 mLԇ�������F��ƿ�У��؏͵ζ��ĴΣ�ÿ�����ĵ�KMnO4 �˜���Һ�w�e���±���ʾ��
��һ�� | �ڶ��� | ������ | ���Ĵ� | |
�w�e(mL) | 17.10 | 18.10 | 18.00 | 17.90 |
Ӌ��ԇ�����^������ĝ�Ȟ�__________moL��L-1 (������λ��Ч��(sh��)�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ƽ���ҕ�@ʾ�����a(ch��n)�^���Юa(ch��n)�������ďU������ĩ����SiO2��Fe2O3��CeO2��FeO�����|(zh��)����ij�n�}С�M�Դ˷�ĩ��ԭ�ϣ��OӋ���¹�ˇ���̌��YԴ�M�л��գ��õ�Ce(OH)4�������F�@�\��

��֪��
�������ԗl���£����ˮ��Һ����Ce3+��Ce4+�ɷN��Ҫ������ʽ��Ce3+��ˮ����Ce4+���^�������ԣ�
����CeO2������ϡ���
���������F�@�\��Fe2(SO4) 3��(NH4) 2SO4��24H2O�ݏV������ˮ�ă���̎����
��1���VҺA����Ҫ�ɷ� ������Wʽ����
��2���������������x�ӷ���ʽ ��
��3��������֮ǰҪϴ��V��B�����V��B�M��ϴ��Č����������� ��
��4��ϡ��Ԫ�ص��ἃ��߀�ɲ�����ȡ������֪������HT������ȡ���܌���x�ӏ�ˮ��Һ����ȡ�������^�̱�ʾ��Ce2(SO4)3 (ˮ��)+ 6HT(�ЙC��)![]() 2CeT3 (�ЙC�ӣ�+3H2SO4(ˮ��) ����Һ�õ�CeT3 (�ЙC�ӣ����ټ���H2SO4 �@���^���ĺ�Ce3+��ˮ��Һ�����x������������ȡ����ԭ���� ��
2CeT3 (�ЙC�ӣ�+3H2SO4(ˮ��) ����Һ�õ�CeT3 (�ЙC�ӣ����ټ���H2SO4 �@���^���ĺ�Ce3+��ˮ��Һ�����x������������ȡ����ԭ���� ��
��5���õζ����y���Ƶõ�Ce(OH)4�a(ch��n)Ʒ���ȡ�
![]()
����FeSO4��Һ�ڿ՚���¶��һ�Εr�g�����M�еζ����t�y��ԓCe(OH)4�a(ch��n)Ʒ���|(zh��)���֔�(sh��) �����ƫ����ƫС���oӰ푡���
��6����֪Fe3+������pH������2.2��3.2��F(xi��n)e2+������pH������5.8��7.9��Zn2+������pH������5.8��11.0��pH>11�rZn(OH)2������NaOH��Һ����[Zn(OH)4]2�����F(xi��n)��FeSO4��Һ������ZnSO4�s�|(zh��)�����Ƃ������F�@�\������п��x�õ�ԇ���� KMnO4��Һ��30%H2O2�� NaOH��Һ���ʯ��ˮ��ϡH2SO4��Һ��ϡ�}�ᡣ
���E���Ξ飺
����ZnSO4�s�|(zh��)��FeSO4��Һ�У�����������NaOH��Һ��pH>11�� ��
�� ��
�������еõ�����Һ�м��������@��Һ�� ���^�V��ϴ�졢�������ɣ��������F�@���w(NH4) Fe(SO4)2��12H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��������Һ�У����|(zh��)������Ȟ�1 mol��L��1����(����)
A����40 g NaOH����1 Lˮ���õ���Һ
B����80 g SO3����ˮ�����1 L����Һ
C����0.5 mol��L��1 NaNO3��Һ100 mL�ӟ����l(f��)��50 gˮ����Һ
D����K�� 2 mol��K2SO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���������|(zh��)����늽��|(zh��)����
A. ���� B. Br2 C. BaSO4 D. �������c��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ���F(xi��n)��mgij���w�������pԭ�ӷ��Ә�(g��u)�ɣ�����Ħ���|(zh��)����Mg/mol���������ӵ��_����(sh��)��NA��ʾ���t��
(1)ԓ���w�����|(zh��)������________mol��
(2)ԓ���w����ԭ�ӿ���(sh��)��________����
(3)ԓ���w�ژ˜ʠ�r�µ��w�e��________L��
(4)ԓ���w����1Lˮ��(�����]����)������Һ�����|(zh��)���|(zh��)���֔�(sh��)��____________���O��Һ���ܶȞ��g/cm3���tԓ��Һ�����|(zh��)������Ȟ�__________mol��L��1��
(5)ԓ���w����ˮ���γ�VL��Һ������Һ�����|(zh��)������Ȟ�________mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ��ij�dȤС�M�OӋ��D��ʾ����b�ã����r�Ȕ��_K2���]��K1���ɘO���К��ݮa(ch��n)����һ�Εr�g���_K1���]��K2���l(f��)�F(xi��n)�����Aָ�ƫ�D(zhu��n)���������P�������_����

A�����_K2���]��K1�r���������x�ӷ���ʽ�飺2H+ + 2Cl����Cl2��+H2��
B�����_K2���]��K1�r��ʯī늘O������Һ׃�t
C�����_K1���]��K2�r���~늘O�ϵ�늘O�����飺 Cl2+2e����2Cl��
D�����_K1���]��K2�r��ʯī늘O�����O
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
���}Ŀ�����ЈDʾ�c�����Ĕ����������
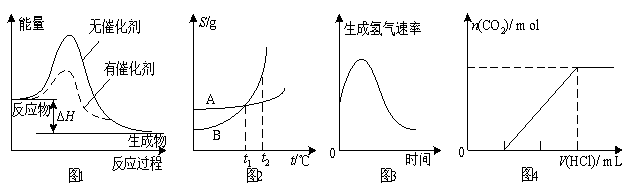
A���D1��ʾij�şᷴ���քe���С��o��������r�·����^���е�����׃��
B���D2��ʾA��B�����|(zh��)���ܽ���S�ض�׃����r����t1��rA��B�����Һ�քe������t2��r�����|(zh��)���|(zh��)���֔�(sh��)B��A
C���D3��ʾ�V�l�����}�������ɚ�������S�r�g��׃��������������ʼӿ��ԭ�������ԓ������şᷴ��
D���D4��ʾ�ں������|(zh��)����NaOH��Na2CO3�Ļ����Һ�еμ�0.1 mol��L��1�}�����^���r���a(ch��n)�����w���w�e�c�����}����Pϵ
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com