
【題目】(1)寫出NaHSO4在水中的電離方程式_____。
(2)粗鹽中含可溶性CaCl2、MgCl2及一些硫酸鹽,要除去這些雜質,可選用以下試劑:①Na2CO3、②NaOH、③BaCl2,則試劑加入的先后順序是_____(填序號)。
(3)實驗證明銅不能在低溫下與O2反應,也不能與稀H2SO4共熱發生反應,但工業上卻是將廢銅屑倒入熱的稀H2SO4中并通入空氣來制備CuSO4溶液的,則銅屑在此狀態下被溶解的化學方程式為___________。
【答案】NaHSO4=Na++H++SO42- ②③①或③②① 2Cu+2H2SO4(稀)+O2![]() 2CuSO4+2H2O
2CuSO4+2H2O
【解析】
(1)NaHSO4在水中完全電離生成鈉離子、氫離子和硫酸根離子;
(2)鹽中含可溶性CaCl2、MgCl2及一些硫酸鹽,先除去鎂離子或硫酸根離子,再除去鈣離子,過濾后,最后加鹽酸,據此進行分析;
(3)銅與稀硫酸、氧氣反應生成硫酸銅和水。
(1)NaHSO4在水中完全電離生成鈉離子、氫離子和硫酸根離子,電離方程式為NaHSO4=Na++H++SO42-;
(2)粗鹽中含可溶性CaCl2、MgCl2及一些硫酸鹽,先加入②氫氧化鈉溶液除去鎂離子或加入③氯化鋇溶液除去硫酸根離子,再加入適量①除去除去鈣離子以及過量的鋇離子,然后過濾除去難溶物,最后加鹽酸,除去過量的碳酸鈉、氫氧化鈉,所以試劑的順序為②③①或③②①;
(3)將廢銅屑倒入熱的稀H2SO4中并通入空氣來制備CuSO4溶液,反應的化學方程式為2Cu+2H2SO4(稀)+O2![]() 2CuSO4+2H2O。
2CuSO4+2H2O。


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:
【題目】25℃某二元堿B(OH)2水溶液中,B2+、B(OH)+和B(OH)2三者各自的物質的量分數δ隨溶液pH的變化曲線如圖所示,下列說法錯誤的是(已知多元堿的電離是逐級進行的)
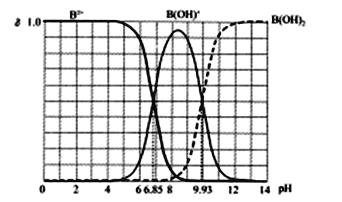
A. Kb2[B(OH)2]的數量級為10-8
B. 在B(OH)Cl溶液中c(OH-)>c(H+)
C. 等物質的量的BCl2和B(OH)Cl混合溶液中δ(B2+)<δ[B(OH)+]
D. B(OH)Cl溶液中,若c[B(OH)2]+2c(B2+)+c(H+)-c(OH-),則δ[B(OH)2]=δ[B(OH)+]
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高鐵酸鉀(K2FeO 4)是一種新型、高效、多功能水處理劑,下列反應可制取K2FeO4:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6□+8H2O。下列說法不正確的是
A. 每轉移1mole-,可以得到33g K2FeO4
B. □處的物質應為KCl
C. 該反應中鐵元素的化合價升高
D. 氧化性:Cl2>K2FeO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通過以下反應均可獲取CO。下列有關說法正確的是
①木炭不完全燃燒制CO:2C(s)+O2(g)=2CO(g) ΔH1=-221kJ·mol-1
②木炭還原CO2制CO:C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
③焦炭還原Fe2O3制CO:Fe2O3(s) + 3C(s) ![]() 2Fe(s) + 3CO(g) ΔH 3=+489.0kJ·mol-1
2Fe(s) + 3CO(g) ΔH 3=+489.0kJ·mol-1
A. 反應①中化學能全部轉化為熱能
B. 反應②為吸熱反應,在任何情況下都不能自發進行
C. 反應③中使用催化劑或移走部分CO,均可提高Fe2O3的轉化率
D. 反應Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) ΔH =-28.5 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電池的“理論比能量”指單位質量的電極材料理論上能釋放的最大電能。“金屬(M)空氣電池”(如下圖)具有原料易得、能量密度高等優點。該類電池放電的總反應方程式為:4M+nO2+2nH2O=4M(OH) n。下列說法不正確的是
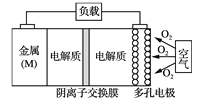
A. “金屬(M)空氣電池”放電過程的正極反應式: O2+2H2O+4e-=4OH-
B. 比較Mg、Al、Zn三種“金屬—空氣電池”,“Al—空氣電池”的理論比能量最高
C. 電解質溶液中的陰離子從負極區移向正極區
D. 在“M—空氣電池”中,為防止負極區沉積Mg(OH)2,宜采用中性電解質及陽離子交換膜
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知有下列反應:
①2H2O+Cl2+SO2===H2SO4+2HCl
②2KMnO4+16HCl(濃) ===2KCl+2MnCl2+5Cl2↑+8H2O
根據上述兩個反應回答:
(1)Cl2、KMnO4、H2SO4三者氧化性強弱順序為______________,Cl-、SO2、Mn2+三者還原性強弱順序為___________。
(2)反應①中氧化產物和還原產物的質量之比為________。
(3)反應②中濃鹽酸表現出的性質是________。
A.還原性 B.酸性 C.氧化性
(4)用雙線橋法標出反應②電子轉移的方向和數目_________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)我國首創以鋁_空氣_海水電池作為能源的新型的海水標志燈,以海水為電解質溶液,靠空氣中的氧氣使鋁不斷氧化而產生電流,只要把燈放入海水數分鐘,就會發出耀眼的白光。則電源的負極材料是________,負極反應為_____________;正極材料是__________,正極反應為_______________。
(2)熔鹽電池具有高的發電效率,因而受到重視, 可用Li2CO3和Na2CO3的熔融鹽混合物作電解質,CO為陽極燃氣,空氣與CO2的混合氣為陰極助燃氣,制得在650 ℃下工作的燃料電池,完成有關電池反應式。陽極反應式:2CO+2CO![]() -4e-===4CO2,陰極反應式:____________,電池總反應式:____________ 。
-4e-===4CO2,陰極反應式:____________,電池總反應式:____________ 。
(3)離子液體是一種室溫熔融鹽,為非水體系,由有機陽離子、Al2Cl7—和AlCl4—組成的離子液體作電解液時,可在鋼制品上電鍍鋁。鋼制品應接電源的________極,已知電鍍過程中不產生其他離子且有機陽離子不參與電極反應,陰極電極反應式為_______________。若改用AlCl3水溶液作電解液,則陰極產物為_________。
(4) “鎂-次氯酸鹽”燃料電池的裝置如圖所示,該電池的正極反應式為_________________。
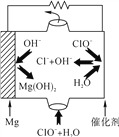
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量與滴入NaOH溶液的體積關系如右圖所示,則原混合液中Al2(SO4)3與MgSO4的物質的量濃度之比為( )

A. 6:1 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋅銅原電池裝置如圖所示,其中陽離子交換膜只允許陽離子和水分子通過,下列有關敘述正確的是( )
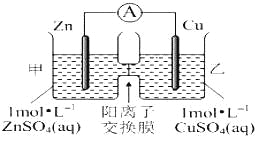
A. 銅電極上發生氧化反應
B. 電池工作一段時間后,甲池的C(SO42-)減小
C. 電池工作一段時間后,乙池溶液的總質量增加
D. 陽離子通過交換膜向正極移動,陰離子通過交換膜向負極移動,保持溶液中電荷平衡
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com