
【題目】工業上利用電解飽和食鹽水生產氯氣(Cl2)、燒堿和氫氣的化學方程式是:2NaCl + 2H2O![]() 2NaOH + Cl2↑+ H2↑
2NaOH + Cl2↑+ H2↑
(1)用雙線橋表示出電子轉移的方向和數目______________,題干中反應改寫成離子方程式是___________________________________
(2)電解食鹽水的過程中,氧化產物是__________________________________
(3)電解食鹽水要求對粗食鹽水進行精制,以除去粗食鹽水中含有的泥沙和SO42-、Ca2+,Mg2+等雜質離子。精制時依次加入氯化鋇溶液、純堿、燒堿,充分反應后過濾,在濾液中加入鹽酸中和至中性。鹽酸與濾液反應的離子方程式:____________________________
【答案】  2Cl-+2H2O
2Cl-+2H2O![]() 2OH- +Cl2↑+ H2↑ 氯氣(或Cl2) H++OH-
2OH- +Cl2↑+ H2↑ 氯氣(或Cl2) H++OH-![]() H2O CO32- +2H+
H2O CO32- +2H+ ![]() CO2↑+ H2O
CO2↑+ H2O
【解析】(1)電解氯化鈉溶液時,生成1mol氯氣需要2mol電子,生成1mol氫氣需要2mol電子,所以其轉移電子數是2,電子轉移方向和數目為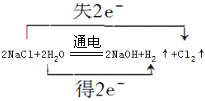 ,離子方程式為:2Cl-+2H2O
,離子方程式為:2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑,故答案為:
2OH-+Cl2↑+H2↑,故答案為: ;2Cl-+2H2O
;2Cl-+2H2O![]() 2OH-+Cl2↑+H2↑;
2OH-+Cl2↑+H2↑;
(2)反應2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑中,化合價升高的Cl元素被氧化,生成氯氣,氯氣為氧化產物,故答案為:氯氣(或Cl2);
2NaOH+Cl2↑+H2↑中,化合價升高的Cl元素被氧化,生成氯氣,氯氣為氧化產物,故答案為:氯氣(或Cl2);
(3)電解食鹽水要求對粗食鹽水進行精制,以除去粗食鹽水中含有的泥沙和SO42-、Ca2+,Mg2+等雜質離子。精制時依次加入氯化鋇溶液,除去硫酸根離子;加入純堿,除去鈣離子和過量的鋇離子;加入燒堿,除去鎂離子,充分反應后過濾,濾液中主要含有過量的碳酸鈉和氫氧化鈉,加入鹽酸中和至中性,反應的離子方程式有H++OH-=H2O、CO32- +2H+ =CO2↑+ H2O,故答案為:H++OH-=H2O、CO32- +2H+ =CO2↑+ H2O。


 開心練習課課練與單元檢測系列答案
開心練習課課練與單元檢測系列答案科目:高中化學 來源: 題型:
【題目】參考下列(a)~(c)項回答問題:
(a)皂化值是使1g油脂皂化所需要的KOH的毫克數.
(b)碘值是使100g油脂加成碘的克數.
(c)各種油脂的皂化值、碘值列表如下:
花生油 | 亞麻仁油 | 牛油 | 黃油 | 硬化大豆油 | 大豆油 | |
皂化值 | 190 | 180 | 195 | 226 | 193 | 193 |
碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(1)單純由(C17H33COO)3C3H5(相對分子質量884)形成的油,皂化值是
(2)在橫線上填入適當的詞句:
亞麻仁油比花生油所含的多,黃油比牛油的小.硬化大豆油的碘值小的原因是 .
(3)為使碘值為180的魚油100g硬化所需要的H2的體積為升(標準狀況下)?
(4)結構簡式為 ![]() 的酯,若皂化值為430,求n為 .
的酯,若皂化值為430,求n為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO、NO2等有毒氣體的轉化以及氮的化合物合成、應用及氮的固定一直是科學研究的熱點。
(1)以CO2與NH3為原料合成化肥尿素[CO(NH2)2]的主要反應如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) △H= -159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) △H=akJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g) △H= -86.98kJ·mol-1
則a=_______。
(2)反應2NH3(g)+CO2(g)![]() CO(NH2)2(1)+H2O(g),在合成塔中進行。右圖中I、II、III三條曲線為合成塔中按不同氨碳比和水碳比投料時二氧化碳轉化率的情況。曲線I、II、III水碳比的數值分別為:
CO(NH2)2(1)+H2O(g),在合成塔中進行。右圖中I、II、III三條曲線為合成塔中按不同氨碳比和水碳比投料時二氧化碳轉化率的情況。曲線I、II、III水碳比的數值分別為:
I.0.6~0.7 II.1~1.1 III.1.5~1.61
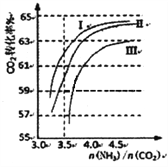
生產中應選用水碳比的數值為__________(選填序號)。
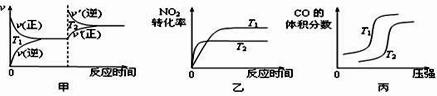
(3)4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1 ,對于該反應,溫度不同(T2>T1)、其他條件相同時,下列圖像正確的是_____(填代號)。
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1 ,對于該反應,溫度不同(T2>T1)、其他條件相同時,下列圖像正確的是_____(填代號)。
(4)用活性炭還原法也可以處理氮氧化物,某研究小組向某密閉容器加入一定量的活性炭和NO,發生反應C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH在T1℃時,反應進行到不同時間測得各物質的量濃度如下:
N2(g)+CO2(g) ΔH在T1℃時,反應進行到不同時間測得各物質的量濃度如下:
濃度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①30min后,只改變某一條件,根據上表的數據判斷改變的條件可能是_______(填字母代號)。
a.加入一定量的活性炭 b.通入一定量的NO
c.適當縮小容器的體積 d.加入合適的催化劑
②若30min后升高溫度至T2℃,達到平衡時,容器中NO、N2、CO2的濃度之比為5:3:3,則達到新平衡時NO的轉化率_________(填“升高”或“降低”),ΔH___________0(填“>”或“<”).
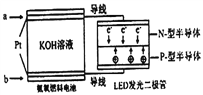
(5)一種氨燃料電池,使用的電解質溶液是2mol/L的KOH溶液。電池反應為:4NH3+3O2=2N2+6H2O;請寫出通入a氣體一極的電極反應式為____________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】咖啡酸具有止血功效,存在于多種中藥中,其結構簡式如圖:則下列有關說法正確的是( ) 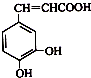
A.該物質中苯環上一氯代物有2種
B.1 mol該物質可以與1.5 mol碳酸鈉溶液反應生成1.5 mol CO2
C.既能發生取代反應,也能發生加成反應
D.所有碳原子不可能都在同一個平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E、F六種元素為原子序數依次增大的短周期元素。A為原子半徑最小的元素,A和B可形成4原子10電子的分子X;C的最外層電子數是內層的3倍;D原子的最外層電子數是最內層電子數的一半;E是地殼中含量最多的金屬元素;F元素的最高正價與最低負價代數和為6。請回答下列問題:
(1)A和C按原子個數比1∶1形成4原子分子Y,Y的結構式是___________。
(2)分子X的電子式是__________;D可以在液態X中發生類似于與A2C的反應,寫出反應的化學方程式_________________________________。
(3)實驗證明,熔融的EF3 不導電,其原因是_______________________。
(4)E的單質可溶于A、C、D形成的化合物Z的水溶液中。拉曼光譜證實此反應生成的陰離子主要以E(CA)4- 的形式存在,寫出E溶于Z溶液的離子方程式:_____________________。
(5)工業品Z的溶液中含有某些含氧酸根雜質,可用離子交換膜法電解提純。電解槽內裝有陽離子交換膜(只允許陽離子通過),其工作原理如圖所示。
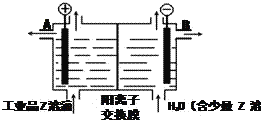
①該電解槽的陽極反應式是_________________。
②通電開始后,陰極附近溶液pH___________(“增大”、“減小”或“不變”)。
③除去雜質后的Z溶液從液體出口_________(填寫“A”或“B”)導出。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究人員最近發現了一種“水”電池,這種電池能利用淡水與海水之間含鹽量差別進行發電,在海水中電池總反應可表示為: ![]() 。下列“水”電池在海水中放電時的有關說法正確的是( )
。下列“水”電池在海水中放電時的有關說法正確的是( )
A. ![]() 是還原產物 B.
是還原產物 B. ![]() 不斷向“水”電池的負極移動
不斷向“水”電池的負極移動
C. 正極反應式: ![]() D. 每生成
D. 每生成![]() 轉移
轉移![]() 電子
電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組混合物,不能用分液漏斗分開的是( ) ①四氯化碳、水 ②乙醇、甘油 ③乙醇、水 ④苯、水 ⑤已烷、水 ⑥環已烷、苯 ⑦溴苯、水.
A.①②③
B.②③⑥
C.①④⑤⑦
D.④⑤⑥
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com