
| A. | C2H5OH在電池的負極上參加反應 | |
| B. | 在外電路中電子由負極沿導線流向正極 | |
| C. | 1mol乙醇被氧化轉移6mol電子 | |
| D. | 電解質溶液中陽離子移向正極,陰離子移向負極 |
分析 A、在燃料電池中,燃料在負極發生失電子的反應,
B、在外電路中,電子從負極流向正極;
C、根據氧化還原反應中化合價的升降來判斷電子的轉移;
D、原電池中陽離子移向正極,陰離子移向負極.
解答 解:A、在燃料電池中,燃料乙醇在負極發生失電子的反應,故A正確;
B、在燃料電池的外電路中,電子由負極沿導線流向正極,和電流的流向相反,故B正確;
C、根據電池反應:C2H5OH+3O2=2CO2+3H2O,反應轉移電子數為12,所以1mol乙醇被氧化時就有12mol電子轉移,故C錯誤;
D、原電池中陽離子移向正極,陰離子移向負極,故D正確;
故選C.
點評 本題考查學生燃料電池的工作原理知識,可以根據燃料電池的電極反應規律知識進行回答,難度不大.


 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:解答題
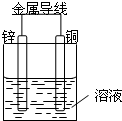 將Zn棒和Cu棒用導線連接后,放入某電解質溶液中,構成如圖所示裝置.試回答下列問題:
將Zn棒和Cu棒用導線連接后,放入某電解質溶液中,構成如圖所示裝置.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化石能源物質內部蘊儲著大量的能量 | |
| B. | 綠色植物進行光合作用時,將太陽能轉化為化學能“貯存”起來 | |
| C. | 物質的化學能可以在不同條件下轉為熱能、電能為人類所利用 | |
| D. | 我國經濟發展要全部依靠化石能源 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Li是負極,電極反應為Li+e-=Li+ | |
| B. | Li是正極,電極反應為Li+e-=Li- | |
| C. | MnO2是負極,電極反應為MnO2+e-=MnO2- | |
| D. | 鋰電池是一種環保型電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某小組用如圖所示裝置對Cl2與Na2S2O3的反應進行探究(氣密性已檢驗).
某小組用如圖所示裝置對Cl2與Na2S2O3的反應進行探究(氣密性已檢驗).| 操作 | 現象 |
| 打開分液漏斗活塞,滴加一定量濃鹽酸,加熱 | i.A中有黃綠色氣體生成,C中液面上方有白霧,溶液中開始出現少量渾濁; ii.一段時間后,C中產生大量黃色沉淀. |
| 用濕潤的淀粉碘化鉀試紙檢驗C中白霧 | 淀粉碘化鉀試紙變藍 |
| C中濁液過濾后,取少量濾液用鹽酸酸化,滴加氯化鋇溶液 | 有白色沉淀生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (代號DMP)是一種常用的酯類塑化劑,其蒸氣對氫氣的相對密度為97.工業上生產DMP的流程如圖所示:
(代號DMP)是一種常用的酯類塑化劑,其蒸氣對氫氣的相對密度為97.工業上生產DMP的流程如圖所示:
 的名稱1,2-二甲苯(或鄰二甲苯),D的核磁共振氫譜有3組峰,DMP的分子式為C10H10O4.
的名稱1,2-二甲苯(或鄰二甲苯),D的核磁共振氫譜有3組峰,DMP的分子式為C10H10O4. .
.
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 弱電解質化學式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 電離平衡常數 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 | 1.8×l0-5 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com